El desarrollo del sistema nervioso en los seres humanos, o desarrollo neuronal, o neurodesarrollo involucra los estudios de embriología , biología del desarrollo y neurociencia . Estos describen los mecanismos celulares y moleculares mediante los cuales se forma el complejo sistema nervioso en los humanos, se desarrolla durante el desarrollo prenatal y continúa desarrollándose posnatalmente.
Algunos hitos del desarrollo neuronal en el embrión incluyen:
Normalmente, estos procesos de desarrollo neurológico se pueden dividir en dos clases:
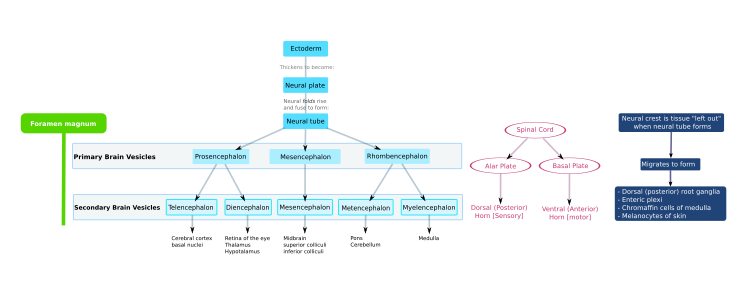
El sistema nervioso central (SNC) se deriva del ectodermo , la capa de tejido más externa del embrión. En la tercera semana del desarrollo embrionario humano aparece el neuroectodermo y forma la placa neural a lo largo del lado dorsal del embrión. La placa neural es la fuente de la mayoría de las neuronas y células gliales del SNC. Se forma un surco a lo largo del eje longitudinal de la placa neural y, en la cuarta semana de desarrollo, la placa neural se envuelve sobre sí misma para dar origen al tubo neural , que se llena de líquido cefalorraquídeo (LCR). [1] A medida que el embrión se desarrolla, la parte anterior del tubo neural forma tres vesículas cerebrales primarias , que se convierten en las regiones anatómicas primarias del cerebro: el prosencéfalo ( prosencéfalo ), el mesencéfalo ( mesencéfalo ) y el rombencéfalo ( rombencéfalo ). [2] Estas vesículas tempranas simples se agrandan y se dividen en cinco vesículas cerebrales secundarias : el telencéfalo (futuros corteza cerebral y ganglios basales ), diencéfalo (futuros tálamo e hipotálamo ), mesencéfalo (futuros colículos ), metencéfalo (futuros puentes y cerebelo) . ) y mielencéfalo (futura médula ). [3] La cámara central llena de LCR es continua desde el telencéfalo hasta la médula espinal y constituye el sistema ventricular en desarrollo del SNC. Debido a que el tubo neural da lugar al cerebro y la médula espinal, cualquier mutación en esta etapa del desarrollo puede provocar deformidades fatales como la anencefalia o discapacidades de por vida como la espina bífida . Durante este tiempo, las paredes del tubo neural contienen células madre neurales , que impulsan el crecimiento del cerebro a medida que se dividen muchas veces. Poco a poco algunas de las células dejan de dividirse y se diferencian en neuronas y células gliales , que son los principales componentes celulares del SNC. [2] Las neuronas recién generadas migran a diferentes partes del cerebro en desarrollo para autoorganizarse en diferentes estructuras cerebrales. Una vez que las neuronas han alcanzado sus posiciones regionales, extienden los axones.y dendritas , que les permiten comunicarse con otras neuronas a través de sinapsis . La comunicación sináptica entre neuronas conduce al establecimiento de circuitos neuronales funcionales que median en el procesamiento sensorial y motor y subyacen al comportamiento. [4]
Durante el desarrollo embrionario temprano , el ectodermo se especifica para dar origen a la epidermis (piel) y la placa neural. La conversión de ectodermo indiferenciado en neuroectodermo requiere señales del mesodermo . Al inicio de la gastrulación, las presuntas células mesodérmicas se mueven a través del labio dorsal del blastoporo y forman una capa entre el endodermo y el ectodermo. Estas células mesodérmicas que migran a lo largo de la línea media dorsal dan lugar a una estructura llamada notocorda . Las células ectodérmicas que recubren la notocorda se desarrollan hasta formar la placa neural en respuesta a una señal difusible producida por la notocorda. El resto del ectodermo da origen a la epidermis (piel). La capacidad del mesodermo para convertir el ectodermo suprayacente en tejido neural se denomina inducción neural.
La placa neural se pliega hacia afuera durante la tercera semana de gestación para formar el surco neural . A partir de la futura región del cuello, los pliegues neurales de este surco se cierran para formar el tubo neural . La formación del tubo neural a partir del ectodermo se llama neurulación . La parte ventral del tubo neural se llama placa basal ; la parte dorsal se llama placa alar . El interior hueco se llama canal neural . Al final de la cuarta semana de gestación, los extremos abiertos del tubo neural, llamados neuroporos, se cierran. [5]
Un labio de blastoporo trasplantado puede convertir el ectodermo en tejido neural y se dice que tiene un efecto inductivo. Los inductores neuronales son moléculas que pueden inducir la expresión de genes neuronales en explantes de ectodermo sin inducir también genes mesodérmicos. La inducción neuronal se estudia a menudo en embriones de xenopus , ya que tienen un patrón corporal simple y existen buenos marcadores para distinguir entre tejido neural y no neural. Ejemplos de inductores neuronales son las moléculas noggin y chordin .
Cuando las células ectodérmicas embrionarias se cultivan a baja densidad en ausencia de células mesodérmicas, se someten a diferenciación neural (expresan genes neurales), lo que sugiere que la diferenciación neural es el destino predeterminado de las células ectodérmicas. En los cultivos de explantes (que permiten interacciones directas entre células), las mismas células se diferencian en epidermis. Esto se debe a la acción de BMP4 (una proteína de la familia TGF-β ) que induce a los cultivos ectodérmicos a diferenciarse en epidermis. Durante la inducción neural, el mesodermo dorsal (notocorda) produce noggin y cordina y se difunden hacia el ectodermo suprayacente para inhibir la actividad de BMP4. Esta inhibición de BMP4 hace que las células se diferencien en células neurales. La inhibición de la señalización de TGF-β y BMP (proteína morfogenética ósea) puede inducir eficientemente tejido neural a partir de células madre pluripotentes humanas , [6] un modelo de desarrollo humano temprano.
A finales de la cuarta semana, la parte superior del tubo neural se flexiona al nivel del futuro mesencéfalo: el mesencéfalo . Por encima del mesencéfalo está el prosencéfalo (futuro prosencéfalo) y debajo está el rombencéfalo (futuro rombencéfalo). La vesícula óptica (que eventualmente se convertirá en el nervio óptico, la retina y el iris) se forma en la placa basal del prosencéfalo.
La médula espinal se forma a partir de la parte inferior del tubo neural. La pared del tubo neural está formada por células neuroepiteliales, que se diferencian en neuroblastos y forman la capa del manto (la materia gris). Las fibras nerviosas emergen de estos neuroblastos para formar la capa marginal (la sustancia blanca). La parte ventral de la capa del manto (las placas basales) forma las áreas motoras de la médula espinal, mientras que la parte dorsal (las placas alares) forma las áreas sensoriales. Entre las placas basal y alar hay una capa intermedia que contiene neuronas del sistema nervioso autónomo. [7]
En la quinta semana, la placa alar del prosencéfalo se expande para formar los hemisferios cerebrales (el telencéfalo ). La placa basal se convierte en el diencéfalo .
El diencéfalo, el mesencéfalo y el rombencéfalo constituyen el tronco encefálico del embrión. Continúa flexionándose en el mesencéfalo. El rombencéfalo se pliega hacia atrás, lo que hace que su placa alar se ensanche y forme el cuarto ventrículo del cerebro. La protuberancia y el cerebelo se forman en la parte superior del rombencéfalo, mientras que el bulbo raquídeo se forma en la parte inferior.
La neuroimagen es responsable de grandes avances en la comprensión de cómo se desarrolla el cerebro. EEG y ERP son procesos de obtención de imágenes eficaces que se utilizan principalmente en bebés y niños pequeños, ya que son más suaves. Por lo general, a los bebés se les realiza la prueba con fNIRS . La resonancia magnética y la resonancia magnética funcional se utilizan ampliamente para la investigación del cerebro debido a la calidad de las imágenes y el análisis que permiten.
Las resonancias magnéticas son útiles para analizar muchos aspectos del cerebro. La relación de transferencia de magnetización (MTR) mide la integridad mediante magnetización. La anisotropía fraccional (FA) mide la organización mediante la difusión de moléculas de agua. Además, la difusividad media (MD) mide la fuerza de los tractos de materia blanca . [8]
Utilizando la resonancia magnética estructural, se puede realizar una evaluación cuantitativa de una serie de procesos de desarrollo, incluida la definición de patrones de crecimiento [9] y la caracterización de la secuencia de mielinización. [10] Estos datos complementan la evidencia de los estudios de imágenes con tensor de difusión (DTI) que se han utilizado ampliamente para investigar el desarrollo de la materia blanca.
Test de fMRI que mentaliza, que es la teoría de la mente mediante la activación de una red. El surco temporal superior posterior (pSTS) y la unión temporoparietal (TPJ) son útiles para predecir el movimiento. En adultos, el pSTS derecho mostró una mayor respuesta que la misma región en adolescentes cuando se probó la causalidad intencional. Estas regiones también se activaron durante el ejercicio "mente en los ojos", donde las emociones deben juzgarse en función de diferentes imágenes de los ojos. Otra región clave es la corteza temporal anterior (ATC) en la región posterior. En adultos, el ATC izquierdo mostró una mayor respuesta que la misma región en adolescentes cuando se sometieron a pruebas emocionales de mentalización. Finalmente, la corteza prefrontal medial (MPFC) y la corteza dorsal anterior (dMPFC) se activan cuando la mente es estimulada por la psicología. [8]
Las imágenes de mayor resolución han permitido que la ecografía tridimensional ayude a identificar el desarrollo del cerebro humano durante las etapas embrionarias. Los estudios informan que se forman tres estructuras primarias en la sexta semana de gestación . Estos son el prosencéfalo , el mesencéfalo y el rombencéfalo , también conocidos como prosencéfalo, mesencéfalo y rombencéfalo respectivamente. Cinco estructuras secundarias de estas en la séptima semana gestacional. Estos son el telencéfalo, diencéfalo, mesencéfalo, metencéfalo y mielencéfalo que luego se convierten en los ventrículos laterales, el tercer ventrículo, el acueducto y las partes superior e inferior del cuarto ventrículo desde el telencéfalo hasta el mielencéfalo, durante la edad adulta. Las imágenes por ultrasonido en 3D permiten representaciones in vivo del desarrollo cerebral ideal que pueden ayudar a reconocer irregularidades durante la gestación. [11]
Mediante resonancia magnética, los estudios demostraron que mientras la materia blanca aumenta desde la niñez (~9 años) hasta la adolescencia (~14 años), la materia gris disminuye. Esto se observó principalmente en las cortezas frontal y parietal. Las teorías sobre por qué ocurre esto varían. Una idea es que la mielinización intracortical combinada con un mayor calibre axonal aumenta el volumen de tejido de sustancia blanca. Otra es que la reorganización sináptica se produce a partir de la proliferación y luego de la poda. [8]
El aumento y la caída del volumen de materia gris en los lóbulos frontal y parietal alcanzó su punto máximo alrededor de los 12 años de edad. El pico para los lóbulos temporales fue de ~17 años, siendo la corteza temporal superior la última en madurar. Las regiones sensoriales y motoras maduraron primero, después de lo cual se desarrolló el resto de la corteza. Esto se caracterizó por la pérdida de materia gris y ocurrió desde la región posterior a la anterior. Esta pérdida de materia gris y aumento de materia blanca puede ocurrir a lo largo de la vida, aunque los cambios más intensos ocurren desde la niñez hasta la adolescencia. [8]
La migración neuronal es el método por el cual las neuronas viajan desde su origen o lugar de nacimiento hasta su posición final en el cerebro. Sus medios de migración más comunes son la migración radial y tangencial.
Las células madre neurales proliferan en la zona ventricular del neocórtex en desarrollo . Las primeras células posmitóticas que migran desde la preplaca y están destinadas a convertirse en células de Cajal-Retzius y neuronas de subplaca . Estas células lo hacen por translocación somal. Las neuronas que migran con este modo de locomoción son bipolares y unen el borde delantero del proceso a la piamadre . Luego, el soma se transporta a la superficie pial mediante nucleokenisis, un proceso mediante el cual una "jaula" de microtúbulos alrededor del núcleo se alarga y se contrae en asociación con el centrosoma para guiar el núcleo hasta su destino final. [12] Las fibras radiales (también conocidas como glía radial) pueden trasladarse a la placa cortical y diferenciarse en astrocitos o neuronas . [13] [ cita necesaria ] La translocación somal puede ocurrir en cualquier momento durante el desarrollo. [14]
Las ondas posteriores de neuronas dividen la preplaca migrando a lo largo de fibras gliales radiales para formar la placa cortical. Cada ola de células migratorias viaja más allá de sus predecesoras formando capas de adentro hacia afuera, lo que significa que las neuronas más jóvenes son las más cercanas a la superficie. [15] [16] Se estima que la migración guiada por glial representa entre el 80% y el 90% de las neuronas migratorias. [17]
Muchas neuronas que migran a lo largo del eje anteroposterior del cuerpo utilizan tractos axónicos existentes para migrar en un proceso llamado migración axófila. [18] Un ejemplo de este modo de migración son las neuronas que expresan GnRH , que realizan un largo viaje desde su lugar de nacimiento en la nariz, a través del prosencéfalo y hasta el hipotálamo. [19] Muchos de los mecanismos de esta migración se han resuelto, comenzando con las señales de guía extracelulares [20] que desencadenan la señalización intracelular. Estas señales intracelulares, como la señalización del calcio , conducen a la dinámica citoesquelética de actina [21] y microtúbulos [22] , que producen fuerzas celulares que interactúan con el entorno extracelular a través de proteínas de adhesión celular [23] para provocar el movimiento de estas células. La migración neurofílica se refiere a la migración de neuronas a lo largo de un axón que pertenece a un nervio diferente. La migración gliofílica es la migración de la glía a lo largo de fibras gliales. [24]
La mayoría de las interneuronas migran tangencialmente a través de múltiples modos de migración para alcanzar su ubicación apropiada en la corteza. Un ejemplo de migración tangencial es el movimiento de las células de Cajal-Retzius dentro de la zona marginal del neuroepitelio cortical. [25]
También existe un método de migración neuronal llamado migración multipolar . [26] [27] Esto se observa en las células multipolares, que están abundantemente presentes en la zona intermedia cortical . No se parecen a las células que migran por locomoción o translocación somal. En cambio, estas células multipolares expresan marcadores neuronales y extienden múltiples procesos delgados en varias direcciones independientemente de las fibras gliales radiales. [26]
Los factores neurotróficos son moléculas que promueven y regulan la supervivencia neuronal en el sistema nervioso en desarrollo. Se distinguen de los metabolitos ubicuos necesarios para el mantenimiento y el crecimiento celular por su especificidad; cada factor neurotrófico promueve la supervivencia de sólo ciertos tipos de neuronas durante una etapa particular de su desarrollo. Además, se ha argumentado que los factores neurotróficos están implicados en muchos otros aspectos del desarrollo neuronal, desde la guía axonal hasta la regulación de la síntesis de neurotransmisores. [28]
El neurodesarrollo en el sistema nervioso adulto incluye mecanismos como la remielinización , la generación de nuevas neuronas , la glía , los axones , la mielina o las sinapsis . La neuroregeneración se diferencia entre el sistema nervioso periférico (SNP) y el sistema nervioso central (SNC) por los mecanismos funcionales y, especialmente, por la extensión y velocidad.
El sistema nervioso continúa desarrollándose durante la edad adulta hasta la muerte cerebral . [ se necesitan citas adicionales ] Por ejemplo:
Las investigaciones, los tratamientos y las políticas a menudo distinguen entre cerebros "maduros" y cerebros "en desarrollo", mientras que los científicos han señalado que "la naturaleza compleja del neurodesarrollo en sí plantea desafíos para establecer un punto de referencia que indique cuándo un cerebro está maduro" y que varios Las medidas estructurales del cerebro cambian constantemente a lo largo de la fase adulta de la vida, [34] aunque es posible que no se vuelvan a alcanzar los niveles de neuroplasticidad infantil [ cita necesaria ] y se cree que existen varios períodos críticos y sensibles en el desarrollo del cerebro. [35]
El aprendizaje suele ser más eficiente en los niños y lleva más tiempo o es más difícil con la edad . Un estudio que utilizó neuroimagen identificó el aumento rápido del neurotransmisor GABA como un componente potencial importante para explicar por qué esto es así. [36] [37]
Los cerebros de los niños contienen más " sinapsis silenciosas " que están inactivas hasta que se reclutan como parte de la neuroplasticidad y el aprendizaje o los recuerdos flexibles . [38] [39] La neuroplasticidad aumenta durante los períodos críticos o sensibles del desarrollo del cerebro, refiriéndose principalmente al desarrollo del cerebro durante el desarrollo infantil . [40]
Lo que los humanos aprenden en las primeras etapas y lo que aprenden a aplicar marca el rumbo de la vida o tiene un impacto desproporcionado. [41] Los adultos suelen tener una mayor capacidad para seleccionar lo que aprenden, en qué medida y cómo. Por ejemplo, los niños pueden aprender determinadas materias y temas del plan de estudios escolar a través de la transcripción escrita a mano en la pizarra del aula , en lugar de poder elegir temas/habilidades o trabajos específicos para aprender y los estilos de aprendizaje. Por ejemplo, es posible que los niños no hayan desarrollado intereses consolidados, ética, interés en propósitos y actividades significativas, conocimiento sobre los requisitos, demandas y prioridades del mundo real.En las primeras etapas del desarrollo (antes del nacimiento y durante los primeros meses), el cerebro sufre más cambios de tamaño, forma y estructura que en cualquier otro momento de la vida. Una mejor comprensión del desarrollo cerebral durante este período crítico es importante para mapear el crecimiento normal y para investigar los mecanismos de lesión asociados con factores de riesgo de mal desarrollo, como el nacimiento prematuro. Por lo tanto, existe la necesidad de una cobertura densa de este rango de edad con un atlas que varíe en el tiempo y dependa de la edad. Estos atlas espacio-temporales pueden representar con precisión los cambios dinámicos que ocurren durante el desarrollo temprano del cerebro [9] y pueden usarse como un espacio de referencia normativo.
Además, se han realizado estudios de expresión genética a gran escala de diferentes regiones del cerebro desde la gestación temprana hasta el envejecimiento. Este tipo de datos proporciona una visión única de los cambios que ocurren en el cerebro durante este largo período. Este enfoque demostró que el 86 por ciento de los genes se expresaban y que el 90 por ciento de ellos estaban regulados diferencialmente a nivel de transcripción completa o de exón en todas las regiones del cerebro y/o en el tiempo. La mayoría de estas diferencias espacio-temporales se detectaron antes del nacimiento, con aumentos posteriores en la similitud entre los transcriptomas regionales. Además, las diferencias interrealistas exhiben un patrón temporal de reloj de arena, que divide el desarrollo neocortical humano en tres fases principales. Durante la primera fase, en los primeros seis meses después de la concepción, la arquitectura general de las regiones del cerebro está formada en gran medida por un estallido de actividad genética, que es distinta para regiones específicas de la neocorteza. A este subidón le sigue una especie de intermedio que comienza en el tercer trimestre del embarazo. Durante este período, la mayoría de los genes que están activos en regiones específicas del cerebro se silencian, excepto los genes que estimulan las conexiones entre todas las regiones del neocórtex. Luego, al final de la infancia y al principio de la adolescencia, la orquesta genética comienza de nuevo y ayuda a dar forma sutil a las regiones del neocórtex que progresivamente realizan tareas más especializadas, un proceso que continúa hasta la edad adulta. [42] [43] [44]
Los enfoques para investigar la organogénesis y el desarrollo temprano del cerebro o sistema nervioso humano incluyen:
La inaccesibilidad a los tejidos humanos ha impedido la comprensión molecular de la formación de capacidades cognitivas. [45] También se investiga la placenta . [55] [56] [54]
Una mejor comprensión del desarrollo puede potencialmente permitir conocer las enfermedades del sistema nervioso, mejorar la inteligencia y una mejor protección contra los impactos dañinos de los factores identificados del desarrollo fetal (que potencialmente incluyen enfermedades de la madre, diversos eventos y xenobióticos ). [53] [54] [ se necesitan citas adicionales ]
La investigación ha podido realizar nuevos descubrimientos para varias partes del cerebro gracias a las imágenes no invasivas disponibles.
En esta región se observa más actividad en los adolescentes que en los adultos cuando se enfrentan a pruebas de tareas de mentalización, así como de intención comunicativa y personal. Disminución de la actividad desde la adolescencia hasta la edad adulta. En una tarea de mentalización que emplea animación, el dMPFC fue más estimulado en adultos mientras que el MPFC ventral fue más estimulado en niños. Se pueden atribuir al uso de una estrategia objetiva asociada con el dMPFC. Las teorías sobre la disminución de la actividad desde la adolescencia hasta la edad adulta varían. Una teoría es que la estrategia cognitiva se vuelve más automática con la edad y otra es que el cambio funcional ocurre paralelo al cambio neuroanatómico que se caracteriza por la sinaptogénesis y la poda. [8]
El MPFC es un ejemplo de una región específica que se ha comprendido mejor utilizando las técnicas de imagen actuales. La investigación actual proporciona muchos más hallazgos como este.
El estrés en la vida temprana se define como la exposición a circunstancias durante la niñez que abruman los recursos de afrontamiento del niño y conducen a períodos sostenidos de estrés. [57] Los resultados de múltiples estudios indican que los efectos del estrés en los primeros años de vida en el cerebro en desarrollo son significativos e incluyen, entre otros, los siguientes: aumento del volumen de la amígdala, [58] [59] disminución de la actividad en el cerebro límbico y cortical frontal [60] y estructuras alteradas de la materia blanca. [61]
Se cree que el estrés en los primeros años de vida produce cambios en el desarrollo del cerebro al interferir con la neurogénesis, la producción sináptica y la poda de sinapsis y receptores. [57] La interferencia con estos procesos podría resultar en un aumento o disminución del volumen de la región cerebral, lo que podría explicar los hallazgos de que el estrés en la vida temprana se asocia con un aumento del volumen de la amígdala y una disminución del volumen de la corteza cingulada anterior. [58] [62]
De la literatura se han extraído varias conclusiones importantes. Las áreas del cerebro que experimentan un desarrollo posnatal significativo, como las involucradas en la memoria y las emociones, son más vulnerables a los efectos del estrés en los primeros años de vida. [57] [63] Por ejemplo, el hipocampo continúa desarrollándose después del nacimiento y es una estructura que se ve afectada por el maltrato infantil. [63] El estrés en los primeros años de vida parece interferir con la sobreproducción de sinapsis que es típica en la infancia, pero no interfiere con la poda sináptica en la adolescencia. Esto da como resultado volúmenes más pequeños del hipocampo, lo que podría explicar la asociación entre el estrés en los primeros años de vida y la reducción del volumen del hipocampo. [62] Esta reducción de volumen puede estar asociada con los déficits de regulación de las emociones observados en personas expuestas al estrés en los primeros años de vida.
La amígdala es particularmente vulnerable al estrés en los primeros años de vida. [57] La amígdala también experimenta un desarrollo significativo durante la infancia, se altera estructural y funcionalmente en individuos que han experimentado estrés en la vida temprana y se asocia con las dificultades socioemocionales relacionadas con el estrés en la vida temprana.
El tipo de receptor es otra consideración a la hora de determinar si una región del cerebro es sensible o no a los efectos del estrés en los primeros años de vida. Las regiones del cerebro con una alta densidad de receptores de glucocorticoides son especialmente vulnerables a los efectos del estrés en los primeros años de vida, probablemente porque los glucocorticoides se unen a estos receptores durante la exposición al estrés, facilitando el desarrollo de respuestas de supervivencia a costa de otras vías neuronales importantes. [63] Algunos ejemplos de regiones del cerebro con alta densidad de receptores de glucocorticoides son el hipocampo y el vermis cerebeloso. El estrés activa el eje HPA y da como resultado la producción de glucocorticoides. El aumento de la producción de glucocorticoides da como resultado una mayor activación de estas regiones del cerebro, lo que facilita el desarrollo de ciertas vías neuronales a costa de otras.
Las anomalías en la estructura y función del cerebro a menudo se asocian con déficits que pueden persistir durante años después de que se elimina el estrés y pueden ser un factor de riesgo para futuras psicopatologías. [57] Las regiones del cerebro más sensibles al estrés en los primeros años de vida son aquellas que experimentan cambios de desarrollo durante la exposición al estrés. Como resultado, el estrés altera la trayectoria de desarrollo de esa región del cerebro, produciendo alteraciones duraderas en la estructura y función.
Los tipos comunes de estrés en los primeros años de vida que están documentados incluyen el maltrato, la negligencia y la institucionalización previa. También se ha demostrado que vivir en la pobreza influye de manera similar en la función cerebral. [64]