Un alvéolo pulmonar ( pl.: alveoli , del latín alveolus , "pequeña cavidad"), también conocido como saco de aire o espacio aéreo , es una de las millones de cavidades huecas y distensibles en forma de copa en los pulmones donde tiene lugar el intercambio de gases pulmonares. [1] El oxígeno se intercambia por dióxido de carbono en la barrera sangre-aire entre el aire alveolar y el capilar pulmonar . [2] Los alvéolos forman el tejido funcional de los pulmones de los mamíferos conocido como parénquima pulmonar , que ocupa el 90 por ciento del volumen pulmonar total. [3] [4]
Los alvéolos se localizan primero en los bronquiolos respiratorios que marcan el comienzo de la zona respiratoria . Están ubicados escasamente en estos bronquiolos, recubren las paredes de los conductos alveolares y son más numerosos en los sacos alveolares ciegos . [5] Los acinos son las unidades básicas de la respiración, y el intercambio de gases tiene lugar en todos los alvéolos presentes. [6] La membrana alveolar es la superficie de intercambio de gases, rodeada por una red de capilares . El oxígeno se difunde a través de la membrana hacia los capilares y el dióxido de carbono se libera desde los capilares hacia los alvéolos para ser exhalado. [7] [8]
Los alvéolos son característicos de los pulmones de los mamíferos. En otros vertebrados intervienen estructuras diferentes en el intercambio de gases. [9]

Los alvéolos se localizan primero en los bronquiolos respiratorios como bolsas dispersas que se extienden desde sus luces. Los bronquiolos respiratorios recorren longitudes considerables y se vuelven cada vez más alveolados con ramas laterales de conductos alveolares que se recubren profundamente con alvéolos. Los conductos son entre dos y once en cada bronquiolo. [10] Cada conducto se abre en cinco o seis sacos alveolares en los que se abren grupos de alvéolos.
Cada unidad respiratoria terminal se denomina acino y está formada por los bronquiolos respiratorios, los conductos alveolares, los sacos alveolares y los alvéolos. Los alvéolos nuevos continúan formándose hasta los ocho años de edad. [5]
Un par típico de pulmones humanos contiene alrededor de 480 millones de alvéolos, [11] lo que proporciona una superficie total para el intercambio de gases de entre 70 y 80 metros cuadrados. [10] Cada alvéolo está envuelto en una fina malla de capilares que cubre aproximadamente el 70% de su área. [12] El diámetro de un alvéolo es de entre 200 y 500 μm . [12]
Un alvéolo está formado por una capa epitelial de epitelio escamoso simple (células muy delgadas y aplanadas), [13] y una matriz extracelular rodeada de capilares . El revestimiento epitelial es parte de la membrana alveolar, también conocida como membrana respiratoria, que permite el intercambio de gases . La membrana tiene varias capas: una capa de líquido de revestimiento alveolar que contiene surfactante , la capa epitelial y su membrana basal; un espacio intersticial delgado entre el revestimiento epitelial y la membrana capilar; una membrana basal capilar que a menudo se fusiona con la membrana basal alveolar, y la membrana endotelial capilar . Sin embargo, toda la membrana mide solo entre 0,2 μm en su parte más delgada y 0,6 μm en su parte más gruesa. [14]
En las paredes alveolares hay conductos de aire que interconectan los alvéolos, conocidos como poros de Kohn . El tabique alveolar que separa los alvéolos en el saco alveolar contiene algunas fibras de colágeno y fibras elásticas . Los tabiques también albergan la red capilar enredada que rodea cada alvéolo. [3] Las fibras elásticas permiten que los alvéolos se estiren cuando se llenan de aire durante la inhalación. Luego vuelven a su forma original durante la exhalación para expulsar el aire rico en dióxido de carbono.

Existen tres tipos principales de células alveolares . Dos tipos son los neumocitos o neumonocitos, conocidos como células tipo I y tipo II, que se encuentran en la pared alveolar, y una célula fagocítica grande conocida como macrófago alveolar que se mueve en los lúmenes de los alvéolos y en el tejido conectivo entre ellos. Las células tipo I, también llamadas neumocitos tipo I o células alveolares tipo I, son escamosas, delgadas y planas y forman la estructura de los alvéolos. Las células tipo II, también llamadas neumocitos tipo II o células alveolares tipo II, liberan surfactante pulmonar para reducir la tensión superficial y también pueden diferenciarse para reemplazar las células tipo I dañadas. [12] [15]
El desarrollo de las primeras estructuras que contendrán los alvéolos comienza el día 22 y se divide en cinco etapas: embrionaria, pseudoglandular, canalicular, sacular y alveolar. [16] La etapa alveolar comienza aproximadamente a las 36 semanas de desarrollo. Los alvéolos inmaduros aparecen como protuberancias de los sáculos que invaden los tabiques primarios. A medida que los sáculos se desarrollan, las protuberancias en los tabiques primarios se hacen más grandes; los nuevos tabiques son más largos y delgados y se conocen como tabiques secundarios. [16] Los tabiques secundarios son responsables de la división final de los sáculos en alvéolos. La mayor parte de la división alveolar ocurre dentro de los primeros 6 meses, pero continúa desarrollándose hasta los 3 años de edad. Para crear una barrera de difusión más delgada, la red capilar de doble capa se fusiona en una red, cada una asociada estrechamente con dos alvéolos a medida que se desarrollan. [16]
Durante los primeros tres años de vida, el agrandamiento de los pulmones es una consecuencia del aumento del número de alvéolos; después de este punto, tanto el número como el tamaño de los alvéolos aumentan hasta que el desarrollo de los pulmones finaliza aproximadamente a los 8 años de edad. [16]
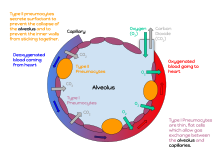


Las células de tipo I son las más grandes de los dos tipos de células; son células de revestimiento epitelial delgadas y planas (neumocitos membranosos), que forman la estructura de los alvéolos. [3] Son escamosas (lo que le da más área de superficie a cada célula) y tienen largas extensiones citoplasmáticas que cubren más del 95% de la superficie alveolar. [12] [17]
Las células de tipo I participan en el proceso de intercambio de gases entre los alvéolos y la sangre . Estas células son extremadamente delgadas, a veces de tan solo 25 nm. Se necesitó un microscopio electrónico para demostrar que todos los alvéolos están revestidos de epitelio . Este revestimiento delgado permite una rápida difusión del intercambio de gases entre el aire de los alvéolos y la sangre en los capilares circundantes.
El núcleo de una célula de tipo I ocupa una gran superficie de citoplasma libre y sus orgánulos se agrupan a su alrededor, lo que reduce el grosor de la célula. Esto también mantiene reducido al mínimo el grosor de la barrera sangre-aire .
El citoplasma de la porción delgada contiene vesículas pinocíticas que pueden desempeñar un papel en la eliminación de contaminantes particulados pequeños de la superficie exterior. Además de los desmosomas , todas las células alveolares de tipo I tienen uniones oclusivas que evitan la fuga de líquido tisular hacia el espacio aéreo alveolar.
La relativamente baja solubilidad (y por lo tanto la velocidad de difusión) del oxígeno requiere una gran superficie interna (aproximadamente 80 m2 [96 yardas cuadradas]) y paredes muy delgadas de los alvéolos. Entre los capilares y ayudando a sostenerlos hay una matriz extracelular , un tejido en forma de malla de fibras elásticas y colágenas. Las fibras de colágeno, al ser más rígidas, dan firmeza a la pared, mientras que las fibras elásticas permiten la expansión y contracción de las paredes durante la respiración.
Los neumocitos de tipo I no pueden replicarse y son susceptibles a las agresiones tóxicas . En caso de daño, las células de tipo II pueden proliferar y diferenciarse en células de tipo I para compensar. [18]
Las células de tipo II son cuboidales y mucho más pequeñas que las de tipo I. [3] Son las células más numerosas en los alvéolos, pero no cubren tanta superficie como las células escamosas de tipo I. [18] Las células de tipo II (neumocitos granulosos) en la pared alveolar contienen orgánulos secretores conocidos como cuerpos lamelares o gránulos lamelares, que se fusionan con las membranas celulares y secretan surfactante pulmonar . Este surfactante es una película de sustancias grasas, un grupo de fosfolípidos que reducen la tensión superficial alveolar . Los fosfolípidos se almacenan en los cuerpos lamelares. Sin este recubrimiento, los alvéolos colapsarían. El surfactante se libera continuamente por exocitosis . La reinflación de los alvéolos después de la exhalación se facilita gracias al surfactante, que reduce la tensión superficial en el revestimiento fino de líquido de los alvéolos . El recubrimiento de líquido es producido por el cuerpo para facilitar la transferencia de gases entre la sangre y el aire alveolar, y las células de tipo II se encuentran típicamente en la barrera sangre-aire . [19] [20]
Las células de tipo II comienzan a desarrollarse alrededor de las 26 semanas de gestación y secretan pequeñas cantidades de surfactante. Sin embargo, no se secretan cantidades adecuadas de surfactante hasta alrededor de las 35 semanas de gestación; esta es la razón principal del aumento de las tasas de síndrome de dificultad respiratoria infantil , que se reduce drásticamente a edades superiores a las 35 semanas de gestación.
Las células de tipo II también son capaces de división celular, dando lugar a más células alveolares de tipo I y II cuando el tejido pulmonar está dañado. [21]
MUC1 , un gen humano asociado con los neumocitos tipo II, ha sido identificado como un marcador en el cáncer de pulmón . [22]
La importancia de las células alveolares pulmonares tipo 2 en el desarrollo de síntomas respiratorios graves de COVID-19 y los posibles mecanismos por los que estas células están protegidas por los ISRS fluvoxamina y fluoxetina se resumieron en una revisión en abril de 2022. [23]
Los macrófagos alveolares residen en las superficies luminales internas de los alvéolos, los conductos alveolares y los bronquiolos. Son carroñeros móviles que sirven para engullir partículas extrañas en los pulmones, como polvo, bacterias, partículas de carbono y células sanguíneas de lesiones. [24] También se les llama macrófagos pulmonares y células del polvo . Los macrófagos alveolares también desempeñan un papel crucial en las respuestas inmunitarias contra patógenos virales en los pulmones. [25] Secretan citocinas y quimiocinas, que reclutan y activan otras células inmunitarias, inician la señalización del interferón tipo I e inhiben la exportación nuclear de genomas virales. [25]
La falta de surfactante en los alvéolos es una de las causas que pueden contribuir a la atelectasia (colapso de parte o todo el pulmón). Sin surfactante pulmonar , la atelectasia es una certeza. [26] La condición grave del síndrome de dificultad respiratoria aguda (SDRA) es causada por una deficiencia o disfunción del surfactante. [27] La falta de surfactante en los pulmones de los bebés prematuros causa el síndrome de dificultad respiratoria infantil (IRDS). La relación lecitina-esfingomielina es una medida del líquido amniótico fetal para indicar la madurez o inmadurez pulmonar. [28] Una relación baja indica un factor de riesgo para IRDS. La lecitina y la esfingomielina son dos de los glucolípidos del surfactante pulmonar.
La regulación deficiente del surfactante puede provocar una acumulación de proteínas surfactantes en los alvéolos, lo que se conoce como proteinosis alveolar pulmonar . Esto provoca un intercambio de gases deficiente. [29]
La neumonía es una enfermedad inflamatoria del tejido pulmonar , que puede ser causada tanto por virus como por bacterias . En respuesta a la infección, se liberan citocinas y líquidos en la cavidad alveolar, el intersticio o ambos, lo que hace que se reduzca la superficie efectiva de intercambio de gases. En casos graves en los que no se puede mantener la respiración celular , puede ser necesario administrar oxígeno suplementario . [30] [31]

Casi cualquier tipo de tumor o cáncer de pulmón puede comprimir los alvéolos y reducir la capacidad de intercambio de gases. En algunos casos, el tumor llenará los alvéolos. [33]
Una contusión pulmonar es un hematoma en el tejido pulmonar causado por un traumatismo. [35] Los capilares dañados por una contusión pueden provocar que la sangre y otros fluidos se acumulen en el tejido del pulmón, lo que perjudica el intercambio de gases.
El edema pulmonar es la acumulación de líquido en el parénquima y los alvéolos. El edema suele ser causado por una insuficiencia cardíaca del ventrículo izquierdo o por un daño en el pulmón o su vasculatura.
Debido a la alta expresión de la enzima convertidora de angiotensina 2 (ECA2) en las células alveolares tipo II, los pulmones son susceptibles a infecciones por algunos coronavirus, incluidos los virus que causan el síndrome respiratorio agudo severo (SARS) [36] y la enfermedad por coronavirus 2019 (COVID-19). [37]
{{cite journal}}: CS1 maint: DOI gratuito sin marcar ( enlace )