La prueba de Papanicolaou (abreviada como prueba de Papanicolaou , también conocida como prueba de Papanicolaou (AE), [1] citología cervical (BE), cribado cervical (BE), [2] o prueba de citología (BE)) es un método de cribado cervical utilizado para detectar procesos potencialmente precancerosos y cancerosos en el cuello uterino (abertura del útero o matriz) o, más raramente, en el ano (tanto en hombres como en mujeres). [3] Los hallazgos anormales a menudo van seguidos de procedimientos de diagnóstico más sensibles y, si se justifican, intervenciones que tienen como objetivo prevenir la progresión al cáncer de cuello uterino . La prueba fue inventada de forma independiente en la década de 1920 por el médico griego Georgios Papanikolaou y recibió su nombre. La obstetra canadiense Anna Marion Hilliard introdujo una versión simplificada de la prueba en 1957.
Una prueba de Papanicolaou se realiza abriendo la vagina con un espéculo y recolectando células en la abertura externa del cuello uterino en la zona de transformación (donde las células cervicales escamosas externas se encuentran con las células endocervicales glandulares internas), usando una espátula de Ayre o un citocepillo. Las células recolectadas se examinan bajo un microscopio para buscar anomalías. La prueba tiene como objetivo detectar cambios potencialmente precancerosos (llamados neoplasia intraepitelial cervical (NIC) o displasia cervical; el sistema de lesión intraepitelial escamosa (SIL) también se usa para describir anomalías) causados por el virus del papiloma humano , un virus de ADN de transmisión sexual . La prueba sigue siendo un método eficaz y ampliamente utilizado para la detección temprana de lesiones precancerosas y de cáncer de cuello uterino. Si bien la prueba también puede detectar infecciones y anomalías en el endocérvix y el endometrio , no está diseñada para hacerlo.
Las pautas sobre cuándo comenzar la prueba de Papanicolaou son variadas, pero generalmente comienzan en la edad adulta. Las pautas sobre la frecuencia varían de cada tres a cinco años. [4] [5] [6] Si los resultados son anormales, y dependiendo de la naturaleza de la anomalía, es posible que sea necesario repetir la prueba en seis a doce meses. [7] Si la anomalía requiere un examen más detenido, se puede derivar a la paciente para una inspección detallada del cuello uterino mediante colposcopia , que magnifica la vista de las superficies del cuello uterino, la vagina y la vulva. La persona también puede ser remitida a una prueba de ADN del VPH , que puede servir como complemento de la prueba de Papanicolaou. En algunos países, primero se analiza el ADN viral, antes de buscar células anormales. [8] Están evolucionando biomarcadores adicionales que pueden aplicarse como pruebas auxiliares con la prueba de Papanicolaou. [9]
Las pautas de detección varían de un país a otro. En general, las pruebas de detección comienzan alrededor de los 20 o 25 años y continúan hasta los 50 o 60 años aproximadamente . [12] Las pruebas de detección generalmente se recomiendan cada tres a cinco años, siempre que los resultados sean normales. [11]
El Congreso Estadounidense de Obstetras y Ginecólogos (ACOG) y otros recomiendan comenzar las pruebas de detección a los 21 años. [5] [15] Muchos otros países esperan hasta los 25 años o más para comenzar las pruebas de detección. Por ejemplo, algunas partes de Gran Bretaña comienzan a hacerse pruebas de detección a los 25 años. La recomendación general del ACOG es que las personas con órganos reproductivos femeninos de entre 30 y 65 años se sometan a un examen anual de bienestar femenino , que no se hagan pruebas de Papanicolaou anuales y que sí se hagan pruebas de Papanicolaou. pruebas a intervalos de tres a cinco años. [dieciséis]
El VPH se transmite a través del contacto de piel a piel; El sexo no tiene por qué ocurrir, aunque es una forma común de propagarse. [17] Se necesita un promedio de un año, pero puede tomar hasta cuatro años, para que el sistema inmunológico de una persona elimine la infección inicial. Las pruebas de detección durante este período pueden mostrar esta reacción y reparación inmunitaria como anomalías leves, que generalmente no están asociadas con el cáncer de cuello uterino, pero que podrían causar estrés a la paciente y dar lugar a más pruebas y un posible tratamiento. El cáncer de cuello uterino suele tardar en desarrollarse, por lo que retrasar unos años el inicio de las pruebas de detección plantea poco riesgo de pasar por alto una lesión potencialmente precancerosa. Por ejemplo, realizar pruebas de detección a personas menores de 25 años no reduce las tasas de cáncer menores de 30 años. [18]
El VPH se puede transmitir en las relaciones sexuales entre mujeres, por lo que aquellas que sólo han tenido relaciones sexuales con otras mujeres deben hacerse pruebas de detección, aunque tienen un riesgo algo menor de sufrir cáncer de cuello uterino. [19]
Las pautas sobre la frecuencia de las pruebas de detección varían: generalmente cada tres a cinco años para quienes no han tenido frotis anormales anteriormente. [11] Algunas recomendaciones anteriores sugerían realizar pruebas de detección con una frecuencia de uno a dos años; sin embargo, hay poca evidencia que respalde dicha detección frecuente; La evaluación anual tiene pocos beneficios, pero genera costos mucho mayores y muchos procedimientos y tratamientos innecesarios. [5] Desde antes de 1980 se reconoce que la mayoría de las personas pueden someterse a pruebas de detección con menos frecuencia. [20] En algunas directrices, la frecuencia depende de la edad; por ejemplo, en Gran Bretaña se recomienda realizar pruebas de detección cada tres años para las mujeres menores de 50 años y cada cinco años para las mayores. [21]
Las pruebas de detección deben suspenderse aproximadamente a los 65 años, a menos que haya antecedentes de resultados anormales en las pruebas o enfermedad. Probablemente no haya ningún beneficio en realizar pruebas de detección a personas de 60 años o más cuyas pruebas anteriores hayan sido negativas. [13] Si los últimos tres resultados de Papanicolaou de una mujer fueron normales, puede suspender la prueba a los 65 años, según USPSTF, ACOG, ACS y ASCP; [5] El NHS de Inglaterra dice 64. No es necesario continuar realizando pruebas de detección después de una histerectomía completa para detectar enfermedades benignas.
La prueba de Papanicolaou todavía se recomienda para quienes han sido vacunadas contra el VPH [11] , ya que las vacunas no cubren todos los tipos de VPH que pueden causar cáncer de cuello uterino. Además, la vacuna no protege contra la exposición al VPH antes de la vacunación. [22]
Las personas con antecedentes de cáncer de endometrio deben suspender las pruebas de Papanicolaou de rutina después de la histerectomía. [14] [23] Es poco probable que pruebas adicionales detecten la recurrencia del cáncer, pero conllevan el riesgo de dar resultados falsos positivos, lo que conduciría a pruebas adicionales innecesarias. [14]
Es posible que se necesiten pruebas de Papanicolaou más frecuentes para realizar un seguimiento después de una prueba de Papanicolaou anormal, después de un tratamiento por resultados anormales de Papanicolaou o de una biopsia, o después del tratamiento de un cáncer (cervical, anal, etc.). [24]
La prueba de Papanicolaou, cuando se combina con un programa regular de detección y seguimiento adecuado, puede reducir las muertes por cáncer de cuello uterino hasta en un 80%. [11]
El fracaso de la prevención del cáncer mediante la prueba de Papanicolaou puede ocurrir por muchas razones, incluida la falta de exámenes de detección regulares, la falta de un seguimiento adecuado de los resultados anormales y errores de muestreo e interpretación. [25] En los EE. UU., más de la mitad de todos los cánceres invasivos ocurren en mujeres que nunca se han realizado una prueba de Papanicolaou; entre el 10 y el 20% adicional de los cánceres ocurren en quienes no se han realizado una prueba de Papanicolaou en los cinco años anteriores. Aproximadamente una cuarta parte de los cánceres de cuello uterino en EE. UU. ocurrieron en personas que tuvieron una prueba de Papanicolaou anormal pero que no recibieron un seguimiento adecuado (el paciente no regresó para recibir atención médica o el médico no realizó las pruebas o el tratamiento recomendados). [ cita necesaria ]
No se ha demostrado que las pruebas de Papanicolaou prevengan el adenocarcinoma de cuello uterino. [25] En el Reino Unido, que tiene un programa de detección de prueba de Papanicolaou, el adenocarcinoma representa aproximadamente el 15% de todos los cánceres de cuello uterino. [26]
Las estimaciones sobre la eficacia del sistema de llamadas y retiros del Reino Unido varían ampliamente, pero puede evitar alrededor de 700 muertes por año en el Reino Unido. [27]
Múltiples estudios han realizado análisis de sensibilidad y especificidad en las pruebas de Papanicolaou. El análisis de sensibilidad captura la capacidad de las pruebas de Papanicolaou para identificar correctamente a las mujeres con cáncer de cuello uterino. Varios estudios han revelado que la sensibilidad de la prueba de Papanicolaou se sitúa entre el 47,19 y el 55,5%. [28] [29] [30] El análisis de especificidad captura la capacidad de las pruebas de Papanicolaou para identificar correctamente a las mujeres sin cáncer de cuello uterino. Varios estudios han revelado que la especificidad de la prueba de Papanicolaou está entre 64,79 y 96,8%. [28] [29] [30] Si bien las pruebas de Papanicolaou pueden no ser del todo precisas, siguen siendo una de las herramientas de prevención del cáncer de cuello uterino más efectivas. Las pruebas de Papanicolaou se pueden complementar con pruebas de ADN del VPH. [ cita necesaria ]
Al realizar pruebas de detección en una población general o de bajo riesgo, la mayoría de los resultados de Papanicolaou son normales.
En los Estados Unidos, cada año se encuentran entre 2 y 3 millones de resultados anormales en la prueba de Papanicolaou. [31] La mayoría de los resultados anormales son levemente anormales ( ASC-US (normalmente 2 a 5 % de los resultados de Papanicolaou) o lesión intraepitelial escamosa de bajo grado ( LSIL ) (aproximadamente 2 % de los resultados)), lo que indica infección por VPH. [ cita necesaria ] Aunque la mayoría de las displasias cervicales de bajo grado regresan espontáneamente sin provocar cáncer de cuello uterino , la displasia puede servir como una indicación de que se necesita una mayor vigilancia.
En un escenario típico, alrededor del 0,5 % de los resultados de la prueba de Papanicolaou son SIL de alto grado ( HSIL ) y menos del 0,5 % de los resultados indican cáncer; Del 0,2 al 0,8 % de los resultados indican células glandulares atípicas de significado indeterminado (AGC-NOS). [ cita necesaria ]
A medida que las preparaciones de base líquida (LBP) se convierten en un medio común para las pruebas, las tasas de resultados atípicos han aumentado. La tasa mediana para todas las preparaciones con lesiones intraepiteliales escamosas de bajo grado que utilizaron LBP fue del 2,9% en 2006, en comparación con una tasa mediana del 2,1% en 2003. Las tasas de lesiones intraepiteliales escamosas de alto grado (mediana, 0,5%) y células escamosas atípicas han cambiado poco. [32]
Los resultados anormales se informan según el sistema Bethesda . [33] Incluyen: [31]
También se pueden detectar anomalías endocervicales y endometriales, al igual que una serie de procesos infecciosos, incluidos los hongos , el virus del herpes simple y la tricomoniasis . Sin embargo, no es muy sensible para detectar estas infecciones, por lo que la ausencia de detección en una prueba de Papanicolaou no significa ausencia de infección. [ cita necesaria ]
Las pruebas de Papanicolaou generalmente se pueden realizar durante el embarazo hasta al menos las 24 semanas de edad gestacional . [34] Las pruebas de Papanicolaou durante el embarazo no se han asociado con un mayor riesgo de aborto espontáneo . [34] Se observa comúnmente un componente inflamatorio en las pruebas de Papanicolaou de mujeres embarazadas [35] y no parece representar un riesgo de parto prematuro posterior . [36]
Después del parto, se recomienda esperar 12 semanas antes de realizar la prueba de Papanicolaou porque la inflamación del cuello uterino provocada por el parto interfiere con la interpretación de la prueba. [37]
Los hombres transgénero también suelen tener riesgo de contraer el VPH debido a la retención del cuello uterino en la mayoría de las personas de este subgrupo. [38] [39] Como tal, las pautas profesionales recomiendan que los hombres transgénero sean examinados de forma rutinaria para detectar cáncer de cuello uterino utilizando métodos como la prueba de Papanicolaou, idénticos a las recomendaciones para las mujeres cisgénero. [40]
Sin embargo, los hombres transgénero tienen tasas más bajas de detección de cáncer de cuello uterino que las mujeres cisgénero. [41] Muchos hombres transgénero reportan barreras para recibir atención médica que afirme su género, [42] [43] incluida la falta de cobertura de seguro y el estigma/discriminación [44] [45] durante los encuentros clínicos, y pueden encontrar ideas erróneas del proveedor sobre el riesgo en esta población. para el cáncer de cuello uterino. Las pruebas de Papanicolaou pueden presentarse a los pacientes como procedimientos de detección de cáncer sin género en lugar de uno específico para el examen de los órganos reproductores femeninos. Las pruebas de Papanicolaou pueden desencadenar disforia de género en los pacientes y se puede utilizar un lenguaje neutral en cuanto al género al explicar la patogénesis del cáncer debido a una infección, enfatizando la omnipresencia de la infección por VPH independientemente del género. [46]
Las mujeres transgénero que no se han sometido a vaginoplastias no corren riesgo de desarrollar cáncer de cuello uterino porque no tienen cuello uterino. Las mujeres transgénero que se han sometido a vaginoplastias y tienen un neocérvix o una neovagina tienen una pequeña probabilidad de desarrollar cáncer, según la Sociedad Canadiense del Cáncer. [47] Los cirujanos suelen utilizar la piel del pene para crear la nueva vagina y el cuello uterino, lo que puede contraer el VPH y provocar cáncer de pene , aunque es considerablemente más raro que el cáncer de cuello uterino. [48] Debido a que el riesgo de este tipo de cáncer es tan bajo, las pruebas de detección del cáncer de cuello uterino no se ofrecen de forma rutinaria a quienes tienen un neocérvix. [49] [39] [50] [48]

Según los CDC, las mujeres deben evitar las relaciones sexuales, las duchas vaginales y el uso de medicamentos vaginales o espuma espermicida durante 2 días antes de la prueba. [51] Varios estudios han demostrado que el uso de una pequeña cantidad de gel lubricante a base de agua no interfiere, oscurece ni distorsiona la prueba de Papanicolaou. Además, la citología no se ve afectada, ni tampoco algunas pruebas de ETS. [52] Si una mujer ha tenido relaciones sexuales antes de la prueba, se le recomienda acudir a la cita según lo previsto, pero avisar al médico. [51] Los CDC aconsejan que ella también debería ir si está menstruando ; [51] sin embargo, otras organizaciones de salud recomiendan evitar hacerse un frotis cervical durante la menstruación, o los 2 días antes y después de su período. [53] Las pruebas de Papanicolaou se pueden realizar durante el período menstrual de una mujer, especialmente si el médico utiliza una prueba de base líquida; sin embargo, si el sangrado es extremadamente abundante, las células endometriales pueden oscurecer las células del cuello uterino y, si esto ocurre, es posible que sea necesario repetir la prueba al cabo de 6 meses. [54]
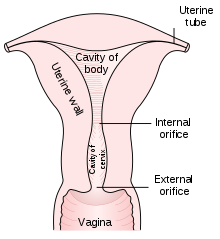
El trabajador de la salud comienza insertando un espéculo en la vagina de la mujer, que abre la vagina y permite el acceso al cuello uterino . Luego, el proveedor de atención médica recolecta una muestra de células de la abertura exterior o del orificio externo del cuello uterino raspándola con una espátula o un cepillo. [55]
Obtener una prueba de Papanicolaou no debería causar mucho dolor, [56] pero puede resultar incómodo. [57] El uso del espéculo puede ser doloroso si la mujer tiene vaginismo . Ciertos problemas no tratados, como la estenosis cervical, también pueden hacer que sea más doloroso.
En una prueba de Papanicolaou convencional, las células se colocan en un portaobjetos de vidrio y se llevan al laboratorio para detectar anomalías. [58]
A veces se utiliza una escoba con hoja de plástico en lugar de la espátula o el cepillo. La escoba no es un dispositivo de recolección tan bueno, ya que es mucho menos eficaz para recolectar material endocervical que la espátula y el cepillo. [59] La escoba se usa con más frecuencia con la llegada de la citología de base líquida , aunque se puede usar cualquier tipo de dispositivo de recolección con cualquier tipo de citología.
La muestra se tiñe mediante la técnica de Papanicolaou , en la que las células retienen selectivamente colorantes y ácidos tintóreos . Las células no teñidas no se pueden ver adecuadamente con un microscopio óptico. Papanicolaou eligió tinciones que resaltaban la queratinización citoplasmática, que en realidad no tiene casi nada que ver con las características nucleares que se utilizan hoy en día para hacer diagnósticos.
Un único frotis tiene un área de 25 x 50 mm y contiene en promedio unos cientos de miles de células. La detección con microscopía óptica se realiza primero con una potencia baja (10x) y luego se cambia a una potencia más alta (40x) al observar hallazgos sospechosos. Las células se analizan a alta potencia en busca de cambios morfológicos indicativos de malignidad (incluido un núcleo agrandado y de forma irregular, un aumento en la relación núcleo-citoplasma y una cromatina más gruesa e irregular). Se requieren aproximadamente 1.000 campos de visión con una potencia 10x para el análisis de una sola muestra, lo que lleva una media de 5 a 10 minutos. [60]
En algunos casos, un sistema informático puede preseleccionar las diapositivas, indicando aquellas que no necesitan ser examinadas por una persona o resaltando áreas que requieren atención especial. Luego, un citotecnólogo especialmente capacitado y calificado examina la muestra utilizando un microscopio óptico . La terminología para determinar quién analiza la muestra varía según el país; En el Reino Unido , el personal se conoce como citoscreeners , científicos biomédicos (BMS), médicos avanzados y patólogos . Los dos últimos asumen la responsabilidad de informar la muestra anormal, lo que puede requerir una investigación más profunda.
En la última década, ha habido intentos exitosos de desarrollar sistemas automatizados de análisis de imágenes por computadora para la detección. [61] Aunque, según la evidencia disponible, no se puede recomendar la implementación del cribado cervical automatizado en un programa nacional de cribado, una evaluación tecnológica reciente del NHS Health concluyó que "probablemente se había presentado un argumento general a favor del análisis automatizado de imágenes". [62] La automatización puede mejorar la sensibilidad y reducir las muestras insatisfactorias. [63] La FDA ha aprobado dos sistemas que funcionan en laboratorios de referencia de gran volumen, con supervisión humana. [ cita necesaria ]


Las pruebas de Papanicolaou suelen examinar anomalías epiteliales, como metaplasia, displasia o cambios límite, todos los cuales pueden ser indicativos de NIC. Los núcleos se teñirán de azul oscuro, las células escamosas se teñirán de verde y las células queratinizadas se teñirán de rosa/naranja. Se pueden observar coilocitos donde hay cierta discariosis (del epitelio). El núcleo de los coilocitos suele ser irregular, lo que indica un posible motivo de preocupación; requiriendo más exámenes y pruebas de confirmación.
Además, la prueba del virus del papiloma humano (VPH) se puede realizar como se indica en caso de resultados anormales de Papanicolaou o, en algunos casos, se realiza una prueba dual, en la que se realizan una prueba de Papanicolaou y una prueba de VPH al mismo tiempo (también llamada prueba de Papanicolaou). -pruebas). [sesenta y cinco]
Se puede tomar una muestra parcial del endocérvix con el dispositivo utilizado para obtener la muestra ectocervical, pero debido a la anatomía de esta área, no se puede garantizar un muestreo consistente y confiable. Dado que se pueden tomar muestras de células endocervicales anormales, a quienes las examinan se les enseña a reconocerlas. [ cita necesaria ]
El endometrio no se toma una muestra directamente con el dispositivo utilizado para tomar muestras del exocérvix. Las células pueden exfoliarse en el cuello uterino y recolectarse desde allí, de modo que, al igual que con las células endocervicales, se pueden reconocer células anormales si están presentes, pero la prueba de Papanicolaou no debe usarse como herramienta de detección de malignidad endometrial. [ cita necesaria ]
En los Estados Unidos, una prueba de Papanicolaou cuesta entre $20 y $30, pero los costos de las visitas para la prueba de Papanicolaou pueden costar más de $1,000, en gran parte porque se agregan pruebas adicionales que pueden ser necesarias o no. [66]
La prueba fue inventada por el médico griego Georgios Papanikolaou , quien comenzó su investigación en 1923 y recibió su nombre . [67] Aurel Babeș hizo descubrimientos similares de forma independiente en 1927. [68] Sin embargo, el método de Babeș era radicalmente diferente del de Papanikolaou. [67] [69]
La prueba de Papanicolaou fue finalmente reconocida sólo después de un artículo destacado en el American Journal of Obstetrics and Gynecology en 1941 por Papanikolaou y Herbert F. Traut, un ginecólogo estadounidense. [67] [70] Una monografía titulada Diagnóstico de cáncer uterino mediante frotis vaginal que publicaron contenía dibujos de las diversas células observadas en pacientes sin enfermedad, afecciones inflamatorias y carcinoma clínico y preclínico. [67] La monografía fue ilustrada por Hashime Murayama , quien más tarde se convirtió en ilustrador del personal de la National Geographic Society . [67] Tanto Papanikolaou como su esposa, Andromachi Papanikolaou , dedicaron el resto de sus vidas a enseñar la técnica a otros médicos y personal de laboratorio. [67]
En el mundo desarrollado, la biopsia cervical guiada por colposcopia se considera el " estándar de oro " para diagnosticar anomalías cervicales después de una prueba de Papanicolaou anormal. Otras técnicas como la prueba triple también se realizan después de una prueba de Papanicolaou anormal. [71] El procedimiento requiere un colposcopista capacitado y puede ser costoso de realizar. Sin embargo, las pruebas de Papanicolaou son muy sensibles y algunos resultados negativos de la biopsia pueden representar una muestra insuficiente de la lesión en la biopsia, por lo que una biopsia negativa con citología positiva requiere un seguimiento cuidadoso. [72]
Las técnicas de visualización experimental utilizan luz de banda ancha (p. ej., visualización directa, especulascopía , cervicografía , inspección visual con ácido acético o con Lugol y colposcopia) y métodos de detección electrónicos (p. ej., Polarprobe y espectroscopia in vivo ). Estas técnicas son menos costosas y se pueden realizar con mucha menos capacitación. No funcionan tan bien como la prueba de Papanicolaou y la colposcopia. En este momento, estas técnicas no han sido validadas por ensayos a gran escala y no son de uso general. [ cita necesaria ]
Australia ha utilizado la prueba de Papanicolaou como parte de su programa de detección cervical desde su implementación en 1991, que exigía que las mujeres mayores de 18 años se hicieran la prueba cada dos años. [73] En diciembre de 2017, Australia suspendió el uso de la prueba de Papanicolaou y la reemplazó con una nueva prueba de VPH que solo debe realizarse una vez cada cinco años a partir de los 25 años. [74] Medicare cubre los costos de la prueba; sin embargo, si el médico de un paciente no permite la facturación masiva, es posible que tenga que pagar la cita y luego reclamar el reembolso de Medicare. [75]
Las pruebas de Papanicolaou gratuitas se ofrecieron entre 1974 y 1984 antes de ser reemplazadas por un sistema en el que todas las mujeres mayores de 30 años podían obtener el reembolso del costo de su prueba de Papanicolaou por parte del Seguro Nacional de Salud en 1995. [76] Esta política todavía estaba en vigor en 2018 y alentó a las mujeres a realizarse pruebas de detección al menos cada tres años. [77]
A pesar de esto, el número de personas que se someten a la prueba de Papanicolaou sigue siendo inferior al de países como Australia. Algunos creen que esto se debe a una falta de conocimiento sobre la prueba y su disponibilidad. También se ha descubierto que las mujeres que padecen enfermedades crónicas u otras enfermedades reproductivas tienen menos probabilidades de hacerse la prueba. [78] [79] [80]
A partir de 2020, [actualizar]el NHS mantiene un programa de detección cervical en el que se invita a mujeres de entre 25 y 49 años a una prueba de frotis cada tres años, y a las mujeres mayores de 50 años cada cinco años. Al igual que Australia, Inglaterra utiliza una prueba de VPH antes de examinar las células que dan positivo en la prueba de Papanicolaou. [81] La prueba es gratuita como parte del programa nacional de detección cervical. [82]
El hallazgo de bacterias cocoides en una prueba de Papanicolaou no tiene importancia, ya que los resultados de la prueba son normales y no hay síntomas infecciosos. Sin embargo, si hay suficiente inflamación como para oscurecer la detección de procesos precancerosos y cancerosos, puede indicar tratamiento con un antibiótico de amplio espectro para estreptococos y bacterias anaerobias (como metronidazol y amoxicilina ) antes de repetir el frotis. Alternativamente, la prueba se repetirá antes de lo habitual. [83] Si hay síntomas de flujo vaginal , mal olor o irritación, la presencia de bacterias cocoides también puede indicar tratamiento con antibióticos como se indicó anteriormente. [83]
ACS y otros han recomendado, desde antes de 1980, que la citología convencional se puede realizar de forma segura hasta cada tres años para la mayoría de las mujeres.