Los iones de sodio ( Na + ) son necesarios en pequeñas cantidades para algunos tipos de plantas , [1] pero el sodio como nutriente generalmente es necesario en cantidades mayores [1] para los animales , debido a que lo utilizan para generar impulsos nerviosos y para el mantenimiento del equilibrio electrolítico y de líquidos . En los animales, los iones de sodio son necesarios para las funciones antes mencionadas y para la actividad cardíaca y determinadas funciones metabólicas . [2] Los efectos de la sal sobre la salud reflejan lo que sucede cuando el cuerpo tiene demasiado o muy poco sodio. Las concentraciones características de sodio en organismos modelo son: 10 mM en E. coli , 30 mM en levadura en ciernes, 10 mM en células de mamíferos y 100 mM en plasma sanguíneo. [3]
Además, los iones de sodio son esenciales para varios procesos celulares. Son responsables del cotransporte de glucosa en el simporte sodio-glucosa, se utilizan para ayudar a mantener la polaridad de la membrana con la ayuda de la bomba de sodio y potasio y se combinan con agua para diluir la mucosidad de la luz de las vías respiratorias cuando la fibrosis quística está activa. El receptor de transporte mueve iones de cloruro hacia las vías respiratorias. [4]
El requerimiento fisiológico mínimo de sodio está entre 115 y 500 mg por día dependiendo de la sudoración debida a la actividad física y de si la persona está adaptada al clima. [5] El cloruro de sodio es la principal fuente de sodio en la dieta y se utiliza como condimento y conservante, como para encurtir y cecina ; la mayor parte proviene de alimentos procesados. [6] La ingesta adecuada de sodio es de 1,2 a 1,5 g por día, [7] pero en promedio las personas en los Estados Unidos consumen 3,4 g por día, [8] [9] la cantidad mínima que promueve la hipertensión. [10] Tenga en cuenta que la sal contiene aproximadamente un 39,3 % de sodio en masa [11] ; el resto es cloro y otras trazas químicas; por lo tanto, el nivel máximo de ingesta tolerable de 2,3 g de sodio sería aproximadamente 5,9 g de sal, aproximadamente 1 cucharadita . [12] La excreción diaria promedio de sodio está entre 40 y 220 mEq. [13]
Los niveles normales de sodio en suero están entre aproximadamente 135 y 145 mEq /L (135 a 145 mmol/L). Un nivel de sodio sérico inferior a 135 mEq/L se considera hiponatremia , que se considera grave cuando el nivel de sodio sérico es inferior a 125 mEq/L. [14] [15]
El sistema renina-angiotensina y el péptido natriurético auricular regulan indirectamente la cantidad de transducción de señales en el sistema nervioso central humano , que depende del movimiento de los iones de sodio a través de la membrana de las células nerviosas, en todos los nervios. Por tanto, el sodio es importante en la función neuronal y en la osmorregulación entre las células y el líquido extracelular ; La distribución de iones de sodio está mediada en todos los animales por bombas de sodio-potasio , que son bombas transportadoras activas de solutos , que bombean iones contra el gradiente, y canales de sodio-potasio. [16] Se sabe que los canales de sodio son menos selectivos en comparación con los canales de potasio. El sodio es el catión más destacado en el líquido extracelular: en los 15 litros de líquido extracelular de un ser humano de 70 kg hay alrededor de 50 gramos de sodio, el 90% del contenido total de sodio del cuerpo.
Algunas neurotoxinas potentes , como la batracotoxina , aumentan la permeabilidad de los iones sodio de las membranas celulares de los nervios y músculos, provocando una despolarización masiva e irreversible de las membranas con consecuencias potencialmente fatales. Sin embargo, los fármacos con efectos menores sobre el movimiento de los iones de sodio en los nervios pueden tener diversos efectos farmacológicos que van desde acciones antidepresivas hasta anticonvulsivas.
Dado que sólo algunas plantas necesitan sodio y aquellas en pequeñas cantidades, una dieta completamente basada en plantas será generalmente muy baja en sodio. [ cita necesaria ] Esto requiere que algunos herbívoros obtengan su sodio de lamidos de sal y otras fuentes minerales. La necesidad animal de sodio es probablemente la razón de la capacidad altamente conservada de saborear el ion sodio como "salado". Los receptores del sabor puro salado responden mejor al sodio; de lo contrario, los receptores responden sólo a unos pocos otros pequeños cationes monovalentes ( Li + , NH+4y algo a K + ). El ion calcio (Ca 2+ ) también tiene un sabor salado y a veces amargo para algunas personas pero, al igual que el potasio, puede desencadenar otros sabores.
Los iones de sodio desempeñan un papel diverso e importante en muchos procesos fisiológicos, actuando para regular el volumen sanguíneo , la presión arterial , el equilibrio osmótico y el pH . [8]
En las plantas C4 , el sodio es un micronutriente que ayuda en el metabolismo, concretamente en la regeneración del fosfoenolpiruvato (implicado en la biosíntesis de diversos compuestos aromáticos y en la fijación de carbono ) y en la síntesis de clorofila. [17] En otros, sustituye al potasio en varias funciones, como mantener la presión de turgencia y ayudar en la apertura y cierre de los estomas. [18] El exceso de sodio en el suelo limita la absorción de agua debido a la disminución del potencial hídrico , lo que puede provocar el marchitamiento; concentraciones similares en el citoplasma pueden provocar inhibición enzimática, lo que a su vez provoca necrosis y clorosis. [19] Para evitar estos problemas, las plantas desarrollaron mecanismos que limitan la absorción de sodio por las raíces, lo almacenan en vacuolas celulares y los controlan a largas distancias; [20] el exceso de sodio también puede almacenarse en el tejido vegetal viejo, lo que limita el daño al nuevo crecimiento. Aunque aún no se ha determinado cuánto exceso de carga de sodio en el xilema. Sin embargo, el anti-porter CHX21 se puede atribuir a la carga activa de sodio en el xilema. [21]
El sodio es el catión primario (ion cargado positivamente) en los fluidos extracelulares de animales y humanos. Estos fluidos, como el plasma sanguíneo y los fluidos extracelulares de otros tejidos, bañan las células y llevan a cabo funciones de transporte de nutrientes y desechos. El sodio también es el catión principal en el agua de mar, aunque la concentración allí es aproximadamente 3,8 veces mayor que la normal en los fluidos corporales extracelulares.
Aunque el sistema para mantener el equilibrio óptimo de sal y agua en el cuerpo es complejo, [22] una de las principales formas en que el cuerpo humano realiza un seguimiento de la pérdida de agua corporal es que los osmorreceptores en el hipotálamo detectan un equilibrio de sodio y agua. Concentración de agua en los líquidos extracelulares. La pérdida relativa de agua corporal hará que la concentración de sodio aumente más de lo normal, una condición conocida como hipernatremia . Esto normalmente resulta en sed. Por el contrario, un exceso de agua corporal causado por beber resultará en muy poco sodio en la sangre ( hiponatremia ), una condición que nuevamente es detectada por el hipotálamo , causando una disminución en la secreción de la hormona vasopresina de la hipófisis posterior y la consiguiente pérdida de agua en la orina, que actúa para restablecer las concentraciones normales de sodio en la sangre.
Las personas gravemente deshidratadas, como las personas rescatadas de situaciones de supervivencia en el océano o en el desierto, suelen tener concentraciones de sodio en sangre muy altas. Estos deben volverse a la normalidad con mucho cuidado y lentamente, ya que una corrección demasiado rápida de la hipernatremia puede provocar daño cerebral debido a la inflamación celular, ya que el agua se mueve repentinamente hacia las células con un alto contenido osmolar .
En humanos, se demostró que una ingesta elevada de sal atenúa la producción de óxido nítrico . El óxido nítrico (NO) contribuye a la homeostasis de los vasos al inhibir la contracción y el crecimiento del músculo liso vascular, la agregación plaquetaria y la adhesión de los leucocitos al endotelio. [23]
Debido a que el sistema hipotálamo / osmorreceptor normalmente funciona bien para hacer que beber u orinar restablezca las concentraciones de sodio del cuerpo a la normalidad, este sistema se puede usar en tratamientos médicos para regular el contenido total de líquidos del cuerpo, controlando primero el contenido de sodio del cuerpo. Así, cuando se administra un fármaco diurético potente que hace que los riñones excreten sodio, el efecto va acompañado de una excreción de agua corporal (la pérdida de agua acompaña a la pérdida de sodio). Esto sucede porque el riñón no puede retener agua de manera eficiente mientras excreta grandes cantidades de sodio. Además, después de la excreción de sodio, el sistema osmorreceptor puede detectar una concentración reducida de sodio en la sangre y luego dirigir la pérdida compensatoria de agua en la orina para corregir el estado hiponatrémico (bajo nivel de sodio en la sangre).

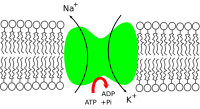
La bomba de sodio-potasio trabaja con los canales de fuga de sodio y potasio para mantener el potencial de membrana entre la célula y el espacio extracelular. El sodio desciende por el gradiente de concentración desde el citosol hacia la matriz extracelular. El potasio desciende por su gradiente de concentración desde la matriz extracelular hacia el citosol. Para mantener el potencial de membrana, la bomba de sodio-potasio actúa como una forma de transporte activo directo donde la hidrólisis de ATP a ADP y un fosfato inorgánico en la ATPasa tipo P mueve 3 iones de potasio hacia afuera de la célula y 2 iones de sodio. iones al interior de la célula. [4]
La bomba de sodio-potasio desempeña un papel importante en la señalización neuronal debido al mantenimiento del potencial de la membrana celular. Esto crea un potencial de acción que hace que las neuronas polaricen y despolaricen sus membranas abriendo y cerrando los canales regulados por voltaje: esto altera el potencial de voltaje y conduce a la secreción de neurotransmisores y, en última instancia, a la transmisión de señales. [24]
Cuando la bomba deja de funcionar, los pacientes son susceptibles a enfermedades como insuficiencia cardíaca y enfermedad pulmonar obstructiva crónica (FRÍO). Aquellos que experimentaron un evento de insuficiencia cardíaca tenían, en promedio, una concentración un 40% menor de ATPasa de sodio y potasio. Esta falta de polarización de la membrana conduce a una incapacidad de los potenciales de acción para propagarse a su ritmo habitual, lo que provoca una frecuencia auditiva reducida y potencialmente insuficiencia cardíaca. [25] En los diagnósticos de resfriado, la mayoría de los pacientes que tenían una cantidad reducida de magnesio y potasio también tenían una concentración reducida de la bomba de sodio-potasio en el músculo esquelético y liso durante la insuficiencia respiratoria. El RESFRIADO se puede tratar a corto plazo con glucocorticoides, que regulan positivamente la bomba de sodio-potasio, lo que ayuda a reforzar la resistencia muscular y aumenta la actividad muscular durante estos episodios de insuficiencia respiratoria. [26]

En el transportador simultáneo de sodio y glucosa , el sodio disminuye su gradiente de concentración para hacer subir la glucosa a su gradiente de concentración. El sodio tiene una mayor concentración fuera de la célula y se une al simportador, que se encuentra en su conformación orientada hacia afuera. Una vez que se une el sodio, la glucosa puede unirse desde el espacio extracelular, lo que hace que el transportador simultáneo cambie a la formación ocluida (cerrada) antes de abrirse hacia el interior de la célula y liberar los dos iones de sodio y la molécula de glucosa. Una vez que ambos se liberan, el symporter se reorienta hacia la conformación que mira hacia afuera y el proceso comienza de nuevo. [4] Un ejemplo importante de regulación positiva del transportador simultáneo de sodio y glucosa se observa en pacientes con diabetes tipo 2 , donde hay aproximadamente una regulación positiva de 3 a 4 veces del transportador simultáneo de sodio y glucosa (SGLT1). Esto conduce a una entrada de glucosa en la célula y produce hiperglucemia. [27]

El Regulador del Transporte de la Fibrosis Quística (CFTR) funciona uniendo dos ATP al dominio de unión de ATP A1 y A2. Esto abre el canal CFTR y permite que los iones de cloruro fluyan hacia los pulmones y la luz de las vías respiratorias. Esta entrada de iones de cloruro con carga negativa hacia la luz de las vías respiratorias hace que el sodio se mueva hacia la luz de las vías respiratorias para equilibrar la carga negativa. Luego, el agua ingresa con el sodio para equilibrar la presión osmótica y, en última instancia, conduce a la dilución del moco. En los casos de fibrosis quística, el CFTR es defectuoso y solo se une a un único ATP, lo que hace que el canal no se abra y evita que los iones de cloruro se difundan hacia la luz de las vías respiratorias. Dado que los iones de cloruro no pueden difundirse, no hay movimiento de sodio hacia la luz de las vías respiratorias y no es necesario que el agua entre en la luz, lo que genera un moco espeso que obstruye e infecta la luz de las vías respiratorias. [4]
Por lo tanto, se puede estimar un requerimiento mínimo promedio para adultos en condiciones de máxima adaptación y sin sudoración activa en no más de 5 mEq/día, lo que corresponde a 115 mg de sodio o aproximadamente 300 mg de cloruro de sodio por día. Teniendo en cuenta la amplia variación de patrones de actividad física y exposición climática, una ingesta mínima segura podría fijarse en 500 mg/día. [Nota: la tabla 11-1 parece aclarar que 500 mg se refiere a sodio, no a cloruro de sodio]