El einstenio es un elemento químico sintético ; tiene símbolo Es y número atómico 99. Es miembro de la serie de actínidos y es el séptimo elemento transuránico . Fue nombrado en honor a Albert Einstein .
El einstenio se descubrió como componente de los restos de la explosión de la primera bomba de hidrógeno en 1952. Su isótopo más común , el einstenio-253 (vida media de 20,47 días), se produce artificialmente a partir de la desintegración del californio -253 en unas pocas instalaciones dedicadas de alta potencia. reactores nucleares con un rendimiento total del orden de un miligramo por año. A la síntesis del reactor le sigue un complejo proceso de separación del einstenio-253 de otros actínidos y productos de su desintegración. Otros isótopos se sintetizan en varios laboratorios, pero en cantidades mucho menores, bombardeando elementos actínidos pesados con iones ligeros. Debido a las pequeñas cantidades de einstenio producido y la corta vida media de su isótopo más común, no tiene aplicaciones prácticas excepto la investigación científica básica. En particular, el einstenio se utilizó para sintetizar, por primera vez, 17 átomos del nuevo elemento mendelevio en 1955.
El einstenio es un metal blando, plateado y paramagnético . Su química es típica de los actínidos tardíos, con preponderancia del estado de oxidación +3 ; el estado de oxidación +2 también es accesible, especialmente en sólidos. La alta radiactividad del einstenio-253 produce un brillo visible y daña rápidamente su red metálica cristalina, con un calor liberado de aproximadamente 1000 vatios por gramo. La dificultad para estudiar sus propiedades se debe a la desintegración del einstenio-253 en berkelio -249 y luego en californio-249 a un ritmo de aproximadamente el 3% por día. El isótopo del einstenio con la vida media más larga, el einstenio-252 (vida media de 471,7 días), sería más adecuado para la investigación de las propiedades físicas, pero ha demostrado ser mucho más difícil de producir y sólo está disponible en cantidades mínimas, no en a granel. [2] El einstenio es el elemento con el número atómico más alto que se ha observado en cantidades macroscópicas en su forma pura como einstenio-253. [3]
Como todos los elementos transuránicos sintéticos, los isótopos del einstenio son muy radiactivos y se consideran muy peligrosos para la salud si se ingieren. [4]

El einstenio fue identificado por primera vez en diciembre de 1952 por Albert Ghiorso y sus compañeros de trabajo de la Universidad de California, Berkeley, en colaboración con los Laboratorios Nacionales de Argonne y Los Alamos , como resultado de la prueba nuclear de Ivy Mike . La prueba se llevó a cabo el 1 de noviembre de 1952 en el atolón de Enewetak en el Océano Pacífico y fue la primera prueba exitosa de un arma termonuclear . [5] El examen inicial de los restos de la explosión había demostrado la producción de un nuevo isótopo de plutonio .244
94PU
, que sólo pudo haberse formado mediante la absorción de seis neutrones por un núcleo de uranio-238 seguida de dos desintegraciones beta .
En aquel momento, se pensaba que la absorción múltiple de neutrones era un proceso extremadamente raro, pero la identificación de244
94PU
indicó que los núcleos de uranio podrían haber capturado aún más neutrones, produciendo así nuevos elementos más pesados que el californio . [5]

Ghiorso y sus colaboradores analizaron papeles de filtro que habían sido lanzados a través de la nube de explosión en aviones (la misma técnica de muestreo que se había utilizado para descubrir244
94PU
). [6] Posteriormente se aislaron mayores cantidades de material radiactivo de los restos de coral del atolón, que fueron entregados a los EE.UU. [5] La separación de nuevos elementos sospechosos se llevó a cabo en presencia de una solución tampón de ácido cítrico / amonio en una solución débilmente medio ácido ( pH ≈ 3,5), utilizando intercambio iónico a temperaturas elevadas; Al final se recuperaron menos de 200 átomos de einstenio. [7] Sin embargo, el elemento 99 (einstenio), es decir, su isótopo 253 Es, pudo detectarse mediante su característica desintegración alfa de alta energía a 6,6 MeV. [5] Fue producido por la captura de 15 neutrones por núcleos de uranio-238 seguido de siete desintegraciones beta, y tuvo una vida media de 20,5 días. Esta absorción múltiple de neutrones fue posible gracias a la alta densidad del flujo de neutrones durante la detonación, de modo que los isótopos pesados recién generados tenían muchos neutrones disponibles para absorber antes de que pudieran desintegrarse en elementos más ligeros. La captura de neutrones inicialmente elevó el número másico sin cambiar el número atómico del nucleido, y las desintegraciones beta concomitantes dieron como resultado un aumento gradual en el número atómico: [5]
Unos 238 átomos de U, sin embargo, podrían absorber dos neutrones adicionales (para un total de 17), dando como resultado 255 Es, así como el isótopo 255 Fm de otro nuevo elemento, el fermio . [8] El descubrimiento de los nuevos elementos y los nuevos datos asociados sobre la captura de múltiples neutrones se mantuvieron inicialmente en secreto por orden del ejército estadounidense hasta 1955 debido a las tensiones de la Guerra Fría y la competencia con la Unión Soviética en tecnologías nucleares. [5] [9] [10] Sin embargo, la rápida captura de tantos neutrones proporcionaría la necesaria confirmación experimental directa del llamado proceso r de absorción múltiple de neutrones, necesaria para explicar la nucleosíntesis (producción) cósmica de ciertos elementos químicos pesados ( más pesado que el níquel) en explosiones de supernovas , antes de la desintegración beta . Este proceso es necesario para explicar la existencia de muchos elementos estables en el universo. [11]
Mientras tanto, en los laboratorios de Berkeley y Argonne se produjeron isótopos del elemento 99 (así como del nuevo elemento 100, el fermio ), en una reacción nuclear entre el nitrógeno -14 y el uranio-238, [12] y posteriormente mediante una intensa irradiación de neutrones del plutonio. o californio :
Estos resultados fueron publicados en varios artículos en 1954 con la advertencia de que no eran los primeros estudios que se realizaban sobre los elementos. [13] [14] [15] [16] [17] El equipo de Berkeley también informó algunos resultados sobre las propiedades químicas del einstenio y el fermio. [18] [19] Los resultados de Ivy Mike fueron desclasificados y publicados en 1955. [9]

En el descubrimiento de los elementos 99 y 100, los equipos americanos habían competido con un grupo del Instituto Nobel de Física de Estocolmo , Suecia . A finales de 1953 y principios de 1954, el grupo sueco logró sintetizar los isótopos ligeros del elemento 100, en particular el 250 Fm, bombardeando núcleos de uranio con oxígeno. Estos resultados también se publicaron en 1954. [20] Sin embargo, la prioridad del equipo de Berkeley fue generalmente reconocida, ya que sus publicaciones precedieron al artículo sueco y se basaron en los resultados no divulgados anteriormente de la explosión termonuclear de 1952; así, el equipo de Berkeley tuvo el privilegio de nombrar los nuevos elementos. Como el esfuerzo que había llevado al diseño de Ivy Mike tenía el nombre en código Proyecto PANDA, [21] el elemento 99 había sido apodado en broma "Pandemonium" [22] pero los nombres oficiales sugeridos por el grupo de Berkeley derivaban de dos científicos prominentes, Albert Einstein y Enrico Fermi : "Sugerimos para el nombre del elemento con número atómico 99, einstenio (símbolo E) en honor a Albert Einstein y para el nombre del elemento con número atómico 100, fermio (símbolo Fm), en honor a Enrico Fermi." [9] Tanto Einstein como Fermi murieron entre el momento en que se propusieron originalmente los nombres y el momento en que se anunciaron. El descubrimiento de estos nuevos elementos fue anunciado por Albert Ghiorso en la primera Conferencia Atómica de Ginebra celebrada del 8 al 20 de agosto de 1955. [5] El símbolo del einstenio fue dado primero como "E" y luego cambiado a "Es" por la IUPAC. [23] [24]

El einstenio es un metal sintético, plateado y radiactivo. En la tabla periódica , se ubica a la derecha del actínido californio , a la izquierda del actínido fermio y debajo del lantánido holmio con el que comparte muchas similitudes en propiedades físicas y químicas. Su densidad de 8,84 g/cm 3 es menor que la del californio (15,1 g/cm 3 ) y casi la misma que la del holmio (8,79 g/cm 3 ), a pesar de que el einstenio atómico es mucho más pesado que el holmio. El punto de fusión del einstenio (860 °C) también es relativamente bajo: inferior al californio (900 °C), al fermio (1527 °C) y al holmio (1461 °C). [4] [26] El einstenio es un metal blando, con un módulo volumétrico de sólo 15 GPa, cuyo valor es uno de los más bajos entre los metales no alcalinos . [27]
A diferencia de los actínidos más ligeros californio , berkelio , curio y americio , que cristalizan en una estructura hexagonal doble en condiciones ambientales, se cree que el einstenio tiene una simetría cúbica centrada en las caras ( fcc ) con el grupo espacial Fm 3 m y la constante de red a. = 575 pm. Sin embargo, hay un informe de metal de einstenio hexagonal a temperatura ambiente con a = 398 pm y c = 650 pm, que se convirtió a la fase fcc al calentarse a 300 °C. [28]
El autodaño inducido por la radioactividad del einstenio es tan fuerte que destruye rápidamente la red cristalina [29] y la energía liberada durante este proceso, 1000 vatios por gramo de 253 Es, induce un brillo visible. [3] Estos procesos pueden contribuir a la densidad y el punto de fusión relativamente bajos del einstenio. [30] Además, debido al pequeño tamaño de las muestras disponibles, el punto de fusión del einstenio a menudo se deducía observando el calentamiento de la muestra dentro de un microscopio electrónico. [31] Por lo tanto, los efectos superficiales en muestras pequeñas podrían reducir el valor del punto de fusión.
El metal es trivalente y tiene una volatilidad notablemente alta. [32] Para reducir el daño por autoradiación, la mayoría de las mediciones de einstenio sólido y sus compuestos se realizan inmediatamente después del recocido térmico. [33] Además, algunos compuestos se estudian bajo la atmósfera del gas reductor, por ejemplo H 2 O+ HCl para EsOCl, de modo que la muestra vuelve a crecer parcialmente durante su descomposición. [34]
Aparte de la autodestrucción del einstenio sólido y sus compuestos, otras dificultades intrínsecas al estudiar este elemento incluyen la escasez (el isótopo 253 Es más común está disponible sólo una o dos veces al año en cantidades inferiores a miligramos) y la autocontaminación debido a la rápida conversión de einstenio en berkelio y luego en californio a una tasa de aproximadamente 3,3% por día: [35] [36] [37]
Por lo tanto, la mayoría de las muestras de einstenio están contaminadas y sus propiedades intrínsecas a menudo se deducen extrapolando datos experimentales acumulados a lo largo del tiempo. Otras técnicas experimentales para solucionar el problema de la contaminación incluyen la excitación óptica selectiva de iones de einstenio mediante un láser sintonizable, como el estudio de sus propiedades de luminiscencia. [38]
Se han estudiado las propiedades magnéticas del metal einstenio, su óxido y fluoruro. Los tres materiales mostraron un comportamiento paramagnético de Curie-Weiss desde helio líquido hasta temperatura ambiente. Los momentos magnéticos efectivos se dedujeron como10,4 ± 0,3 μ B para Es 2 O 3 y11,4 ± 0,3 μ B para el EsF 3 , que son los valores más altos entre los actínidos, y las temperaturas de Curie correspondientes son 53 y 37 K. [39] [40]
Como todos los actínidos, el einstenio es bastante reactivo. Su estado de oxidación trivalente es más estable en sólidos y soluciones acuosas, donde induce un color rosa pálido. [41] La existencia de einstenio divalente está firmemente establecida, especialmente en la fase sólida; Tal estado +2 no se observa en muchos otros actínidos, incluidos el protactinio , el uranio , el neptunio , el plutonio , el curio y el berkelio . Los compuestos de einstenio (II) se pueden obtener, por ejemplo, reduciendo el einstenio (III) con cloruro de samario (II) . [42]
Se conocen dieciocho isótopos y cinco isómeros nucleares del einstenio, con números de masa que oscilan entre 240 y 257. [1] Todos son radiactivos y el nucleido más estable, el 252 Es, tiene una vida media de 471,7 días. [43] Los siguientes isótopos más estables son 254 Es (vida media de 275,7 días), [44] 255 Es (39,8 días) y 253 Es (20,47 días). Todos los isótopos restantes tienen vidas medias inferiores a 40 horas, la mayoría inferiores a 30 minutos. De los cinco isómeros nucleares, el más estable es el 254m Es con una vida media de 39,3 horas. [1]
El einstenio tiene una alta tasa de fisión nuclear que resulta en una masa crítica baja para una reacción nuclear en cadena sostenida . Esta masa es de 9,89 kilogramos para una esfera desnuda del isótopo 254 Es, y puede reducirse a 2,9 kilogramos añadiendo un reflector de neutrones de acero de 30 centímetros de espesor , o incluso a 2,26 kilogramos con un reflector de agua de 20 cm de espesor. Sin embargo, incluso esta pequeña masa crítica supera con creces la cantidad total de einstenio aislado hasta ahora, especialmente del raro isótopo 254 Es. [45]
Debido a la corta vida media de todos los isótopos del einstenio, cualquier einstenio primordial (es decir, el einstenio que podría haber estado presente en la Tierra en el momento de su formación) hace tiempo que se descompuso. La síntesis de einstenio a partir de actínidos naturales de uranio y torio en la corteza terrestre requiere una captura múltiple de neutrones, lo cual es un evento extremadamente improbable. Por lo tanto, todo el einstenio terrestre se produce en laboratorios científicos, reactores nucleares de alta potencia o en pruebas de armas nucleares , y existe sólo unos pocos años después del momento de la síntesis. [7]
Los elementos transuránicos, desde el americio hasta el fermio , incluido el einstenio, se crearon en el reactor de fisión nuclear natural de Oklo , pero las cantidades producidas entonces se habrían desintegrado hace mucho tiempo. [46]
Teóricamente, el einstenio se observó en el espectro de la estrella de Przybylski . [47] Sin embargo, la autora principal de los estudios que encontraron einstenio y otros actínidos de vida corta en la estrella de Przybylski, Vera F. Gopka, admitió que "la posición de las líneas de los elementos radiactivos buscados se visualizaba simplemente en el espectro sintético como marcadores verticales porque no existen datos atómicos para estas líneas excepto sus longitudes de onda (Sansonetti et al. 2004), lo que permite calcular sus perfiles con intensidades más o menos reales." [48] Desde entonces, los espectros característicos de los isótopos de einstenio se han analizado exhaustivamente de forma experimental (en 2021), [49] aunque no hay ninguna investigación publicada que confirme si las firmas teorizadas de einsteinio propuestas para encontrar en el espectro de la estrella coinciden con los resultados determinados en el laboratorio.

El einstenio se produce en cantidades mínimas bombardeando actínidos más ligeros con neutrones en reactores nucleares dedicados de alto flujo . Las principales fuentes de irradiación del mundo son el reactor de isótopos de alto flujo (HFIR) de 85 megavatios del Laboratorio Nacional Oak Ridge en Tennessee, EE. UU., [51] y el reactor de bucle SM-2 del Instituto de Investigación de Reactores Atómicos (NIIAR) en Dimitrovgrad. , Rusia , [52] ambas dedicadas a la producción de elementos transcurio ( Z > 96). Estas instalaciones tienen niveles de potencia y flujo similares, y se espera que tengan capacidades de producción comparables para elementos de transcurio, [53] aunque las cantidades producidas en NIIAR no se informan ampliamente. En una "campaña de procesamiento típica" en Oak Ridge, se irradian decenas de gramos de curio para producir cantidades de decigramos de californio , miligramos de berkelio ( 249 Bk) y einstenio y picogramos de fermio . [54] [55]
La primera muestra microscópica de 253 Es que pesaba unos 10 nanogramos se preparó en 1961 en HFIR. Se diseñó una balanza magnética especial para estimar su peso. [4] [56] Posteriormente se produjeron lotes más grandes a partir de varios kilogramos de plutonio con rendimientos de einstenio (principalmente 253 Es) de 0,48 miligramos en 1967-1970, 3,2 miligramos en 1971-1973, seguidos por una producción constante de alrededor de 3 miligramos por año entre 1974 y 1978. [57] Sin embargo, estas cantidades se refieren a la cantidad integral en el objetivo inmediatamente después de la irradiación. Los procedimientos de separación posteriores redujeron aproximadamente diez veces la cantidad de einstenio isotópicamente puro. [53]
La intensa irradiación de neutrones del plutonio produce cuatro isótopos principales de einstenio: 253 Es (emisor α con vida media de 20,47 días y con una vida media de fisión espontánea de 7×10 5 años); 254m Es (emisor β con vida media de 39,3 horas), 254 Es (emisor α con vida media de aproximadamente 276 días) y 255 Es (emisor β con vida media de 39,8 días). [58] [59] Una ruta alternativa implica el bombardeo de uranio-238 con haces de iones de nitrógeno u oxígeno de alta intensidad. [60]
El einstenio-247 (vida media de 4,55 minutos) se produjo irradiando americio-241 con carbono o uranio-238 con iones nitrógeno. [61] Esta última reacción se realizó por primera vez en 1967 en Dubna, Rusia, y los científicos involucrados recibieron el Premio Lenin Komsomol . [62]
El isótopo 248 Es se produjo irradiando 249 Cf con iones de deuterio . Se desintegra principalmente por emisión de electrones a 248 Cf con una vida media de25 ± 5 minutos, pero también libera partículas α de 6,87 MeV de energía, con una proporción de electrones a partículas α de aproximadamente 400. [63]
Los isótopos más pesados 249 Es, 250 Es, 251 Es y 252 Es se obtuvieron bombardeando 249 Bk con partículas α. En este proceso se liberan de uno a cuatro neutrones, lo que hace posible la formación de cuatro isótopos diferentes en una reacción. [64]
El einstenio-253 se produjo irradiando un objetivo de 252 Cf de 0,1 a 0,2 miligramos con un flujo de neutrones térmicos de (2–5)×10 14 neutrones·cm −2 ·s −1 durante 500 a 900 horas: [65]
En 2020, los científicos del Laboratorio Nacional de Oak Ridge pudieron crear unos 200 nanogramos de 254 Es, un nuevo récord mundial. [ cita necesaria ] Esto permitió estudiar algunas propiedades químicas del elemento por primera vez. [66]

El análisis de los restos del ensayo nuclear de Ivy Mike, de 10 megatones, formaba parte de un proyecto a largo plazo. Uno de cuyos objetivos era estudiar la eficiencia de la producción de elementos transuránicos en explosiones nucleares de alta potencia. La motivación de estos experimentos fue que la síntesis de dichos elementos a partir de uranio requiere la captura múltiple de neutrones. La probabilidad de tales eventos aumenta con el flujo de neutrones , y las explosiones nucleares son las fuentes de neutrones más poderosas creadas por el hombre, proporcionando densidades del orden de 10 23 neutrones/cm 2 en un microsegundo, o alrededor de 10 29 neutrones/(cm 2 ·s). ). En comparación, el flujo del reactor HFIR es 5 × 1015 neutrones/(cm 2 ·s). Se instaló un laboratorio exclusivo en el atolón de Enewetak para el análisis preliminar de los desechos, ya que algunos isótopos podrían haberse desintegrado cuando las muestras de desechos llegaron a los EE. UU. continentales. El laboratorio estaba recibiendo muestras para su análisis lo antes posible, desde aviones equipados con filtros de papel. que sobrevoló el atolón después de las pruebas. Aunque se esperaba descubrir nuevos elementos químicos más pesados que el fermio, ninguno de ellos se encontró incluso después de una serie de explosiones de megatones realizadas entre 1954 y 1956 en el atolón. [6]
Los resultados atmosféricos se complementaron con los datos de pruebas subterráneas acumulados en la década de 1960 en el sitio de pruebas de Nevada , ya que se esperaba que explosiones poderosas realizadas en espacios confinados pudieran dar como resultado rendimientos mejorados e isótopos más pesados. Además de las cargas de uranio tradicionales, se han probado combinaciones de uranio con americio y torio , así como una carga mixta de plutonio y neptunio, pero tuvieron menos éxito en términos de rendimiento y se atribuyeron a mayores pérdidas de isótopos pesados debido al aumento de las tasas de fisión. en cargas de elementos pesados. El aislamiento del producto fue problemático ya que las explosiones esparcieron escombros al derretir y vaporizar las rocas circundantes a profundidades de 300 a 600 metros. La perforación a tales profundidades para extraer los productos fue lenta e ineficiente en términos de volúmenes recolectados. [6] [67]
Entre las nueve pruebas subterráneas que se realizaron entre 1962 y 1969, [68] [69] la última fue la más poderosa y tuvo el mayor rendimiento de elementos transuránicos. En un microsegundo se produjeron miligramos de einstenio que normalmente requerirían un año de irradiación en un reactor de alta potencia. [67] Sin embargo, el principal problema práctico de toda la propuesta fue recolectar los desechos radiactivos dispersados por la poderosa explosión. Los filtros de avión adsorbieron solo alrededor de 4 × 10-14 de la cantidad total, y la recolección de toneladas de corales en el atolón Enewetak aumentó esta fracción en sólo dos órdenes de magnitud. La extracción de unos 500 kilogramos de rocas subterráneas 60 días después de la explosión de Hutch recuperó sólo alrededor de 1 × 10−7 de la carga total. La cantidad de elementos transuránicos en este lote de 500 kg era sólo 30 veces mayor que en una roca de 0,4 kg recogida 7 días después de la prueba, lo que demostró la dependencia altamente no lineal del rendimiento de elementos transuránicos de la cantidad de roca radiactiva recuperada. [70] Se perforaron pozos en el sitio antes de la prueba para acelerar la recolección de muestras después de la explosión, de modo que la explosión expulsara el material radiactivo del epicentro a través de los pozos y hacia los volúmenes de recolección cerca de la superficie. Este método se probó en dos pruebas y obtuvo instantáneamente cientos de kilogramos de material, pero con una concentración de actínidos 3 veces menor que en las muestras obtenidas después de la perforación. Si bien ese método podría haber sido eficaz en estudios científicos de isótopos de vida corta, no pudo mejorar la eficiencia general de recolección de los actínidos producidos. [71]
Aunque no se pudieron detectar nuevos elementos (aparte del einstenio y el fermio) en los restos de las pruebas nucleares, y los rendimientos totales de elementos transuránicos fueron decepcionantemente bajos, estas pruebas proporcionaron cantidades significativamente mayores de isótopos pesados raros que los disponibles anteriormente en los laboratorios. [72]
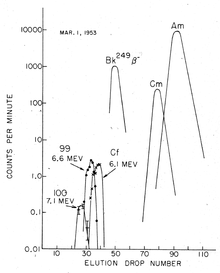
El procedimiento de separación del einstenio depende del método de síntesis. En el caso del bombardeo con iones ligeros dentro de un ciclotrón, el objetivo del ion pesado se fija a una lámina delgada y el einstenio generado simplemente se elimina de la lámina después de la irradiación. Sin embargo, las cantidades producidas en tales experimentos son relativamente bajas. [73] Los rendimientos son mucho mayores para la irradiación del reactor, pero allí, el producto es una mezcla de varios isótopos actínidos, así como lantánidos producidos en las desintegraciones de la fisión nuclear. En este caso, el aislamiento de einstenio es un procedimiento tedioso que implica varios pasos repetidos de intercambio catiónico, a temperatura y presión elevadas, y cromatografía. La separación del berkelio es importante, porque el isótopo de einstenio más común producido en los reactores nucleares, el 253 Es, se desintegra con una vida media de sólo 20 días a 249 Bk, lo cual es rápido en la escala de tiempo de la mayoría de los experimentos. Dicha separación se basa en el hecho de que el berkelio se oxida fácilmente al estado sólido +4 y precipita, mientras que otros actínidos, incluido el einstenio, permanecen en su estado +3 en soluciones. [74]
La separación de actínidos trivalentes de los productos de fisión de lantánidos se puede realizar mediante una columna de resina de intercambio catiónico utilizando una solución de 90% de agua/10% de etanol saturada con ácido clorhídrico (HCl) como eluyente . Generalmente va seguido de una cromatografía de intercambio aniónico utilizando HCl 6 molar como eluyente. Luego se usa una columna de resina de intercambio catiónico (columna de intercambio Dowex-50) tratada con sales de amonio para separar las fracciones que contienen los elementos 99, 100 y 101. Luego, estos elementos se pueden identificar simplemente basándose en su posición/tiempo de elución, usando α-hidroxiisobutirato. solución (α-HIB), por ejemplo, como eluyente. [75]
La separación de los 3+ actínidos también se puede lograr mediante cromatografía de extracción con disolvente, utilizando ácido bis-(2-etilhexil)fosfórico (abreviado como HDEHP) como fase orgánica estacionaria y ácido nítrico como fase acuosa móvil. La secuencia de elución de actínidos es inversa a la de la columna de resina de intercambio catiónico. El einstenio separado mediante este método tiene la ventaja de estar libre de agentes complejantes orgánicos, en comparación con la separación mediante una columna de resina. [75]
El einstenio es altamente reactivo y, por lo tanto, se requieren fuertes agentes reductores para obtener el metal puro a partir de sus compuestos. [76] Esto se puede lograr mediante la reducción del fluoruro de einstenio (III) con litio metálico :
Sin embargo, debido a su bajo punto de fusión y su alta tasa de daño por autorradiación, el einstenio tiene una alta presión de vapor, que es mayor que la del fluoruro de litio. Esto hace que esta reacción de reducción sea bastante ineficiente. Se probó en los primeros intentos de preparación y rápidamente se abandonó en favor de la reducción del óxido de einstenio (III) con lantano metálico: [28] [30] [77]
El óxido de einstenio (III) (Es 2 O 3 ) se obtuvo quemando nitrato de einstenio (III). Forma cristales cúbicos incoloros, que se caracterizaron por primera vez a partir de muestras de microgramos de unos 30 nanómetros. [29] [36] Se conocen otras dos fases, monoclínica y hexagonal, para este óxido. La formación de una determinada fase de Es 2 O 3 depende de la técnica de preparación y del historial de la muestra, y no existe un diagrama de fases claro. Las interconversiones entre las tres fases pueden ocurrir espontáneamente, como resultado de la autoirradiación o el autocalentamiento. [86] La fase hexagonal es isotípica con óxido de lantano donde el ion Es 3+ está rodeado por un grupo de 6 coordinados de iones O 2− . [78] [83]

Los haluros de einstenio son conocidos por los estados de oxidación +2 y +3. [85] [87] El estado más estable es +3 para todos los haluros, desde fluoruro hasta yoduro.
El fluoruro de einstenio (III) (EsF 3 ) se puede precipitar a partir de soluciones de cloruro de einstenio (III) al reaccionar con iones fluoruro . Un procedimiento de preparación alternativo es exponer el óxido de einstenio (III) a trifluoruro de cloro (ClF 3 ) o gas F 2 a una presión de 1 a 2 atmósferas y una temperatura entre 300 y 400 °C. La estructura cristalina de EsF 3 es hexagonal, como en el fluoruro de californio (III) (CfF 3 ), donde los iones Es 3+ están ocho veces coordinados por iones de flúor en una disposición de prisma trigonal bicamerado . [35] [88] [89]
El cloruro de einstenio (III) (EsCl 3 ) se puede preparar recociendo óxido de einstenio (III) en una atmósfera de vapores secos de cloruro de hidrógeno a aproximadamente 500 °C durante unos 20 minutos. Cristaliza al enfriarse a aproximadamente 425 °C en un sólido naranja con una estructura hexagonal de tipo UCl 3 , donde los átomos de einstenio están coordinados nueve veces por los átomos de cloro en una geometría de prisma trigonal tricapeado. [81] [88] [90] El bromuro de einstenio (III) (EsBr 3 ) es un sólido de color amarillo pálido con una estructura monoclínica de tipo AlCl 3 , donde los átomos de einstenio están coordinados octaédricamente por el bromo (número de coordinación 6). [84] [88]
Los compuestos divalentes de einstenio se obtienen reduciendo los haluros trivalentes con hidrógeno : [91]
Se han producido cloruro de einstenio (II) (EsCl 2 ), [92] bromuro de einstenio (II) (EsBr 2 ), [93] y yoduro de einstenio (II) (EsI 2 ) [85] y se han caracterizado por absorción óptica, sin información estructural disponible todavía. [84]
Los oxihaluros de einstenio conocidos incluyen EsOCl, [85] EsOBr [91] y EsOI. [85] Estas sales se sintetizan tratando un trihaluro con una mezcla de vapor de agua y el correspondiente haluro de hidrógeno: por ejemplo, EsCl 3 + H 2 O/HCl para obtener EsOCl. [34]
La alta radiactividad del einstenio tiene un uso potencial en radioterapia , y se han sintetizado complejos organometálicos para administrar átomos de einstenio a un órgano apropiado del cuerpo. Se han realizado experimentos inyectando citrato de einstenio (así como compuestos de fermio) a perros. [3] El einstenio (III) también se incorporó a complejos de quelato de beta-dicetona, ya que complejos análogos con lantánidos previamente mostraban la luminiscencia excitada por UV más fuerte entre los compuestos metalorgánicos. Al preparar complejos de einstenio, los iones Es 3+ se diluyeron 1000 veces con iones Gd 3+ . Esto permitió reducir el daño por radiación para que los compuestos no se desintegraran durante el período de 20 minutos requerido para las mediciones. La luminiscencia resultante del Es 3+ era demasiado débil para ser detectada. Esto se explicó por las energías relativas desfavorables de los constituyentes individuales del compuesto que obstaculizaron la transferencia eficiente de energía desde la matriz del quelato a los iones Es 3+ . Se llegó a una conclusión similar respecto de otros actínidos: americio, berkelio y fermio. [94]
Sin embargo, se observó luminiscencia de iones Es 3+ tanto en soluciones inorgánicas de ácido clorhídrico como en soluciones orgánicas con ácido di(2-etilhexil)ortofosfórico. Muestra un pico amplio de aproximadamente 1064 nanómetros (la mitad del ancho es de aproximadamente 100 nm) que puede excitarse resonantemente con luz verde (aproximadamente 495 nm de longitud de onda). La luminiscencia tiene una vida útil de varios microsegundos y el rendimiento cuántico es inferior al 0,1%. Las tasas de desintegración no radiativa relativamente altas, en comparación con los lantánidos, en Es 3+ se asociaron con la interacción más fuerte de los electrones f con los electrones internos de Es 3+ . [95]
Casi no hay uso para ningún isótopo de einstenio fuera de la investigación científica básica dirigida a la producción de elementos transuránicos superiores y elementos superpesados . [96]
En 1955, se sintetizó mendelevio irradiando un objetivo que constaba de aproximadamente 10 9 átomos de 253 Es en el ciclotrón de 60 pulgadas del Laboratorio Berkeley. La reacción resultante de 253 Es(α,n) 256 Md produjo 17 átomos del nuevo elemento con el número atómico de 101. [97]
El raro isótopo 254 Es es el preferido para la producción de elementos superpesados debido a su gran masa, su vida media relativamente larga de 270 días y su disponibilidad en cantidades significativas de varios microgramos. [98] Por lo tanto, 254 Es se utilizó como objetivo en el intento de síntesis de ununennium (elemento 119) en 1985 bombardeándolo con iones calcio-48 en el acelerador lineal de partículas superHILAC en Berkeley, California. No se identificaron átomos, lo que establece un límite superior para la sección transversal de esta reacción en 300 nanobarns . [99]
254 Es se utilizó como marcador de calibración en el espectrómetro de análisis químico (" analizador de superficie de dispersión alfa ") de la sonda lunar Surveyor 5 . La gran masa de este isótopo redujo la superposición espectral entre las señales del marcador y los elementos más ligeros estudiados de la superficie lunar. [100]
La mayoría de los datos disponibles sobre la toxicidad del einstenio provienen de investigaciones en animales. Tras la ingestión por ratas , sólo ~0,01% termina en el torrente sanguíneo. De ahí, alrededor del 65% va a los huesos, donde permanecería durante ~50 años si no fuera por su desintegración radiactiva, por no hablar de la vida útil máxima de 3 años de las ratas, el 25% a los pulmones (vida media biológica ~ 20 años, aunque esto vuelve a ser irrelevante debido a la corta vida media del einstenio), 0,035% a los testículos o 0,01% a los ovarios, donde el einstenio permanece indefinidamente. Aproximadamente el 10% de la cantidad ingerida se excreta. La distribución del einstenio sobre las superficies óseas es uniforme y similar a la del plutonio. [101]
{{citation}}: CS1 maint: multiple names: authors list (link)Laboratorio de Radiación, Universidad de California, Berkeley, UCRL-2591{{cite book}}: CS1 maint: location missing publisher (link)