Los canales de potencial receptor transitorio ( canales TRP ) son un grupo de canales iónicos ubicados principalmente en la membrana plasmática de numerosos tipos de células animales. La mayoría de estos se agrupan en dos grandes grupos: el grupo 1 incluye TRPC ("C" para canónico), TRPV ("V" para vanilloide), TRPVL ("VL" para tipo vanilloide), TRPM ("M" para melastatina) , TRPS ("S" para soromelastatina), TRPN ("N" para potencial de mecanorreceptor C) y TRPA ("A" para anquirina). El grupo 2 consta de TRPP ("P" para poliquístico) y TRPML ("ML" para mucolipina). [1] [2] Existen otros canales TRP menos categorizados, incluidos los canales de levadura y varios canales del Grupo 1 y del Grupo 2 presentes en animales no animales. [2] [3] [4] Muchos de estos canales median una variedad de sensaciones como dolor, temperatura, diferentes tipos de gusto, presión y visión. En el cuerpo, se cree que algunos canales TRP se comportan como termómetros microscópicos y se utilizan en animales para detectar calor o frío. [5] Algunos canales TRP son activados por moléculas que se encuentran en especias como el ajo ( alicina ), el ají ( capsaicina ), el wasabi ( isotiocianato de alilo ); otros se activan con mentol , alcanfor , menta y agentes refrescantes; y otros se activan mediante moléculas que se encuentran en el cannabis (es decir, THC , CBD y CBN ) o la stevia . Algunos actúan como sensores de presión osmótica, volumen, estiramiento y vibración. La mayoría de los canales se activan o inhiben mediante lípidos de señalización y contribuyen a una familia de canales iónicos activados por lípidos . [6] [7]
Estos canales iónicos tienen una permeabilidad relativamente no selectiva a los cationes , incluidos el sodio , el calcio y el magnesio .
Los canales TRP se descubrieron inicialmente en la cepa mutante denominada "potencial receptor transitorio" (mutante trp ) de la mosca de la fruta Drosophila , de ahí su nombre (consulte Historia de los canales TRP de Drosophila a continuación). Posteriormente, se encontraron canales TRP en vertebrados, donde se expresan de forma ubicua en muchos tipos de células y tejidos. La mayoría de los canales TRP están compuestos por 6 hélices que atraviesan la membrana con extremos N y C intracelulares . Los canales TRP de los mamíferos se activan y regulan mediante una amplia variedad de estímulos y se expresan en todo el cuerpo.
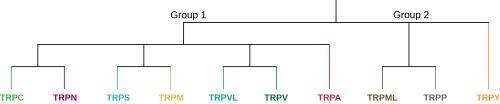
En la superfamilia animal TRP hay actualmente 9 familias propuestas divididas en dos grupos, cada familia contiene varias subfamilias. [2] El grupo uno consta de TRPC, TRPV, TRPVL, TRPA, TRPM, TRPS y TRPN, mientras que el grupo dos contiene TRPP y TRPML. Hay una familia adicional denominada TRPY que no siempre se incluye en ninguno de estos grupos. Todas estas subfamilias son similares en el sentido de que son canales catiónicos no selectivos de detección molecular que tienen seis segmentos transmembrana; sin embargo, cada subfamilia es muy única y comparte poca homología estructural entre sí. Esta singularidad da lugar a las diversas funciones de percepción y regulación sensorial que tienen los canales TRP en todo el cuerpo. El grupo uno y el grupo dos varían en que tanto TRPP como TRPML del grupo dos tienen un bucle extracelular mucho más largo entre los segmentos transmembrana S1 y S2. Otra característica diferenciadora es que todas las subfamilias del grupo uno contienen una secuencia repetida de anquirina intracelular N-terminal, una secuencia de dominio TRP C-terminal o ambas, mientras que ambas subfamilias del grupo dos no tienen ninguna. [8] A continuación se muestran los miembros de las subfamilias y una breve descripción de cada una:
TRPA, A de "ankyrin", recibe su nombre por la gran cantidad de repeticiones de ankyrin que se encuentran cerca del extremo N. [12] TRPA se encuentra principalmente en las fibras nerviosas nociceptivas aferentes y se asocia con la amplificación de la señalización del dolor, así como con la hipersensibilidad al dolor por frío. Se ha demostrado que estos canales son receptores mecánicos del dolor y quimiosensores activados por diversas especies químicas, incluidos los isotiocianatos (sustancias químicas picantes en sustancias como el aceite de mostaza y el wasabi), cannabinoides, analgésicos generales y locales y cinamaldehído. [13]
Si bien TRPA1 se expresa en una amplia variedad de animales, existe una variedad de otros canales TRPA fuera de los vertebrados. TRPA5, indoloro, pirexia y waterwitch son ramas filogenéticas distintas dentro del clado TRPA, y solo se evidencia que se expresan en crustáceos e insectos, [8] mientras que HsTRPA surgió como una duplicación de waterwitch específica de himenópteros. [14] Al igual que TRPA1 y otros canales TRP, estos funcionan como canales iónicos en varios sistemas sensoriales. Los canales TRPA o similares a TRPA1 también existen en una variedad de especies como un clado filogenéticamente distinto, pero no se comprenden tan bien. [10]
TRPC, C de "canónico", recibe su nombre por ser el más estrechamente relacionado con Drosophila TRP, el homónimo de los canales TRP. La filogenia de los canales TRPC no se ha resuelto en detalle, pero están presentes en todos los taxones animales. En realidad, solo hay seis canales TRPC expresados en humanos porque TRPC2 se expresa únicamente en ratones y se considera un pseudogen en humanos; Esto se debe en parte al papel de TRPC2 en la detección de feromonas, cuya capacidad los ratones tienen mayor en comparación con los humanos. Las mutaciones en los canales TRPC se han asociado con enfermedades respiratorias junto con glomeruloesclerosis focal y segmentaria en los riñones. [13] Todos los canales TRPC se activan mediante fosfolipasa C (PLC) o diacilglicerol (DAG).
TRPML, ML para "mucolipina", recibe su nombre del trastorno del desarrollo neurológico mucolipidosis IV . La mucolipidosis IV fue descubierta por primera vez en 1974 por ER Berman, quien notó anomalías en los ojos de un bebé. [18] Estas anomalías pronto se asociaron con mutaciones en el gen MCOLN1 que codifica el canal iónico TRPML1. TRPML aún no está muy caracterizado. Las tres copias de vertebrados conocidas se limitan a vertebrados con mandíbulas, con algunas excepciones (por ejemplo, Xenopus tropicalis ). [17]
TRPM, M de "melastatina", se encontró durante un análisis genético comparativo entre nevos benignos y nevos malignos (melanoma). [12] Las mutaciones dentro de los canales TRPM se han asociado con hipomagnesemia con hipocalcemia secundaria. Los canales TRPM también se han hecho conocidos por sus mecanismos de detección de frío, como es el caso de TRPM8. [13] Estudios comparativos han demostrado que los dominios funcionales y los aminoácidos críticos de los canales TRPM están altamente conservados entre especies. [19] [10] [20]
La filogenética ha demostrado que los canales TRPM se dividen en dos clados principales, αTRPM y βTRPM. [10] [16] Los αTRPM incluyen TRPM1, TRPM3 de vertebrados y las "chanzimas" TRPM6 y TRPM7, así como el único canal TRPM de insectos, entre otros. Los βTRPM incluyen, entre otros, TRPM2, TRPM4, TRPM5 y TRPM8 de vertebrados (el sensor de frío y mentol). Se han descrito dos clados principales adicionales: TRPMc, que está presente sólo en una variedad de artrópodos, [16] y un clado basal, [11] [10] que desde entonces se ha propuesto como una familia de canales TRP distinta y separada (TRPS ). [dieciséis]
TRPN was originally described in Drosophila melanogaster and Caenorhabditis elegans as nompC, a mechanically gated ion channel.[22][21] Only a single TRPN, N for "no mechanoreceptor potential C," or "nompC", is known to be broadly expressed in animals (although some Cnidarians have more), and is notably only a pseudogene in amniote vertebrates.[21][11] Despite TRPA being named for ankyrin repeats, TRPN channels are thought to have the most of any TRP channel, typically around 28, which are highly conserved across taxa [21] Since its discovery, Drosophila nompC has been implicated in mechanosensation (including mechanical stimulation of the cuticle and sound detection) and cold nociception.[23]
TRPP, P for "polycistin", is named for polycystic kidney disease, which is associated with these channels.[12] These channels are also referred to as PKD (polycistic kidney disease) ion channels.
PKD2-like genes (examples include TRPP2, TRPP3, and TRPP5) encode canonical TRP channels. PKD1-like genes encode much larger proteins with 11 transmembrane segments, which do not have all the features of other TRP channels. However, 6 of the transmebrane segments of PKD1-like proteins have substantial sequence homology with TRP channels, indicating they may simply have diversified greatly from other closely related proteins.[26]
Insects have a third sub-family of TRPP, called brividos, which participate in cold sensing.[25][2]
TRPS, S for Soromelastatin, was named as it forms a sister group to TRPM. TRPS is broadly present in animals, but notably absent in vertebrates and insects (among others).[16] TRPS has not yet been well described functionally, though it is known that the C. elegans TRPS, known as CED-11, is a calcium channel which participates in apoptosis.[27]
TRPV, V de "vanilloide", se descubrió originalmente en Caenorhabditis elegans y lleva el nombre de las sustancias químicas vanilloides que activan algunos de estos canales. [24] [29] Estos canales se han hecho famosos por su asociación con moléculas como la capsaicina (un agonista de TRPV1). [13] Además de los 6 parálogos de vertebrados conocidos, se conocen 2 clados principales fuera de los deterostomas: nanchung e Iav. Los estudios mecanicistas de estos últimos clados se han restringido en gran medida a Drosophila , pero los análisis filogenéticos han colocado dentro de ellos otros genes de Placozoa, Annelida, Cnidaria, Mollusca y otros artrópodos. [11] [30] [31] Los canales TRPV también se han descrito en protistas. [11]
Se ha propuesto que TRPVL sea un clado hermano de TRPV y se limite a los cnidarios Nematostella vectensis e Hydra magnipapillata , y al anélido Capitella teleta . [11] Poco se sabe sobre estos canales.
TRPY, Y de "levadura", está altamente localizado en la vacuola de levadura, que es el equivalente funcional de un lisosoma en una célula de mamífero, y actúa como un mecanosensor de la presión osmótica vacuolar. Las técnicas de pinzamiento del parche y la estimulación hiperosmótica han ilustrado que TRPY desempeña un papel en la liberación de calcio intracelular. [32] El análisis filogenético ha demostrado que TRPY1 no forma parte de los otros grupos uno y dos de TRP de metazoos, y se sugiere que evolucionó después de la divergencia de metazoos y hongos. [8] Otros han indicado que TRPY están más estrechamente relacionados con TRPP. [33]
Los canales TRP están compuestos por 6 hélices que atraviesan la membrana (S1-S6) con extremos N y C intracelulares . Los canales TRP de los mamíferos se activan y regulan mediante una amplia variedad de estímulos que incluyen muchos mecanismos postranscripcionales como la fosforilación , el acoplamiento del receptor de proteína G , la activación de ligandos y la ubiquitinación . Los receptores se encuentran en casi todos los tipos de células y están localizados en gran medida en las membranas celulares y de orgánulos, modulando la entrada de iones.
La mayoría de los canales TRP forman homotetrámeros o heterotetrámeros cuando son completamente funcionales. El filtro de selectividad iónica, el poro, está formado por la combinación compleja de bucles p en la proteína tetramérica, que se encuentran en el dominio extracelular entre los segmentos transmembrana S5 y S6. Como ocurre con la mayoría de los canales catiónicos, los canales TRP tienen residuos cargados negativamente dentro del poro para atraer los iones cargados positivamente. [34]
Cada canal de este grupo es estructuralmente único, lo que se suma a la diversidad de funciones que poseen los canales TRP; sin embargo, existen algunos puntos en común que distinguen a este grupo de otros. A partir del extremo N intracelular hay longitudes variables de repeticiones de ankryin (excepto en TRPM) que ayudan con el anclaje de la membrana y otras interacciones proteicas. Poco después de S6 en el extremo C-terminal, hay un dominio TRP altamente conservado (excepto en TRPA) que participa en la modulación de activación y la multimerización de canales. También se han observado en este grupo otras modificaciones C-terminales, como los dominios alfa-quinasa en TRPM7 y M8. [8] [13] [12]
El rasgo más distinguible del grupo dos es el largo tramo extracelular entre los segmentos transmembrana S1 y S2. Los miembros del grupo dos también carecen de repeticiones de ankryin y de un dominio TRP. Sin embargo, se ha demostrado que tienen secuencias de retención del retículo endoplásmico (RE) hacia el extremo C-terminal que ilustran posibles interacciones con el RE. [8] [13] [12]
Los canales TRP modulan las fuerzas impulsoras de entrada de iones y la maquinaria de transporte de Ca 2+ y Mg 2+ en la membrana plasmática, donde se encuentran la mayoría de ellos. Los TRP tienen interacciones importantes con otras proteínas y, a menudo, forman complejos de señalización, cuyas vías exactas se desconocen. [35] Los canales TRP se descubrieron inicialmente en la cepa mutante trp de la mosca de la fruta Drosophila [36] que mostraba una elevación transitoria del potencial en respuesta a estímulos luminosos y se denominaron canales de potencial receptor transitorio . [37] Los canales TRPML funcionan como canales de liberación de calcio intracelular y, por lo tanto, desempeñan un papel importante en la regulación de los orgánulos. [35] Es importante destacar que muchos de estos canales median una variedad de sensaciones como las sensaciones de dolor, temperatura, diferentes tipos de gusto, presión y visión. En el cuerpo, se cree que algunos canales TRP se comportan como termómetros microscópicos y se utilizan en animales para detectar calor o frío. Los TRP actúan como sensores de presión osmótica , volumen , estiramiento y vibración . Se ha observado que los PRT desempeñan funciones multidimensionales complejas en la señalización sensorial. Muchos TRP funcionan como canales de liberación de calcio intracelular.
Los canales iónicos TRP convierten la energía en potenciales de acción en los nociceptores somatosensoriales. [38] Los canales Thermo-TRP tienen un dominio C-terminal que es responsable de la termosensación y tienen una región intercambiable específica que les permite detectar estímulos de temperatura que están vinculados a procesos reguladores de ligandos. [39] Aunque la mayoría de los canales TRP están modulados por cambios de temperatura, algunos tienen un papel crucial en la sensación de temperatura. Hay al menos 6 canales Thermo-TRP diferentes y cada uno desempeña una función diferente. Por ejemplo, TRPM8 se relaciona con los mecanismos de detección del frío, TRPV1 y TRPM3 contribuyen a las sensaciones de calor e inflamación, y TRPA1 facilita muchas vías de señalización como la transducción sensorial, la nocicepción , la inflamación y el estrés oxidativo . [38]
TRPM5 participa en la señalización del sabor dulce , amargo y umami mediante la modulación de la vía de señal en las células receptoras del gusto tipo II . [40] TRPM5 es activado por los glucósidos dulces que se encuentran en la planta de stevia .
Varios otros canales TRP desempeñan un papel importante en la quimiosensación a través de terminaciones nerviosas sensoriales en la boca que son independientes de las papilas gustativas. TRPA1 responde al aceite de mostaza ( isotiocianato de alilo ), wasabi y canela, TRPA1 y TRPV1 responden al ajo ( alicina ), TRPV1 responde al chile ( capsaicina ), TRPM8 se activa con mentol , alcanfor , menta y agentes refrescantes; TRPV2 se activa mediante moléculas ( THC , CBD y CBN ) que se encuentran en la marihuana.

Las moscas de la fruta mutantes trp , que carecen de una copia funcional del gen trp, se caracterizan por una respuesta transitoria a la luz, a diferencia de las moscas de tipo salvaje que demuestran una actividad sostenida de las células fotorreceptoras en respuesta a la luz. [36] Posteriormente se identificó una isoforma lejanamente relacionada del canal TRP, el canal similar a TRP (TRPL), en los fotorreceptores de Drosophila , donde se expresa en niveles aproximadamente de 10 a 20 veces más bajos que la proteína TRP. Posteriormente se aisló una mosca mutante, tpl . Además de las diferencias estructurales, los canales TRP y TRPL difieren en la permeabilidad catiónica y las propiedades farmacológicas.
Los canales TRP/TRPL son los únicos responsables de la despolarización de la membrana plasmática de los fotorreceptores de insectos en respuesta a la luz. Cuando estos canales se abren, permiten que el sodio y el calcio ingresen a la célula a favor del gradiente de concentración, lo que despolariza la membrana. Las variaciones en la intensidad de la luz afectan el número total de canales TRP/TRPL abiertos y, por tanto, el grado de despolarización de la membrana. Estas respuestas de voltaje gradual se propagan a las sinapsis de los fotorreceptores con las neuronas retinianas de segundo orden y más allá del cerebro.
Es importante señalar que el mecanismo de fotorrecepción de los insectos es dramáticamente diferente al de los mamíferos. La excitación de la rodopsina en los fotorreceptores de los mamíferos conduce a la hiperpolarización de la membrana del receptor, pero no a la despolarización como en el ojo del insecto. En Drosophila y, se supone, en otros insectos, una cascada de señalización mediada por fosfolipasa C (PLC) vincula la fotoexcitación de la rodopsina con la apertura de los canales TRP/TRPL. Aunque desde hace años se conocen numerosos activadores de estos canales, como el fosfatidilinositol-4,5-bifosfato (PIP 2 ) y los ácidos grasos poliinsaturados (PUFA), un factor clave que media el acoplamiento químico entre los canales PLC y TRP/TRPL sigue siendo un misterio hasta hace poco. Se descubrió que la degradación de un producto lipídico de la cascada PLC, el diacilglicerol (DAG), por la enzima diacilglicerol lipasa , genera PUFA que pueden activar los canales TRP, iniciando así la despolarización de la membrana en respuesta a la luz. [41] Este mecanismo de activación del canal TRP puede estar bien conservado entre otros tipos de células donde estos canales realizan diversas funciones.
Las mutaciones en los TRP se han relacionado con trastornos neurodegenerativos , displasia esquelética , trastornos renales [35] y pueden desempeñar un papel importante en el cáncer. Los PRT pueden ser objetivos terapéuticos importantes. Existe una importancia clínica significativa para el papel de TRPV1, TRPV2, TRPV3 y TRPM8 como termorreceptores, y el papel de TRPV4 y TRPA1 como mecanorreceptores; La reducción del dolor crónico puede ser posible dirigiéndose a los canales iónicos implicados en la sensación térmica, química y mecánica para reducir su sensibilidad a los estímulos. [42] Por ejemplo, el uso de agonistas de TRPV1 podría inhibir potencialmente la nocicepción en TRPV1, particularmente en el tejido pancreático donde TRPV1 se expresa altamente. [43] El agonista de TRPV1 capsaicina, que se encuentra en los chiles, ha sido indicado para aliviar el dolor neuropático. [35] Los agonistas de TRPV1 inhiben la nocicepción en TRPV1
La expresión alterada de las proteínas TRP a menudo conduce a la tumorigénesis , como se informó para TRPV1, TRPV6, TRPC1, TRPC6, TRPM4, TRPM5 y TRPM8. [43] TRPV1 y TRPV2 han sido implicados en el cáncer de mama. La expresión de TRPV1 en agregados encontrados en el retículo endoplásmico o el aparato de Golgi y/o rodeando estas estructuras en pacientes con cáncer de mama confiere una peor supervivencia. [44]
La familia de canales iónicos TRPM está particularmente asociada con el cáncer de próstata, donde TRPM2 (y su largo ARN no codificante TRPM2-AS ), TRPM4 y TRPM8 se sobreexpresan en el cáncer de próstata y se asocian con resultados más agresivos. [45] Se ha demostrado que TRPM3 promueve el crecimiento y la autofagia en el carcinoma de células renales de células claras, [46] TRPM4 se sobreexpresa en el linfoma difuso de células B grandes asociado con una peor supervivencia, [47] mientras que TRPM5 tiene propiedades oncogénicas en el melanoma . [48]
Los canales TRP ocupan un lugar central en la modulación de la resistencia a la quimioterapia en el cáncer de mama. [49] Algunos canales TRP, como TRPA1 y TRPC5, están estrechamente asociados con la resistencia a los medicamentos durante el tratamiento del cáncer; El alto influjo de Ca 2+ mediado por TRPC5 activa el factor de transcripción NFATC3 (factor nuclear de células T activadas, citoplasmático 3), que desencadena la transcripción de la glicoproteína p (p-gp). La sobreexpresión de p-gp es ampliamente reconocida como un factor importante en la quimiorresistencia en las células cancerosas, ya que funciona como una bomba de eflujo activa que puede eliminar diversas sustancias extrañas, incluidos agentes quimioterapéuticos, del interior de la célula. [49]

Por el contrario, se ha demostrado que otros canales TRP, como TRPV1 y TRPV2, potencian los efectos antitumorales de ciertos agentes quimioterapéuticos y TRPV2 es un biomarcador potencial y una diana terapéutica en el cáncer de mama triple negativo. [49]
Además de las vías mediadas por TLR4 , ciertos miembros de la familia de canales iónicos potenciales del receptor transitorio reconocen el LPS . La activación de TRPA1 mediada por LPS se demostró en ratones [50] y en moscas Drosophila melanogaster . [51] En concentraciones más altas, el LPS también activa otros miembros de la familia de canales sensoriales TRP, como TRPV1, TRPM3 y, hasta cierto punto, TRPM8. [52] El TRPV4 reconoce el LPS en las células epiteliales. La activación de TRPV4 por LPS fue necesaria y suficiente para inducir la producción de óxido nítrico con efecto bactericida. [53]
El mutante TRP original en Drosophila fue descrito por primera vez por Cosens y Manning en 1969 como "una cepa mutante de D. melanogaster que, aunque se comporta fototácticamente positiva en un laberinto en forma de T bajo poca luz ambiental, tiene problemas de visión y se comporta como si fuera ciego". . También mostró una respuesta anormal del electrorretinograma de los fotorreceptores a la luz, que fue transitoria en lugar de sostenida como en el "tipo salvaje". [36] Fue investigado posteriormente por Baruch Minke, un postdoctorado en el grupo de William Pak, y lo denominó TRP según su comportamiento en el ERG. [54] La identidad de la proteína mutada se desconocía hasta que fue clonada por Craig Montell, un investigador postdoctoral en el grupo de investigación de Gerald Rubin, en 1989, quien observó su relación estructural predicha con los canales conocidos en ese momento [37] y Roger Hardie y Baruch Minke quienes proporcionaron evidencia en 1992 de que es un canal iónico que se abre en respuesta a la estimulación luminosa. [55] El canal TRPL fue clonado y caracterizado en 1992 por el grupo de investigación de Leonard Kelly. [56] En 2013, Montell y su grupo de investigación descubrieron que el canal catiónico TRPL (similar a TRP) era un objetivo directo para los saborizantes en las neuronas receptoras gustativas y podía regularse a la baja de manera reversible. [57]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )