
Los analgésicos opioides son agonistas de los receptores opioides que producen un efecto analgésico. El registro más antiguo de estos fármacos se remonta al año 3500 a. C., cuando los sumerios utilizaban opio para aliviar el dolor. Los opioides se pueden clasificar en diferentes clases según su estructura química o su efecto agonista. Producen el efecto analgésico activando varios tipos de receptores opioides en las neuronas presinápticas y postsinápticas para inhibir la transmisión de señales de dolor. [ cita requerida ]
En términos de farmacocinética, los opioides podrían tener interacciones farmacológicas significativas debido a su metabolismo a través de las enzimas CYP3A y CYP2D6 . Algunos fármacos podrían unirse a la enzima CYP y alterar el metabolismo de los opioides. En términos de farmacodinámica, los opioides podrían interactuar con los depresores del sistema nervioso central y producir un efecto sinérgico que induce una depresión excesiva y puede provocar la muerte. [ cita requerida ]
Los opioides se utilizan comúnmente para aliviar el dolor moderado a severo en pacientes posoperatorios o pacientes con cáncer. Pueden inducir efectos secundarios en el sistema nervioso central, como sedación, somnolencia y depresión. Los opioides también pueden provocar adicción, lo que hace que el abuso de opioides se convierta en un problema de salud importante en la sociedad. Para prevenir la sobredosis de opioides , se sugiere reducir la dosis y la duración de la prescripción para minimizar su efecto en el cuerpo. [ cita requerida ]
Tiempo antiguo
El uso más antiguo registrado de opioides para aliviar el dolor se remonta al 3400 al 3500 a. C., entre los sumerios de la Baja Mesopotamia . Los sumerios usaban opio, un compuesto intensamente adictivo derivado de la adormidera, para tratar el dolor, inducir el sueño y producir euforia. [1] Debido a su uso recreativo y médico, el opio estaba vinculado al dios del sueño y la muerte y pronto se extendió a varias culturas antiguas a lo largo de la Ruta de la Seda, como los asirios , los griegos y China, donde el opio fue la razón subyacente de las Guerras del Opio durante la dinastía Qing . [ cita requerida ]
Revolución industrial

El uso médico de opioides para aliviar el dolor fue un gran avance en el siglo XIX. En 1803, el farmacéutico alemán Friedrich Wilhelm Adam Serturner extrajo la morfina , el ingrediente activo principal del opio, y lo nombró en honor a Morfeo , el dios griego de los sueños [1] . La extracción de opio no había llegado a su fin; pronto, se encontraron y aislaron más de 20 alcaloides farmacológicamente activos del opio. En 1853, un médico francés, Charles-Gabriel Pravaz, introdujo y modificó la jeringa hipodérmica para inyectar medicamentos directamente en el torrente sanguíneo [2] . Al eludir el sistema digestivo, la morfina inyectada logró la máxima biodisponibilidad , que se refería a la cantidad de medicamento que puede llegar a la circulación sistémica, el tiempo de inicio más corto y un régimen de dosificación controlado. Más tarde, en 1894, la compañía farmacéutica Bayer modificó la morfina y sus derivados naturales para sintetizar diacetilmorfina y la denominó Heroína [1] . Inicialmente, Bayers afirmó que la heroína es un análogo no adictivo de la morfina y puede usarse en medicina clínica para tratar la adicción a los opioides , que posteriormente se descubrió que era más adictiva que la morfina. [ cita requerida ]
Guerra del opio
Mientras tanto, el gobierno del Reino Unido inició un comercio trilateral con el Raj británico y la dinastía Qing. El gobierno Qing proporcionó hierbas de té a los británicos, mientras que el Raj británico proporcionó opio como producto médico y recreativo a los Qing. Debido a las características adictivas, el opio pronto creó un éxito masivo dentro de la dinastía Qing, lo que llevó a una fuerza militar deteriorada y una gran salida de riqueza [3] . Los gobernadores de la dinastía Qing tenían la intención de detener la importación de opio, lo que podría reducir los beneficios comerciales de los británicos. Un político llamado Lin ZeXu fue enviado a desechar el opio importado en 1839 en Humen, este evento, la destrucción del opio en Humen, se convirtió en el detonante de los británicos. Como resultado, comenzó la guerra del opio. [ cita requerida ]
Guerras mundiales
El uso y la demanda de analgésicos opioides siguió creciendo durante las guerras. La morfina y la cocaína se utilizaron en unidades médicas durante las guerras mundiales debido a sus propiedades analgésicas y estimulantes. Se utilizan comúnmente en países como Francia, Alemania y Gran Bretaña, ya que podían autoadministrarse principalmente antes de que llegara el médico de campo para minimizar el dolor que sufrían los soldados. Además de la morfina y la cocaína, otros analgésicos opioides como la metadona también se utilizaron en situaciones específicas durante la Segunda Guerra Mundial [4] . Cabe destacar que el uso de analgésicos opioides fue monitoreado y regulado de cerca por profesionales médicos incluso en tiempos de guerra para reducir el riesgo de adicción y abuso. [ cita requerida ]
Periodos postindustriales
La gente empezó a tomar conciencia del problema que suponía la adicción a los opioides. El abuso de opioides no cesó tras el estallido de la guerra; el fentanilo y otros derivados seguían desarrollándose y se comercializaban al público. Más tarde, la Organización Mundial de la Salud anunció una nueva guía de regulación para clasificar y separar los medicamentos de venta libre de los medicamentos con receta durante la década de 1950 [5] . Para impedir que la gente poseyera y vendiera opioides sin la instrucción de profesionales sanitarios, se establecieron posteriormente sanciones penales de penas mínimas. [ cita requerida ]

Sin embargo, el acceso limitado a los analgésicos opioides no logró suprimir la enorme demanda y los inconvenientes de los analgésicos opioides. Por ejemplo, el abuso de fentanilo ha dado lugar a la crisis de opioides más problemática en los Estados Unidos. El número de visitas de emergencia relacionadas con el fentanilo se duplicó durante la década de 2010 y casi 10.000 ciudadanos estadounidenses murieron por el abuso de fentanilo solo en 2015, lo que es casi el doble del año anterior [6] . Esto indicó que el abuso de analgésicos opioides siguió empeorando, lo que se muestra en la imagen proximal.
Los analgésicos opioides tienen dos sistemas de clasificación: estructura y efectos agonistas.
La estructura de los analgésicos opioides se divide en cuatro categorías principales, [7]

Todos los opioides derivados del fenantreno tienen una base de fenantreno rígida y se unen tanto al receptor opioide Mu (µ) como al receptor opioide Kappa (κ) [7] [8] . Los opioides derivados del fenantreno pueden ser naturales o semisintéticos. Los opioides naturales extraídos de las plantas Papaveraceae pertenecen a esta estructura, incluida la morfina, la codeína y la tebaína. La oxicodona y la heroína son ejemplos de opioides semisintéticos derivados del fenantreno que se sintetizan a partir de la morfina [9] .
Los derivados de difenilpropilamina, derivados de benzomorfano y derivados de fenilpiperidina son todos opioides sintéticos. Son opioides flexibles y solo se unen con el receptor opioide Mu (µ) [8] . Los derivados de difenilpropilamina incluyen metadona y propoxifeno . Los derivados de benzomorfano incluyen pentazocina y fenazocina . Los derivados de fenilpiperidina se pueden subdividir en dos categorías: meperidina (petidina) y derivados de fentanilo. Los derivados de fentanilo incluyen fentanilo, remifentanilo y alfentanilo [7] .
Los analgésicos opioides se pueden clasificar en agonistas completos, agonistas parciales, agonistas mixtos y antagonistas. [ cita requerida ]
Los agonistas opioides completos activan los receptores opioides y producen efectos opioides completos [18] . Algunos ejemplos de agonistas opioides completos son la morfina, la heroína y el fentanilo. Tienen un fuerte efecto analgésico o incluso anestésico que se puede utilizar en el tratamiento del dolor intenso [19] y durante la cirugía [20] .

Los agonistas opioides parciales activan el receptor opioide y producen muchos menos efectos opioides que los agonistas completos [18] . Un ejemplo de agonistas opioides parciales es el tramadol. [ cita requerida ]
Los agonistas/antagonistas opioides mixtos activan ciertos receptores opioides y bloquean otros receptores opioides. Por lo general, tienen un menor riesgo de abuso y adicción en comparación con los agonistas completos [21] . La buprenorfina, el butorfanol, la nalbufina y la pentazocina son algunos ejemplos de agonistas/antagonistas mixtos. [ cita requerida ]
Los antagonistas opioides se unen a los receptores opioides y no producen ningún efecto. La naloxona y la naltrexona son los únicos dos antagonistas opioides aprobados por la FDA para tratar la depresión respiratoria causada por una sobredosis de opioides. Se ha registrado que más de 26 500 personas se salvaron usando naloxona para tratar la sobredosis de opioides en los EE. UU. [22] .
Los analgésicos opioides son agonistas de los receptores opioides que se unen a los receptores opioides y los activan tanto en las neuronas presinápticas como en las postsinápticas. En las neuronas presinápticas, la activación de los receptores opioides desencadena la liberación del complejo G-beta-gamma , que luego interactúa con los canales de calcio dependientes del voltaje . [23] Esta interacción inhibe la apertura de los canales, lo que impide la entrada de iones de calcio en las neuronas presinápticas tras la llegada de un potencial de acción. Como resultado, se reduce la liberación de neurotransmisores , incluidos el glutamato, la calcitonina y la sustancia P, lo que bloquea eficazmente la transmisión de la señalización del dolor. [19]

En las neuronas postsinápticas, la activación de los receptores opioides también conduce a la liberación de subunidades G-beta-gamma. Las subunidades abrirían los canales de potasio acoplados a la proteína G, lo que provocaría la salida de iones de potasio. Esto despolariza las neuronas y contrarresta la hiperpolarización inducida por las señales de dolor. El potencial de acción se vuelve más difícil de generar dentro de las neuronas, inhibiendo así la transmisión de señales de dolor. [ cita requerida ]
Si bien la mayoría de los receptores opioides pueden producir efectos analgésicos, sus respuestas farmacodinámicas exactas varían según los receptores a los que se unen. La unión de los receptores Mu puede producir diversos efectos, incluidos vómitos, sedación y retención urinaria, mientras que la unión de los receptores Kappa puede contribuir a la depresión respiratoria, disforia y disnea. Por otro lado, la unión de los receptores Delta ejerce principalmente efectos analgésicos espinales. La afinidad de los fármacos por estos diferentes receptores determina sus efectos secundarios específicos. Por ejemplo, la morfina , un potente agonista de los receptores Mu, puede provocar sedación cuando los pacientes la toman. [ cita requerida ]
Las interacciones farmacológicas se pueden subdividir en dos tipos de interacción: interacción farmacocinética e interacción farmacodinámica [ cita requerida ]
El metabolismo principal de los fármacos opioides se realiza a través de la enzima CYP450 [24] . El metabolismo de fase 1 de los fármacos opioides se realiza principalmente a través de las enzimas CYP3A4 y CYP2D6 [25] [26] .
La mayoría del fentanilo, la oxicodona, la codeína y la metadona se metabolizan en la fase 1 a través de la enzima CYP3A4 [25] . La enzima CYP2D6 es responsable del metabolismo de la codeína [25] , con efectos menores en el metabolismo de la oxicodona y la metadona. Por lo tanto, los inhibidores de la enzima CYP3A4 o CYP2D6 aumentarán la concentración sérica de ciertos fármacos opioides, lo que puede provocar una sobredosis de opioides [26] .
Para prevenir la sobredosis de opioides, la naloxona se puede recetar junto con analgésicos opioides [27] . La naloxona es un antagonista del receptor opioide que puede revertir el efecto de los opioides [28] . La inyección intravenosa de 0,04-2 mg de naloxona puede tratar a pacientes que experimentan un paro cardíaco o depresión respiratoria debido a la toxicidad de los opioides [29] .
El efecto depresor del SNC es uno de los principales efectos secundarios de los analgésicos opioides, especialmente de los opioides de mayor potencia como el fentanilo y la meperidina. Se informó que se encontraron antihistamínicos en el 14,7% de las muertes por sobredosis de opioides en 2019 en los Estados Unidos [30] . Además, la difenhidramina , un antihistamínico de primera generación que ejerce un efecto sedante, se relacionó con más del 50% de las muertes relacionadas con antihistamínicos. Se sugirió que el efecto depresor del SNC de los opioides se sinergizó con el efecto sedante de los antihistamínicos, lo que provocó depresión respiratoria y resultó en la muerte [31] .
Los depresores del SNC como las benzodiazepinas y el alcohol también pueden potenciar el efecto depresor del SNC de los analgésicos opioides. Por lo tanto, se creará un efecto sinérgico y el usuario puede experimentar supresión de la respiración que puede provocar la muerte [32] . Además, un estudio de 2015 sobre la coadministración de benzodiazepinas y analgésicos opioides mostró un mayor uso de los servicios de emergencia por parte de los pacientes [33] . Por lo tanto, en general, los analgésicos opioides no deben prescribirse conjuntamente con ansiolíticos benzodiazepínicos como el diazepam. Los pacientes también deben evitar consumir alcohol cuando se administran analgésicos opioides, ya que la coadministración de opioides y alcohol conduce a más del 60% de sobredosis y muertes no intencionadas [34] .
Los efectos analgésicos de los opioides también podrían sinergizarse con los AINE (antiinflamatorios no esteroideos) y el paracetamol . La administración conjunta de AINE y analgésicos opioides puede aumentar el efecto analgésico y producir un mejor efecto analgésico [35] . El uso de paracetamol también podría reducir la dosis total de morfina necesaria como analgésico complementario después de la cirugía [36] .
Los analgésicos opioides se utilizan habitualmente para mejorar la experiencia del paciente cuando se trata de un dolor agudo intolerable. La fuente de la sensación de dolor puede ser el resultado de diversas razones, incluidas enfermedades crónicas, operaciones y fracturas, etc. El objetivo del uso de opioides también puede ser proporcionar cuidados paliativos para aliviar el dolor en enfermedades terminales, por ejemplo, cáncer, insuficiencia cardíaca crónica o enfermedad respiratoria en etapa avanzada. [ cita requerida ]
En general, las opciones de fármacos orales de primera línea disponibles para tratar el dolor moderado son oxicodona 5 mg, hidrocodona 5 mg con paracetamol o ibuprofeno e hidromorfona 2 mg. Para lograr un control adecuado del dolor, el paciente suele tomar las pastillas de 3 a 4 pastillas al día. Sin embargo, la única formulación intravenosa para el dolor moderado es la morfina de liberación inmediata 7,5 mg [37] [38]
En cuanto al dolor intenso, las opciones de fármacos orales son básicamente las mismas. La única diferencia es que la frecuencia aumentó de 3 a 4 pastillas por día a 4 a 6 pastillas por día, y la formulación intravenosa hace lo mismo. [37]
Las opciones de opioides para el tratamiento del dolor no se limitan a las mencionadas anteriormente; Tramadol, tapentadol y codeína también pueden usarse clínicamente en un entorno de segunda línea, dependiendo de la medicación concurrente. [37]
Los opioides logran su efecto terapéutico al unirse a tres tipos diferentes de receptores: Mu, Delta y Kappa. Cuando estos receptores se activan, alivian la sensación de dolor intenso y producen algunos efectos no deseados. El estreñimiento, las náuseas o vómitos, la fatiga, la confusión, la diuresis, el síndrome depresivo respiratorio y los dolores de cabeza son los efectos secundarios más comunes, mientras que el vaciamiento gástrico retardado, los calambres musculares y la hipotensión se observan con menos frecuencia [39].
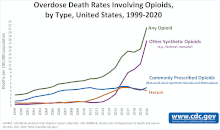
En Estados Unidos, los opioides son uno de los medicamentos más populares que se recetan para aliviar el dolor agudo y crónico. [40] Su uso generalizado ha provocado que se notifiquen más casos de sobredosis. Según los Centros para el Control y la Prevención de Enfermedades, los opioides provocaron más de ochenta mil muertes por sobredosis en 2021, diez veces más que en 1999. [ cita requerida ]
Para reducir el riesgo de abuso de opioides, existen analgésicos alternativos no opioides, como el paracetamol o los antiinflamatorios no esteroides (AINE). [41] En el caso de pacientes con afecciones menos graves, como dolor lumbar [42] o algunos casos de traumatismos agudos [43] , los AINE pueden actuar como analgésicos más suaves, que tienen menos probabilidades de causar adicción o dependencia de fármacos. Otro analgésico más suave, el paracetamol, también se puede utilizar en pacientes que experimentan un dolor menos intenso, como la osteoartritis de rodilla y cadera . [44]
Si el dolor de los pacientes no se controla bien con fármacos no opioides, se pueden considerar opioides de acción corta en lugar de formas de acción prolongada o de liberación prolongada. [45] Los opioides de acción corta pueden reducir eficazmente la duración de la permanencia del fármaco en el organismo, disminuyendo así el riesgo de adicción. También es crucial iniciar el tratamiento con la dosis efectiva más baja posible para minimizar los posibles efectos secundarios. En cuanto a la duración de la prescripción para el dolor agudo, se recomiendan tres días para evitar la adicción. [ cita requerida ]
Una vez iniciado el tratamiento con opioides, es esencial brindar una educación integral al paciente sobre los riesgos de sobredosis y las estrategias para la prevención, así como la eliminación de opioides. [46] Además, se debe recordar a los pacientes las consecuencias de la sobredosis, como la depresión respiratoria . [ cita requerida ]
Algunos signos sospechosos pueden indicar adicción a los opioides en los pacientes, como reclamar recetas perdidas o destruidas para adquirir más medicamentos. Es importante que los médicos verifiquen la validez de las reclamaciones y controlen de cerca el régimen de dosificación para identificar signos de adicción en una etapa temprana. [ cita requerida ]
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )