Un biosensor es un dispositivo analítico, utilizado para la detección de una sustancia química, que combina un componente biológico con un detector fisicoquímico . [1] [2] [3] [4] El elemento biológico sensible , por ejemplo, tejido, microorganismos, orgánulos , receptores celulares , enzimas , anticuerpos , ácidos nucleicos , etc., es un material de origen biológico o componente biomimético que interactúa con él, se une con o reconoce el analito en estudio. Los elementos biológicamente sensibles también pueden crearse mediante ingeniería biológica . El transductor o elemento detector , que transforma una señal en otra, funciona de forma fisicoquímica: óptica, piezoeléctrica , electroquímica, electroquimioluminiscencia , etc., resultante de la interacción del analito con el elemento biológico, para medir y cuantificar fácilmente. El dispositivo lector de biosensores se conecta con la electrónica asociada o procesadores de señales que son los principales responsables de la visualización de los resultados de una manera fácil de usar. [5] Esto a veces representa la parte más cara del dispositivo sensor; sin embargo, es posible generar una pantalla fácil de usar que incluya un transductor y un elemento sensible ( sensor holográfico ). Los lectores suelen diseñarse y fabricarse a medida para adaptarse a los diferentes principios de funcionamiento de los biosensores.
Un biosensor normalmente consta de un biorreceptor (enzima/anticuerpo/célula/ácido nucleico/aptámero), un componente transductor (material semiconductor/nanomaterial) y un sistema electrónico que incluye un amplificador de señal , un procesador y una pantalla. [6] Los transductores y la electrónica se pueden combinar, por ejemplo, en sistemas de microsensores basados en CMOS . [7] [8] El componente de reconocimiento, a menudo llamado biorreceptor, utiliza biomoléculas de organismos o receptores modelados a partir de sistemas biológicos para interactuar con el analito de interés. Esta interacción se mide mediante el biotransductor que genera una señal mensurable proporcional a la presencia del analito objetivo en la muestra. El objetivo general del diseño de un biosensor es permitir pruebas rápidas y convenientes en el punto de preocupación o atención donde se obtuvo la muestra. [1] [9] [10]
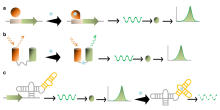
En un biosensor, el biorreceptor está diseñado para interactuar con el analito específico de interés para producir un efecto medible por el transductor. La alta selectividad para el analito entre una matriz de otros componentes químicos o biológicos es un requisito clave del biorreceptor. Si bien el tipo de biomolécula utilizada puede variar ampliamente, los biosensores se pueden clasificar según tipos comunes de interacciones de biorreceptores que involucran: anticuerpo/antígeno, [11] enzimas/ligandos, ácidos nucleicos/ADN, estructuras/células celulares o materiales biomiméticos. [12] [13]
Un inmunosensor utiliza la afinidad de unión muy específica de los anticuerpos por un compuesto o antígeno específico . La naturaleza específica de la interacción anticuerpo-antígeno es análoga a un cierre con llave en el sentido de que el antígeno sólo se unirá al anticuerpo si tiene la conformación correcta. Los eventos de unión dan como resultado un cambio fisicoquímico que, en combinación con un marcador, como moléculas fluorescentes, enzimas o radioisótopos, puede generar una señal. Existen limitaciones con el uso de anticuerpos en sensores: 1. La capacidad de unión del anticuerpo depende en gran medida de las condiciones del ensayo (p. ej., pH y temperatura), y 2. la interacción anticuerpo-antígeno es generalmente sólida; sin embargo, la unión puede verse alterada por reactivos caotrópicos . disolventes orgánicos o incluso radiación ultrasónica. [14] [15]
Las interacciones anticuerpo-antígeno también se pueden utilizar para pruebas serológicas o para la detección de anticuerpos circulantes en respuesta a una enfermedad específica. Es importante destacar que las pruebas serológicas se han convertido en una parte importante de la respuesta global a la pandemia de COVID-19 . [dieciséis]
El uso de anticuerpos como componente de biorreconocimiento de biosensores tiene varios inconvenientes. Tienen pesos moleculares elevados y estabilidad limitada, contienen enlaces disulfuro esenciales y su producción es costosa. En un enfoque para superar estas limitaciones, se han diseñado fragmentos de unión recombinantes ( Fab , Fv o scFv ) o dominios (VH, VHH ) de anticuerpos. [17] En otro enfoque, se han diseñado pequeños andamios proteicos con propiedades biofísicas favorables para generar familias artificiales de proteínas de unión a antígenos (AgBP), capaces de unirse específicamente a diferentes proteínas diana conservando al mismo tiempo las propiedades favorables de la molécula original. Los elementos de la familia que se unen específicamente a un antígeno diana determinado, a menudo se seleccionan in vitro mediante técnicas de presentación: presentación en fagos , presentación en ribosomas , presentación en levaduras o presentación en ARNm . Las proteínas de unión artificiales son mucho más pequeñas que los anticuerpos (generalmente menos de 100 residuos de aminoácidos), tienen una gran estabilidad, carecen de enlaces disulfuro y pueden expresarse con alto rendimiento en entornos celulares reductores como el citoplasma bacteriano, a diferencia de los anticuerpos y sus derivados. . [18] [19] Por lo tanto, son especialmente adecuados para crear biosensores. [20] [21]
Las capacidades de unión específicas y la actividad catalítica de las enzimas las convierten en biorreceptores populares. El reconocimiento del analito se permite a través de varios mecanismos posibles: 1) la enzima convierte el analito en un producto que es detectable por sensor, 2) detecta la inhibición o activación de la enzima por el analito, o 3) monitorea la modificación de las propiedades de la enzima resultantes de la interacción con el analito. . [15] Las principales razones para el uso común de enzimas en biosensores son: 1) capacidad de catalizar una gran cantidad de reacciones; 2) potencial para detectar un grupo de analitos (sustratos, productos, inhibidores y moduladores de la actividad catalítica); y 3) idoneidad con varios métodos de transducción diferentes para detectar el analito. En particular, dado que las enzimas no se consumen en las reacciones, el biosensor se puede utilizar fácilmente de forma continua. La actividad catalítica de las enzimas también permite límites de detección más bajos en comparación con las técnicas de unión comunes. Sin embargo, la vida útil del sensor está limitada por la estabilidad de la enzima.
Los anticuerpos tienen una constante de unión alta , superior a 10^8 L/mol, lo que representa una asociación casi irreversible una vez que se ha formado la pareja antígeno-anticuerpo. Para ciertas moléculas de analito, como la glucosa, existen proteínas de unión por afinidad que se unen a su ligando con una alta especificidad como un anticuerpo, pero con una constante de unión mucho menor, del orden de 10 ^ 2 a 10 ^ 4 L / mol. La asociación entre analito y receptor es entonces de naturaleza reversible y además de la pareja entre ambos también se producen sus moléculas libres en una concentración mensurable. En el caso de la glucosa, por ejemplo, la concanavalina A puede funcionar como receptor de afinidad mostrando una constante de unión de 4x10^2 L/mol. [22] Schultz y Sims propusieron el uso de receptores de unión por afinidad con fines de biodetección en 1979 [23] y posteriormente se configuraron en un ensayo fluorescente para medir la glucosa en el rango fisiológico relevante entre 4,4 y 6,1 mmol/L. [24] El principio del sensor tiene la ventaja de que no consume el analito en una reacción química como ocurre en los ensayos enzimáticos.
Los biosensores que emplean receptores basados en ácidos nucleicos pueden basarse en interacciones de emparejamiento de bases complementarias denominadas genosensores o imitadores de anticuerpos específicos basados en ácidos nucleicos (aptámeros) como aptasensores. [25] En el primero, el proceso de reconocimiento se basa en el principio del emparejamiento de bases complementarias , adenina:timina y citosina:guanina en el ADN . Si se conoce la secuencia de ácido nucleico diana, se pueden sintetizar, marcar y luego inmovilizar secuencias complementarias en el sensor. El evento de hibridación puede detectarse ópticamente y determinarse la presencia de ADN/ARN diana. En este último, los aptámeros generados contra el objetivo lo reconocen mediante la interacción de interacciones no covalentes específicas y el ajuste inducido. Estos aptámeros se pueden marcar fácilmente con un fluoróforo/nanopartículas metálicas para la detección óptica o se pueden emplear para plataformas de detección basadas en voladizo o electroquímicas sin etiquetas para una amplia gama de moléculas objetivo o objetivos complejos como células y virus. [26] [27] Además, los aptámeros se pueden combinar con enzimas de ácido nucleico, como las ADNzimas que escinden el ARN, proporcionando tanto reconocimiento de objetivos como generación de señales en una sola molécula, lo que muestra aplicaciones potenciales en el desarrollo de biosensores múltiples. [28]
Se ha propuesto que se puedan aprovechar resonadores ópticos integrados adecuadamente optimizados para detectar modificaciones epigenéticas (por ejemplo, metilación del ADN, modificaciones postraduccionales de histonas) en fluidos corporales de pacientes afectados por cáncer u otras enfermedades. [29] Actualmente se están desarrollando a nivel de investigación biosensores fotónicos con ultrasensibilidad para detectar fácilmente células cancerosas en la orina del paciente. [30] Diferentes proyectos de investigación tienen como objetivo desarrollar nuevos dispositivos portátiles que utilicen cartuchos desechables, baratos y respetuosos con el medio ambiente, que requieran un manejo sencillo sin necesidad de procesamiento, lavado o manipulación posterior por parte de técnicos expertos. [31]
Los orgánulos forman compartimentos separados dentro de las células y normalmente realizan funciones de forma independiente. Los diferentes tipos de orgánulos tienen diversas vías metabólicas y contienen enzimas para cumplir su función. Los orgánulos de uso común incluyen lisosomas, cloroplastos y mitocondrias. El patrón de distribución espacio-temporal del calcio está estrechamente relacionado con la vía de señalización ubicua. Las mitocondrias participan activamente en el metabolismo de los iones de calcio para controlar la función y también modular las vías de señalización relacionadas con el calcio. Los experimentos han demostrado que las mitocondrias tienen la capacidad de responder a las altas concentraciones de calcio generadas en sus proximidades abriendo los canales de calcio. [32] De esta manera, las mitocondrias se pueden utilizar para detectar la concentración de calcio en el medio y la detección es muy sensible debido a la alta resolución espacial. Otra aplicación de las mitocondrias es la detección de la contaminación del agua. La toxicidad de los compuestos detergentes dañará la estructura celular y subcelular, incluidas las mitocondrias. Los detergentes provocarán un efecto de hinchazón que podría medirse mediante un cambio de absorbancia. Los datos del experimento muestran que la tasa de cambio es proporcional a la concentración de detergente, lo que proporciona un alto estándar de precisión de detección. [33]
Las células se utilizan a menudo en biorreceptores porque son sensibles al entorno circundante y pueden responder a todo tipo de estimulantes. Las células tienden a adherirse a la superficie para poder inmovilizarlas fácilmente. En comparación con los orgánulos, permanecen activos durante más tiempo y su reproducibilidad los hace reutilizables. Se utilizan comúnmente para detectar parámetros globales como condiciones de estrés, toxicidad y derivados orgánicos. También se pueden utilizar para controlar el efecto del tratamiento de los medicamentos. Una aplicación es utilizar células para determinar los herbicidas que son los principales contaminantes acuáticos. [34] Las microalgas quedan atrapadas en una microfibra de cuarzo y la fluorescencia de la clorofila modificada por herbicidas se recoge en la punta de un haz de fibras ópticas y se transmite a un fluorímetro. Las algas se cultivan continuamente para obtener mediciones optimizadas. Los resultados muestran que el límite de detección de ciertos herbicidas puede alcanzar un nivel de concentración inferior a ppb. Algunas celdas también se pueden utilizar para controlar la corrosión microbiana. [35] Pseudomonassp. Se aísla de la superficie del material corroído y se inmoviliza sobre una membrana de acetilcelulosa. La actividad respiratoria se determina midiendo el consumo de oxígeno. Existe una relación lineal entre la corriente generada y la concentración de ácido sulfúrico . El tiempo de respuesta está relacionado con la carga de las celdas y los entornos circundantes y puede controlarse a no más de 5 minutos.
Los tejidos se utilizan como biosensores por la abundancia de enzimas existentes. Las ventajas de los tejidos como biosensores incluyen las siguientes: [36]
También existen algunas desventajas de los tejidos, como la falta de especificidad debido a la interferencia de otras enzimas y un mayor tiempo de respuesta debido a la barrera de transporte.
Los biosensores microbianos aprovechan la respuesta de las bacterias a una sustancia determinada. Por ejemplo, el arsénico se puede detectar utilizando el operón ars que se encuentra en varios taxones bacterianos. [37]

Una parte importante de un biosensor es unir los elementos biológicos (pequeñas moléculas/proteínas/células) a la superficie del sensor (ya sea metal, polímero o vidrio). La forma más sencilla es funcionalizar la superficie para recubrirla con los elementos biológicos. Esto se puede realizar mediante polilisina, aminosilano, epoxisilano o nitrocelulosa en el caso de chips de silicio/vidrio de sílice. A continuación también se puede fijar el agente biológico unido, por ejemplo mediante depósito capa por capa de recubrimientos poliméricos con cargas alternativas. [38]
Alternativamente, se pueden usar redes tridimensionales ( hidrogel / xerogel ) para atraparlos química o físicamente (por lo que atrapado químicamente se entiende que el elemento biológico se mantiene en su lugar mediante un vínculo fuerte, mientras que físicamente se mantienen en su lugar al no poder hacerlo). pasar a través de los poros de la matriz del gel). El hidrogel más comúnmente utilizado es el sol-gel , sílice vítrea generada por polimerización de monómeros de silicato (añadidos como ortosilicatos de tetraalquilo, como TMOS o TEOS ) en presencia de elementos biológicos (junto con otros polímeros estabilizantes, como PEG ) en el caso de atrapamiento físico. [39]
Otro grupo de hidrogeles, que se endurecen en condiciones adecuadas para células o proteínas, son los hidrogeles de acrilato , que polimerizan tras la iniciación por radicales . Un tipo de iniciador de radicales es un radical peróxido , generalmente generado combinando un persulfato con TEMED ( el gel de poliacrilamida también se usa comúnmente para la electroforesis de proteínas ), [40] alternativamente se puede usar luz en combinación con un fotoiniciador, como DMPA ( 2, 2-dimetoxi-2-fenilacetofenona ). [41] Los materiales inteligentes que imitan los componentes biológicos de un sensor también pueden clasificarse como biosensores utilizando solo el sitio activo o catalítico o configuraciones análogas de una biomolécula. [42]

Los biosensores se pueden clasificar por su tipo de biotransductor . Los tipos más comunes de biotransductores utilizados en biosensores son:
Los biosensores electroquímicos normalmente se basan en la catálisis enzimática de una reacción que produce o consume electrones (estas enzimas se denominan con razón enzimas redox). El sustrato del sensor suele contener tres electrodos ; un electrodo de referencia , un electrodo de trabajo y un contraelectrodo. El analito objetivo participa en la reacción que tiene lugar en la superficie del electrodo activo, y la reacción puede provocar la transferencia de electrones a través de la doble capa (produciendo una corriente) o puede contribuir al potencial de la doble capa (produciendo un voltaje). Podemos medir la corriente (la velocidad del flujo de electrones ahora es proporcional a la concentración del analito) a un potencial fijo o el potencial se puede medir a una corriente cero (esto da una respuesta logarítmica). Tenga en cuenta que el potencial del electrodo activo o de trabajo es sensible a la carga espacial y esto se utiliza con frecuencia. Además, la detección eléctrica directa y sin etiquetas de pequeños péptidos y proteínas es posible mediante sus cargas intrínsecas utilizando transistores de efecto de campo sensibles a iones biofuncionalizados . [43]
Otro ejemplo, el biosensor potenciométrico (potencial producido a corriente cero) da una respuesta logarítmica con un alto rango dinámico. Estos biosensores a menudo se fabrican mediante serigrafía de los patrones de electrodos sobre un sustrato de plástico, recubierto con un polímero conductor y luego se les une alguna proteína (enzima o anticuerpo). Tienen sólo dos electrodos y son extremadamente sensibles y robustos. Permiten la detección de analitos en niveles que antes solo se podían alcanzar mediante HPLC y LC/MS y sin una preparación rigurosa de la muestra. Todos los biosensores suelen implicar una preparación mínima de la muestra, ya que el componente de detección biológica es altamente selectivo para el analito en cuestión. La señal se produce por cambios electroquímicos y físicos en la capa de polímero conductor debido a los cambios que ocurren en la superficie del sensor. Dichos cambios pueden atribuirse a la fuerza iónica, el pH, la hidratación y las reacciones redox, estas últimas debidas a que el marcador enzimático gira sobre un sustrato. [44] Los transistores de efecto de campo, en los que la región de la puerta se ha modificado con una enzima o anticuerpo, también pueden detectar concentraciones muy bajas de varios analitos, ya que la unión del analito a la región de la puerta del FET provoca un cambio en el drenaje. fuente de corriente.
El desarrollo de biosensores basados en espectroscopia de impedancia ha ido ganando terreno hoy en día y muchos de estos dispositivos/desarrollos se encuentran en el mundo académico y la industria. Se ha demostrado que uno de estos dispositivos, basado en una celda electroquímica de 4 electrodos, que utiliza una membrana de alúmina nanoporosa, detecta concentraciones bajas de alfa trombina humana en presencia de un fondo alto de albúmina sérica. [45] También se han utilizado electrodos interdigitados para biosensores de impedancia. [46]


Se ha demostrado que el uso de canales iónicos ofrece una detección altamente sensible de moléculas biológicas objetivo. [47] Al incrustar los canales iónicos en membranas bicapa soportadas o unidas (t-BLM) unidas a un electrodo de oro, se crea un circuito eléctrico. Las moléculas de captura, como los anticuerpos, se pueden unir al canal iónico de modo que la unión de la molécula objetivo controle el flujo de iones a través del canal. Esto da como resultado un cambio mensurable en la conducción eléctrica que es proporcional a la concentración del objetivo.
Se puede crear un biosensor de interruptor de canal iónico (ICS) utilizando gramicidina, un canal peptídico dimérico, en una membrana bicapa atada. [48] Un péptido de gramicidina, con anticuerpo adjunto, es móvil y el otro es fijo. La ruptura del dímero detiene la corriente iónica a través de la membrana. La magnitud del cambio en la señal eléctrica aumenta considerablemente al separar la membrana de la superficie metálica utilizando un espaciador hidrófilo.
Se ha demostrado la detección cuantitativa de una amplia clase de especies objetivo, incluidas proteínas, bacterias, fármacos y toxinas, utilizando diferentes configuraciones de membrana y captura. [49] [50] El proyecto de investigación europeo Greensense desarrolla un biosensor para realizar análisis cuantitativos de drogas de abuso como THC, morfina y cocaína [51] en saliva y orina.
Un biosensor sin reactivos puede monitorear un analito objetivo en una mezcla biológica compleja sin reactivo adicional. Por tanto, puede funcionar de forma continua si está inmovilizado sobre un soporte sólido. Un biosensor fluorescente reacciona a la interacción con su analito objetivo mediante un cambio en sus propiedades de fluorescencia. Se puede obtener un biosensor fluorescente sin reactivo (biosensor de RF) integrando un receptor biológico, que está dirigido contra el analito objetivo, y un fluoróforo solvatocrómico , cuyas propiedades de emisión son sensibles a la naturaleza de su entorno local, en una sola macromolécula. El fluoróforo transduce el evento de reconocimiento en una señal óptica mensurable. El uso de fluoróforos extrínsecos, cuyas propiedades de emisión difieren ampliamente de las de los fluoróforos intrínsecos de proteínas, triptófano y tirosina, permite detectar y cuantificar inmediatamente el analito en mezclas biológicas complejas. La integración del fluoróforo debe realizarse en un sitio donde sea sensible a la unión del analito sin perturbar la afinidad del receptor.
Los anticuerpos y las familias artificiales de proteínas de unión a antígenos (AgBP) son muy adecuados para proporcionar el módulo de reconocimiento de los biosensores de RF, ya que pueden dirigirse contra cualquier antígeno (consulte el párrafo sobre biorreceptores). Se ha descrito un enfoque general para integrar un fluoróforo solvatocrómico en una AgBP cuando se conoce la estructura atómica del complejo con su antígeno, y así transformarlo en un biosensor de RF. [20] Se identifica un residuo de AgBP en las proximidades del antígeno en su complejo. Este residuo se transforma en cisteína mediante mutagénesis dirigida. El fluoróforo está químicamente acoplado a la cisteína mutante. Cuando el diseño tiene éxito, el fluoróforo acoplado no impide la unión del antígeno, esta unión protege al fluoróforo del disolvente y puede detectarse mediante un cambio de fluorescencia. Esta estrategia también es válida para fragmentos de anticuerpos. [52] [53]
Sin embargo, a falta de datos estructurales específicos, se deben aplicar otras estrategias. Los anticuerpos y las familias artificiales de AgBP están constituidas por un conjunto de posiciones de residuos hipervariables (o aleatorias), ubicadas en una subregión única de la proteína y sostenidas por una estructura polipeptídica constante. Los residuos que forman el sitio de unión para un antígeno determinado se seleccionan entre los residuos hipervariables. Es posible transformar cualquier AgBP de estas familias en un biosensor de RF, específico del antígeno diana, simplemente acoplando un fluoróforo solvatocrómico a uno de los residuos hipervariables que tienen poca o ninguna importancia para la interacción con el antígeno, después de cambiar este residuo. en cisteína por mutagénesis. Más específicamente, la estrategia consiste en cambiar individualmente los residuos de las posiciones hipervariables en cisteína a nivel genético, en acoplar químicamente un fluoróforo solvatocrómico con la cisteína mutante y luego mantener los conjugados resultantes que tienen la mayor sensibilidad (parámetro que involucra tanto afinidad como variación de la señal de fluorescencia). [21] Este enfoque también es válido para familias de fragmentos de anticuerpos. [54]
Estudios a posteriori han demostrado que los mejores biosensores fluorescentes sin reactivos se obtienen cuando el fluoróforo no realiza interacciones no covalentes con la superficie del biorreceptor, lo que aumentaría la señal de fondo, y cuando interactúa con una bolsa de unión en la superficie del antígeno diana. [55] Los biosensores de RF que se obtienen mediante los métodos anteriores pueden funcionar y detectar analitos objetivo dentro de las células vivas. [56]
Los biosensores magnéticos utilizan partículas o cristales paramagnéticos o supraparamagnéticos para detectar interacciones biológicas. Algunos ejemplos podrían ser la inductancia de la bobina, la resistencia u otras propiedades magnéticas. Es común utilizar nano o micropartículas magnéticas. En la superficie de tales partículas se encuentran los biorreceptores, que pueden ser ADN (complementario a una secuencia o aptámeros), anticuerpos u otros. La unión del biorreceptor afectará algunas de las propiedades de las partículas magnéticas que pueden medirse mediante susceptometría de CA, [57] un sensor de efecto Hall, [58] un dispositivo de magnetorresistencia gigante, [59] u otros.
Los sensores piezoeléctricos utilizan cristales que sufren una deformación elástica cuando se les aplica un potencial eléctrico. Un potencial alterno (AC) produce una onda estacionaria en el cristal a una frecuencia característica. Esta frecuencia depende en gran medida de las propiedades elásticas del cristal, de modo que si un cristal está recubierto con un elemento de reconocimiento biológico, la unión de un analito objetivo (grande) a un receptor producirá un cambio en la frecuencia de resonancia, lo que da una unión. señal. En un modo que utiliza ondas acústicas superficiales (SAW), la sensibilidad aumenta considerablemente. Esta es una aplicación especializada de la microbalanza de cristal de cuarzo como biosensor.
La electroquimioluminiscencia (ECL) es hoy en día una técnica líder en biosensores. [60] [61] [62] Dado que las especies excitadas se producen con un estímulo electroquímico en lugar de con una fuente de excitación de luz, ECL muestra una relación señal-ruido mejorada en comparación con la fotoluminiscencia, con efectos minimizados debido a la dispersión de la luz y el fondo de luminiscencia. . En particular, el ECL correactante que opera en solución acuosa tamponada en la región de potenciales positivos (mecanismo de reducción oxidativa) definitivamente impulsó el ECL para inmunoensayo, como lo confirman numerosas aplicaciones de investigación y, más aún, la presencia de importantes empresas que desarrollaron hardware comercial para análisis de inmunoensayos de alto rendimiento en un mercado que vale miles de millones de dólares cada año.
Los biosensores termométricos son raros.
El MOSFET (transistor de efecto de campo semiconductor de óxido metálico, o transistor MOS) fue inventado por Mohamed M. Atalla y Dawon Kahng en 1959 y demostrado en 1960. [63] Dos años más tarde, Leland C. Clark y Champ Lyons inventaron el primer biosensor en 1962. [64] [65] Posteriormente se desarrollaron biosensores MOSFET (BioFET) y desde entonces se han utilizado ampliamente para medir parámetros físicos , químicos , biológicos y ambientales . [66]
El primer BioFET fue el transistor de efecto de campo sensible a iones (ISFET), inventado por Piet Bergveld para aplicaciones electroquímicas y biológicas en 1970. [67] [68] el FET de adsorción (ADFET) fue patentado por PF Cox en 1974, y un I. Lundstrom, MS Shivaraman, CS Svenson y L. Lundkvist demostraron un MOSFET sensible al hidrógeno en 1975. [66] El ISFET es un tipo especial de MOSFET con una compuerta a cierta distancia, [66] y donde la compuerta metálica se reemplaza por una membrana sensible a iones , una solución electrolítica y un electrodo de referencia . [69] El ISFET se utiliza ampliamente en aplicaciones biomédicas , como la detección de hibridación de ADN , detección de biomarcadores en sangre , detección de anticuerpos , medición de glucosa , detección de pH y tecnología genética . [69]
A mediados de la década de 1980, se habían desarrollado otros BioFET, incluido el sensor de gas FET (GASFET), el sensor de presión FET (PRESSFET), el transistor químico de efecto de campo (ChemFET), el ISFET de referencia (REFET) y el FET modificado con enzimas (ENFET). y FET inmunológicamente modificado (IMFET). [66] A principios de la década de 2000, se habían desarrollado BioFET como el transistor de efecto de campo de ADN (DNAFET), el FET modificado genéticamente (GenFET) y el BioFET de potencial celular (CPFET). [69]
La ubicación adecuada de los biosensores depende de su campo de aplicación, que a grandes rasgos se puede dividir en biotecnología , agricultura , tecnología alimentaria y biomedicina .
En biotecnología, el análisis de la composición química del caldo de cultivo se puede realizar en línea, en línea, en línea y fuera de línea. Como lo describe la Administración de Alimentos y Medicamentos de EE. UU. ( FDA ), la muestra no se elimina del flujo de proceso para los sensores en línea, mientras que se desvía del proceso de fabricación para las mediciones en línea. Para sensores en línea, la muestra se puede extraer y analizar muy cerca del flujo del proceso. [70] Un ejemplo de esto último es el seguimiento de la lactosa en una planta procesadora de lácteos. [71] Los biosensores fuera de línea se comparan con técnicas bioanalíticas que no funcionan en el campo, sino en el laboratorio. Estas técnicas se utilizan principalmente en agricultura, tecnología alimentaria y biomedicina.
En aplicaciones médicas, los biosensores generalmente se clasifican en sistemas in vitro e in vivo . Una medición con biosensor in vitro se realiza en un tubo de ensayo, una placa de cultivo, una placa de microtitulación o en cualquier otro lugar fuera de un organismo vivo. El sensor utiliza un biorreceptor y un transductor como se describe anteriormente. Un ejemplo de biosensor in vitro es un biosensor enzimático-conductimétrico para la monitorización de glucosa en sangre . Existe el desafío de crear un biosensor que funcione según el principio de prueba en el lugar de atención , es decir, en el lugar donde se necesita la prueba. [72] [73] El desarrollo de biosensores portátiles se encuentra entre esos estudios. [74] La eliminación de las pruebas de laboratorio puede ahorrar tiempo y dinero. Una aplicación de un biosensor POCT puede ser la prueba del VIH en áreas donde es difícil realizar la prueba a los pacientes. Se puede enviar un biosensor directamente al lugar y se puede utilizar una prueba rápida y sencilla.

Un biosensor in vivo es un dispositivo implantable que funciona dentro del cuerpo. Por supuesto, los implantes de biosensores deben cumplir estrictas normas de esterilización para evitar una respuesta inflamatoria inicial tras la implantación. La segunda preocupación se refiere a la biocompatibilidad a largo plazo , es decir, la interacción no dañina con el entorno corporal durante el período de uso previsto. [76] Otro problema que surge es el fracaso. Si falla, el dispositivo debe retirarse y reemplazarse, lo que provoca una cirugía adicional. Un ejemplo de aplicación de un biosensor in vivo sería el control de la insulina en el cuerpo, que aún no está disponible.
Los implantes biosensores más avanzados se han desarrollado para la monitorización continua de la glucosa. [77] [78] La figura muestra un dispositivo para el cual se utiliza una carcasa de Ti y una batería como se establece para implantes cardiovasculares como marcapasos y desfibriladores . [75] Su tamaño lo determina la batería según sea necesario para una vida útil de un año. Los datos de glucosa medidos se transmitirán de forma inalámbrica fuera del cuerpo dentro de la banda MICS 402-405 MHz aprobada para implantes médicos.
Los biosensores también pueden integrarse en los sistemas de telefonía móvil, haciéndolos fáciles de usar y accesibles para un gran número de usuarios. [79]

Existen muchas aplicaciones potenciales de biosensores de varios tipos. Los principales requisitos para que un enfoque de biosensor sea valioso en términos de investigación y aplicaciones comerciales son la identificación de una molécula objetivo, la disponibilidad de un elemento de reconocimiento biológico adecuado y la posibilidad de que los sistemas de detección portátiles desechables sean preferidos a las sensibles técnicas de laboratorio. en algunas situaciones. Algunos ejemplos son:
Un ejemplo común de biosensor comercial es el biosensor de glucosa en sangre , que utiliza la enzima glucosa oxidasa para descomponer la glucosa en sangre. Al hacerlo, primero oxida la glucosa y utiliza dos electrones para reducir el FAD (un componente de la enzima) a FADH 2 . Éste, a su vez, es oxidado por el electrodo en varios pasos. La corriente resultante es una medida de la concentración de glucosa. En este caso, el electrodo es el transductor y la enzima es el componente biológicamente activo.
Un canario en una jaula , como el que utilizan los mineros para advertir de la presencia de gas, podría considerarse un biosensor. Muchas de las aplicaciones actuales de biosensores son similares, ya que utilizan organismos que responden a sustancias tóxicas en concentraciones mucho más bajas de las que los humanos pueden detectar para advertir de su presencia. Dichos dispositivos se pueden utilizar en monitoreo ambiental , [81] detección de gases traza y en instalaciones de tratamiento de agua.
Los monitores de glucosa disponibles comercialmente se basan en la detección amperométrica de la glucosa mediante la glucosa oxidasa , que oxida la glucosa produciendo peróxido de hidrógeno que es detectado por el electrodo. Para superar la limitación de los sensores amperométricos, se está realizando una avalancha de investigaciones sobre nuevos métodos de detección, como los biosensores de glucosa fluorescentes . [83]
El sensor de imágenes de reflectancia interferométrica (IRIS) se basa en los principios de interferencia óptica y consta de un sustrato de óxido de silicio, óptica estándar y LED coherentes de baja potencia. Cuando se ilumina la luz a través de un objetivo de bajo aumento sobre el sustrato en capas de silicio-óxido de silicio, se produce una firma interferométrica. A medida que la biomasa, que tiene un índice de refracción similar al del óxido de silicio, se acumula en la superficie del sustrato, se produce un cambio en la firma interferométrica y el cambio puede correlacionarse con una masa cuantificable. Daaboul et al. utilizó IRIS para producir una sensibilidad sin etiqueta de aproximadamente 19 ng/ml. [84] Ahn et al. mejoró la sensibilidad del IRIS mediante una técnica de etiquetado masivo. [85]
Desde su publicación inicial, IRIS se ha adaptado para realizar diversas funciones. En primer lugar, IRIS integró una capacidad de obtención de imágenes de fluorescencia en el instrumento de imágenes interferométricas como una forma potencial de abordar la variabilidad de los microarrays de proteínas de fluorescencia. [86] Brevemente, la variación en los microarrays de fluorescencia se deriva principalmente de una inmovilización inconsistente de proteínas en las superficies y puede causar diagnósticos erróneos en los microarrays de alergia. [87] Para corregir cualquier variación en la inmovilización de proteínas, los datos adquiridos en la modalidad de fluorescencia se normalizan con los datos adquiridos en la modalidad sin etiquetas. [87] IRIS también se ha adaptado para realizar el recuento de nanopartículas individuales simplemente cambiando el objetivo de bajo aumento utilizado para la cuantificación de biomasa sin etiquetas a un objetivo de mayor aumento. [88] [89] Esta modalidad permite la discriminación de tamaño en muestras biológicas humanas complejas. Monroe y cols. utilizó IRIS para cuantificar los niveles de proteína añadidos a la sangre total y al suero humanos y determinó la sensibilización a alérgenos en muestras de sangre humana caracterizadas sin procesamiento de muestras. [90] Otros usos prácticos de este dispositivo incluyen la detección de virus y patógenos. [91]
Existen varias aplicaciones de los biosensores en el análisis de alimentos. [92] [93] [94] [95] En la industria alimentaria, las ópticas recubiertas con anticuerpos se utilizan comúnmente para detectar patógenos y toxinas alimentarias. Comúnmente, el sistema de luz en estos biosensores es la fluorescencia, ya que este tipo de medición óptica puede amplificar mucho la señal.
Se ha desarrollado una gama de ensayos de unión de ligandos e inmunoensayos para la detección y medición de moléculas pequeñas, como vitaminas solubles en agua y contaminantes químicos ( residuos de fármacos ), como sulfonamidas y agonistas beta, para su uso en sistemas de sensores basados en SPR , a menudo adaptado de ELISA existente u otro ensayo inmunológico. Estos son de uso generalizado en toda la industria alimentaria.
Los biosensores podrían usarse para monitorear contaminantes del aire , el agua y el suelo, como pesticidas, sustancias potencialmente cancerígenas, mutagénicas y/o tóxicas y sustancias químicas que alteran el sistema endocrino. [96] [97]
Por ejemplo, los bionanotecnólogos desarrollaron un biosensor viable, ROSALIND 2.0 , que puede detectar niveles de diversos contaminantes del agua . [98] [99]
Debido a que el ozono filtra la dañina radiación ultravioleta, el descubrimiento de agujeros en la capa de ozono de la atmósfera terrestre ha generado preocupación sobre cuánta luz ultravioleta llega a la superficie terrestre. De particular preocupación son las cuestiones de hasta qué punto penetra la radiación ultravioleta en el agua del mar y cómo afecta a los organismos marinos , especialmente al plancton (microorganismos flotantes) y a los virus que atacan al plancton. El plancton forma la base de las cadenas alimenticias marinas y se cree que afecta la temperatura y el clima de nuestro planeta mediante la absorción de CO 2 para la fotosíntesis.
Deneb Karentz, investigador del Laboratorio de Radiobiología y Salud Ambiental ( Universidad de California, San Francisco ) ha ideado un método sencillo para medir la penetración y la intensidad de los rayos ultravioleta. Trabajando en el Océano Antártico, sumergió a varias profundidades finas bolsas de plástico que contenían cepas especiales de E. coli que son casi totalmente incapaces de reparar el daño de la radiación ultravioleta en su ADN. Las tasas de muerte bacteriana en estas bolsas se compararon con las tasas en bolsas de control no expuestas del mismo organismo. Los "biosensores" bacterianos revelaron daños ultravioleta importantes y constantes a profundidades de 10 m y frecuentemente a 20 y 30 m. Karentz planea estudios adicionales sobre cómo los rayos ultravioleta pueden afectar las floraciones estacionales de plancton (crecimiento acelerado) en los océanos. [100]
La metástasis es la propagación del cáncer de una parte del cuerpo a otra a través del sistema circulatorio o del sistema linfático. [101] A diferencia de las pruebas de imágenes radiológicas (mamografías), que envían formas de energía (rayos X, campos magnéticos, etc.) a través del cuerpo para tomar únicamente fotografías del interior, los biosensores tienen el potencial de probar directamente el poder maligno del tumor. La combinación de un elemento biológico y detector permite un requisito de muestra pequeño, un diseño compacto, señales rápidas, detección rápida, alta selectividad y alta sensibilidad para el analito que se está estudiando. En comparación con las pruebas de imagen radiológicas habituales, los biosensores tienen la ventaja no sólo de descubrir hasta qué punto se ha extendido el cáncer y comprobar si el tratamiento es eficaz, sino que también son una forma más económica y eficiente (en tiempo, coste y productividad) de evaluar la metástasis en las primeras etapas de la enfermedad. cáncer.
Investigadores de ingeniería biológica han creado biosensores oncológicos para el cáncer de mama. [102] El cáncer de mama es el principal cáncer común entre las mujeres en todo el mundo. [103] Un ejemplo sería una microbalanza de cristal de cuarzo-transferrina (QCM). Como biosensor, las microbalanzas de cristal de cuarzo producen oscilaciones en la frecuencia de la onda estacionaria del cristal a partir de un potencial alterno para detectar cambios de masa de nanogramos. Estos biosensores están diseñados específicamente para interactuar y tienen una alta selectividad por los receptores en las superficies celulares (cancerosas y normales). Idealmente, esto proporciona una detección cuantitativa de células con este receptor por área de superficie en lugar de una detección de imagen cualitativa proporcionada por mamografías.
Seda Atay, investigadora de biotecnología de la Universidad Hacettepe, observó experimentalmente esta especificidad y selectividad entre un QCM y células mamarias MDA-MB 231 , células MCF 7 y células MDA-MB 231 hambrientas in vitro. [102] Con otros investigadores, ideó un método para lavar estas diferentes células niveladas metastásicas sobre los sensores para medir los cambios de masa debido a diferentes cantidades de receptores de transferrina. En particular, el poder metastásico de las células de cáncer de mama puede determinarse mediante microbalanzas de cristal de cuarzo con nanopartículas y transferrina que potencialmente se unirían a los receptores de transferrina en las superficies de las células cancerosas. Existe una selectividad muy alta por los receptores de transferrina porque están sobreexpresados en las células cancerosas. Si las células tienen una alta expresión de receptores de transferrina, lo que demuestra su alto poder metastásico, tienen mayor afinidad y se unen más al QCM que mide el aumento de masa. Dependiendo de la magnitud del cambio de masa de nanogramos, se puede determinar la potencia metastásica.
Además, en los últimos años se ha prestado mucha atención a la detección de biomarcadores de cáncer de pulmón sin biopsia. En este sentido, los biosensores son herramientas muy atractivas y aplicables para proporcionar detecciones rápidas, sensibles, específicas, estables, rentables y no invasivas para el diagnóstico temprano del cáncer de pulmón. Por tanto, los biosensores de cáncer consisten en moléculas de biorreconocimiento específicas, como anticuerpos, sondas de ácido nucleico complementarias u otras biomoléculas inmovilizadas en una superficie de transductor. Las moléculas de biorreconocimiento interactúan específicamente con los biomarcadores (objetivos) y el transductor convierte las respuestas biológicas generadas en una señal analítica mensurable. Dependiendo del tipo de respuesta biológica, se utilizan varios transductores en la fabricación de biosensores de cáncer, como transductores electroquímicos, ópticos y de masa. [104]
Los biosensores podrían usarse para la detección de organismos patógenos. [97]
Se han desarrollado biosensores integrados para firmas patógenas, como la del SARS-CoV-2 , que se pueden llevar puestos , como máscaras faciales con pruebas integradas . [105] [106] Ver también: I+D en transporte público COVID-19
Nuevos tipos de chips biosensores podrían permitir métodos novedosos "como sensores de patógenos instalados en drones que monitorean activamente el aire o las aguas residuales". Los aptámeros de unión a proteínas podrían usarse para detectar patógenos de enfermedades infecciosas. [107] Los sistemas de pieles electrónicas (o pieles de robots) con biosensores (o sensores químicos) incorporados e interfaces hombre-máquina pueden permitir la detección de patógenos (así como de varias sustancias peligrosas) tanto en dispositivos portátiles como en dispositivos de detección remota o robóticos. materiales y percepciones táctiles ). [108] [ se necesitan citas adicionales ]
Muchos biosensores ópticos se basan en el fenómeno de las técnicas de resonancia de plasmones superficiales (SPR). [109] [110] Esto utiliza una propiedad del oro y otros materiales (metales); [111] específicamente que una fina capa de oro sobre una superficie de vidrio de alto índice de refracción puede absorber la luz láser, produciendo ondas de electrones (plasmones superficiales) en la superficie del oro. Esto ocurre sólo en un ángulo y longitud de onda específicos de la luz incidente y depende en gran medida de la superficie del oro, de modo que la unión de un analito objetivo a un receptor en la superficie del oro produce una señal mensurable.
Los sensores de resonancia de plasmón superficial funcionan mediante un chip sensor que consiste en un casete de plástico que sostiene una placa de vidrio, uno de cuyos lados está recubierto con una capa microscópica de oro. Este lado hace contacto con el aparato de detección óptica del instrumento. Luego, el lado opuesto se pone en contacto con un sistema de flujo de microfluidos. El contacto con el sistema de flujo crea canales a través de los cuales se pueden pasar los reactivos en solución. Este lado del chip sensor de vidrio se puede modificar de varias maneras para permitir una fácil unión de las moléculas de interés. Normalmente está recubierto de carboximetildextrano o compuesto similar.
El índice de refracción en el lado del flujo de la superficie del chip tiene una influencia directa en el comportamiento de la luz reflejada en el lado del oro. La unión al lado de flujo del chip tiene un efecto sobre el índice de refracción y de esta manera las interacciones biológicas pueden medirse con un alto grado de sensibilidad con algún tipo de energía. El índice de refracción del medio cerca de la superficie cambia cuando las biomoléculas se adhieren a la superficie, y el ángulo SPR varía en función de este cambio.
La luz de una longitud de onda fija se refleja en el lado dorado del chip en el ángulo de reflexión interna total y se detecta dentro del instrumento. El ángulo de la luz incidente varía para hacer coincidir la velocidad de propagación de la onda evanescente con la velocidad de propagación de los polaritones del plasmón superficial. [112] Esto induce a la onda evanescente a penetrar a través de la placa de vidrio y a cierta distancia en el líquido que fluye sobre la superficie.
Otros biosensores ópticos se basan principalmente en cambios en la absorbancia o la fluorescencia de un compuesto indicador apropiado y no necesitan una geometría de reflexión interna total. Por ejemplo, se ha fabricado un prototipo de dispositivo totalmente operativo que detecta caseína en la leche. El dispositivo se basa en detectar cambios en la absorción de una capa de oro. [113] Una herramienta de investigación ampliamente utilizada, el microarray, también puede considerarse un biosensor.
Los biosensores biológicos, también conocidos como sensores optogenéticos , a menudo incorporan una forma genéticamente modificada de una proteína o enzima nativa. La proteína está configurada para detectar un analito específico y la señal resultante se lee mediante un instrumento de detección como un fluorómetro o un luminómetro. Un ejemplo de biosensor desarrollado recientemente es uno para detectar la concentración citosólica del analito AMPc (monofosfato de adenosina cíclico), un segundo mensajero involucrado en la señalización celular desencadenada por ligandos que interactúan con receptores en la membrana celular. [114] Se han creado sistemas similares para estudiar las respuestas celulares a ligandos nativos o xenobióticos (toxinas o inhibidores de moléculas pequeñas). Estos "ensayos" se utilizan habitualmente en el desarrollo del descubrimiento de fármacos por parte de empresas farmacéuticas y biotecnológicas. La mayoría de los ensayos de AMPc en uso actual requieren la lisis de las células antes de la medición del AMPc. Se puede utilizar un biosensor de células vivas para AMPc en células no lisadas con la ventaja adicional de múltiples lecturas para estudiar la cinética de la respuesta del receptor.
Los nanobiosensores utilizan una sonda biorreceptora inmovilizada que es selectiva para las moléculas del analito objetivo. Los nanomateriales son sensores químicos y biológicos exquisitamente sensibles. Los materiales a nanoescala demuestran propiedades únicas. Su gran relación de superficie a volumen puede lograr reacciones rápidas y de bajo costo, utilizando una variedad de diseños. [115]
Se han comercializado otros biosensores de ondas evanescentes utilizando guías de ondas en las que la constante de propagación a través de la guía de ondas cambia mediante la absorción de moléculas en la superficie de la guía de ondas. Un ejemplo de ello, la interferometría de polarización dual utiliza una guía de ondas enterrada como referencia contra la cual se mide el cambio en la constante de propagación. Otras configuraciones, como la Mach-Zehnder, tienen brazos de referencia definidos litográficamente sobre un sustrato. Se pueden lograr niveles más altos de integración utilizando geometrías de resonador donde la frecuencia de resonancia de un resonador de anillo cambia cuando se absorben las moléculas. [116] [117]
Recientemente, se han aplicado conjuntos de muchas moléculas detectoras diferentes en los llamados dispositivos electrónicos de nariz , donde el patrón de respuesta de los detectores se utiliza para tomar huellas dactilares de una sustancia. [118] En el detector de olores Wasp Hound , el elemento mecánico es una cámara de video y el elemento biológico son cinco avispas parásitas que han sido condicionadas para enjambrar en respuesta a la presencia de una sustancia química específica. [119] Las narices electrónicas comerciales actuales, sin embargo, no utilizan elementos biológicos.
El ADN puede ser el analito de un biosensor, detectándose a través de medios específicos, pero también puede usarse como parte de un biosensor o, en teoría, incluso como un biosensor completo.
Existen muchas técnicas para detectar ADN, que suele ser un medio para detectar organismos que tienen ese ADN en particular. También se pueden usar secuencias de ADN como se describe anteriormente. Pero existen enfoques más avanzados, en los que se puede sintetizar ADN para mantener enzimas en un gel biológico estable. [120] Otras aplicaciones son el diseño de aptámeros, secuencias de ADN que tienen una forma específica para unirse a una molécula deseada. Los procesos más innovadores utilizan para ello origami de ADN , creando secuencias que se pliegan en una estructura predecible que resulta útil para la detección. [121] [122]
Los científicos han construido prototipos de sensores para detectar el ADN de los animales a partir del aire aspirado, el "ADNe en el aire". [123]
Las "nanoantenas" hechas de ADN, un nuevo tipo de antena óptica a nanoescala, pueden unirse a proteínas y producir una señal mediante fluorescencia cuando éstas realizan sus funciones biológicas, en particular para distintos cambios conformacionales . [124] [125]
El grafeno es una sustancia bidimensional a base de carbono con propiedades ópticas, eléctricas, mecánicas, térmicas y mecánicas superiores. La capacidad de absorber e inmovilizar una variedad de proteínas, particularmente algunas con estructuras de anillos de carbono, ha demostrado que el grafeno es un excelente candidato como transductor biosensor. Como resultado, en los últimos tiempos se han explorado y desarrollado varios biosensores basados en grafeno. [14] [126] El grafeno se ha empleado como biosensor en varios formatos, especialmente en sensores electroquímicos y transistores de efecto de campo. Entre ellos, los transistores de efecto de campo de grafeno (GFET), especialmente, han mostrado un rendimiento excelente como diagnóstico rápido en el punto de atención (PoC), como se observa a través de un aumento en el número de artículos de investigación que informan sobre diagnósticos de COVID-19 utilizando GFET. Se ha informado que tienen uno de los límites de detección más bajos y, al mismo tiempo, tienen un tiempo de respuesta rápido de unos pocos segundos junto con capacidades de multiplexación. [127] Estas capacidades permiten la detección inmediata de enfermedades, especialmente en casos con síntomas superpuestos que son difíciles de distinguir al principio, lo que permite mejores resultados para los pacientes, especialmente en entornos médicos con recursos limitados.
{{cite web}}: Mantenimiento CS1: copia archivada como título ( enlace )(consultado el 30 de enero de 2013).