El benzo[ c ]fluoreno es un hidrocarburo aromático policíclico (HAP) con actividad mutagénica . Es un componente del alquitrán de hulla , el humo de los cigarrillos y el smog y se cree que es un importante contribuyente a sus propiedades cancerígenas . [1] La mutagenicidad del benzo[ c ]fluoreno se atribuye principalmente a la formación de metabolitos que son reactivos y capaces de formar aductos de ADN . [2] Según el KEGG es un carcinógeno del grupo 3 (no clasificable en cuanto a su carcinogenicidad para los humanos). [3] Otros nombres para el benzo[ c ]fluoreno son 7 H -benzo[ c ]fluoreno, 3,4-benzofluoreno y NSC 89264. [4] [5]
La estructura del benzo[ c ]fluoreno se muestra en el cuadro de información de la derecha. Es una molécula aromática derivada del fluoreno con un anillo de benceno adicional . Este anillo de benceno está unido al carbono 3 y 4 de la molécula derivada del fluoreno. La estructura 3D del benzo[ c ]fluoreno también se muestra en el cuadro de información de la derecha. Es mayoritariamente plana, porque consta de 3 anillos aromáticos. Solo los 2 átomos de hidrógeno en el anillo 5 están orientados en el plano 3D.
El benzo[ c ]fluoreno se produce de forma natural en el alquitrán, pero también se puede sintetizar manualmente en un proceso de cuatro pasos, que se muestra en la imagen siguiente. El producto de partida es 1-indanona (1). Esta se broma en una reacción de sustitución a 3-bromoindanona (2) utilizando el reactivo N -bromosuccinimida . Esta sustancia se deshidrobroma a 2 H -inden-1-ona (3) utilizando el reactivo trietilamina . La benzo[ c ]fluorenona-9 (4) se genera por autocondensación de 2 H -inden-1-ona, cuando se calienta. El paso final es la reducción de este compuesto con hidrato de hidrazina , generando benzo[ c ]fluoreno (5). [7]

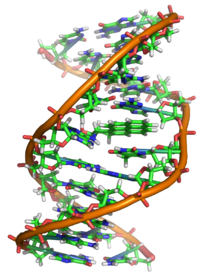
En general, la carcinogénesis por HAP implica la activación por parte de la enzima P-450 de metabolitos de diolepóxido con un anillo de epóxido en la región de la bahía o fiordo. Estos metabolitos de diolepóxido son reactivos y capaces de formar aductos de ADN (véase la imagen adyacente). Si bien el benzo[ c ]fluoreno no tiene una región de bahía o fiordo, sufre una transformación similar con una región pseudobahía que reacciona en su lugar. Se cree que el tipo de citocromo P 450 involucrado es el CYP1A1. [8]
La biotransformación se representa en la imagen siguiente. En primer lugar, el benzo[ c ]fluoreno (1) se transforma en trans-3,4-dihidrodiol (2). Esta sustancia es transformada por el CYP1A1 en los metabolitos altamente cancerígenos anti -diolepóxido (3) y syn -diolepóxido (4). [2]

El benzo[ c ]fluoreno y los HAP en general se absorben principalmente por ingestión, inhalación y contacto dérmico. Además, dependiendo del vehículo (medio de transporte) en el que se encuentren los HAP, los porcentajes de absorción pueden variar. La ingestión de benzo[ c ]fluoreno lo convierte en un tumorígeno pulmonar muy potente [9]. En particular, el benzo[ c ]fluoreno se absorbe mejor en los pulmones. [10]
Una vez absorbido, el benzo[ c ]fluoreno entra en la linfa, circula en la sangre y se metaboliza. La distribución de los HAP depende de su lipofilicidad y probablemente el benzo[ c ]fluoreno puede atravesar fácilmente la membrana celular , debido a esta lipofilicidad. Esto se ha demostrado para sustancias similares como el fluoreno y el fluoranteno , pero aún debe investigarse para el benzo[ c ]fluoreno. [11]
El benzo[ c ]fluoreno se metaboliza principalmente por las enzimas CYP en el hígado . También hay evidencia de que se forma una mayor cantidad de metabolitos en los pulmones, lo que podría explicar por qué el benzo[ c ]fluoreno es un tumorígeno pulmonar tan potente. Es posible que el benzo[ c ]fluoreno pueda tener un mecanismo único (y aún desconocido) de activación o transporte, lo que explica por qué los pulmones son el objetivo. [9] Los pasos iniciales del metabolismo, la biotransformación de fase I , se describen anteriormente.
Se ha demostrado que muchos HAP se conjugan, en la fase II , con glucurónido , sulfato o glutatión . Es necesario realizar más investigaciones sobre este tema en el caso del benzo[ c ]fluoreno. Los conjugados de glucurónido y sulfato de los metabolitos de los HAP se excretan generalmente en la bilis y la orina . Los conjugados de glutatión se metabolizan aún más a ácidos mercaptúricos en el riñón y se excretan en la orina. Los metabolitos hidroxilados de los HAP se excretan en la orina humana tanto como metabolitos hidroxilados libres como metabolitos hidroxilados conjugados con ácido glucurónico y sulfato. [8]
Los metabolitos cancerígenos del benzo[ c ]fluoreno se unen al ADN, lo que implica la apertura del anillo epóxido en el anti- y sin-diolepóxido del benzo[ c ]fluoreno. Los metabolitos del benzo[ c ]fluoreno se unen al ADN de una manera aún desconocida.
Cuando se forma un aducto de ADN en un sitio crítico para la regulación de la diferenciación o el crecimiento celular, puede causar cáncer. Si una aberración en el ADN no es bien reparada por el NER , se producirá una mutación durante la replicación celular. Además, se sabe que las células más afectadas parecen ser aquellas con una replicación rápida, como la médula ósea, la piel y el tejido pulmonar, mientras que los tejidos con una tasa de recambio más lenta, como el hígado, son menos susceptibles. [1] [2]
La exposición al benzo[ c ]fluoreno in vivo conduce a la inducción de tumores principalmente pulmonares donde actúa como un aductor de ADN. Los tumores pulmonares surgen después de la aplicación tópica en ratones con alquitrán de hulla, pero también cuando se ingiere. Además de su participación en los tumores pulmonares, se espera que el benzo[ c ]fluoreno y sus metabolitos estén involucrados en la formación de diferentes tumores . La formación de aductos de ADN en tumores de mama humanos, hepatoma y adenocarcinoma de colon por estos metabolitos se ha demostrado in vitro. Estos aductos y los que se observaron en tumores pulmonares de ratones fueron similares, lo que refuerza la hipótesis de que las células humanas son capaces de formar los metabolitos mutagénicos. [9] [12]
El benzo[ c ]fluoreno pertenece a un grupo de compuestos denominados hidrocarburos aromáticos policíclicos (HAP). Los HAP y sus derivados son omnipresentes en el medio ambiente y se producen en varios procesos industriales y de combustión . [13]
Los trabajadores de industrias o comercios que utilizan o producen carbón , petróleo crudo o productos derivados del carbón tienen el mayor riesgo de exposición a HAP. En general, los HAP se forman durante estos procesos industriales por combustión incompleta o pirólisis de materia orgánica. Cuanto más alta sea la temperatura, más HAP se forman. [14]
Algunos de estos HAP, como el benzo[ c ]fluoreno, son carcinógenos y mutágenos y actúan como posibles disruptores endocrinos . Para estimar los efectos sobre la salud que surgen de la exposición a los HAP y al benzo[ c ]fluoreno es necesario determinar la concentración de estos compuestos en la atmósfera. Esto se realizó en un estudio de Morisaki et al. 2016. Compararon las concentraciones de diferentes HAP, incluido el benzo[ c ]fluoreno, en Beijing y Kanazawa en invierno y verano.
Los investigadores corrigieron la mutagenicidad relativa de los compuestos en comparación con el benzo[ a ]pireno . [15] Los resultados de esto se presentan como BaPeq, que es igual a la concentración del compuesto, multiplicada por la potencia del compuesto en comparación con el benzo[ a ]pireno (RPF). Aunque las concentraciones medidas de benzo[ c ]fluoreno son bastante bajas, cuando se corrige la mutagenicidad, el benzo[ c ]fluoreno es el HAP más importante de los que se midieron en términos de posibles riesgos para la salud. [13]
En un estudio, se realizó la prueba de Ames sobre el benzo[ c ]fluoreno. Se utilizaron dos cepas diferentes, TA100 y TA98. Un grupo de cada cepa tenía una fracción de hígado de rata y el otro grupo no. La diferencia entre la cepa TA100 y la TA98 es que la cepa TA98 tiene una mutación por cambio de marco de lectura y la TA100 tiene una mutación por sustitución de bases. Cuando se aumenta la cantidad de benzo[ c ]fluoreno en la cepa de levadura TA 100, la cantidad de revertientes por placa no aumenta. Solo en la placa de la cepa TA98, que contenía una fracción de hígado de rata, una dosis más alta de benzo[ c ]fluoreno parece corresponderse con una mayor cantidad de revertientes. Esto indica que el benzo[ c ]fluoreno es metabolizado por enzimas en el hígado de la rata en compuestos mutagénicos más potentes. Estos compuestos solo afectaron a la cepa TA98. Esto indica que los aductos formados por metabolitos de benzo[ c ]fluoreno causan mutaciones por desplazamiento del marco de lectura , y no mutaciones puntuales . [16]
En un estudio realizado con animales, los ratones alimentados con alquitrán de hulla desarrollaron tumores pulmonares. Se analizaron los aductos de ADN de estos ratones y se pudo rastrear su origen hasta el benzo[ c ]fluoreno. Este estudio y otro similar sugieren una contribución del benzo[ c ]fluoreno a la potencia cancerígena del alquitrán de hulla cuando se administra por vía oral. [1] [18]
Otro estudio descubrió que el benzo[ c ]fluoreno también es cancerígeno en ratones cuando se aplica tópicamente , provocando cáncer de pulmón y de piel. A partir de los resultados de este estudio se ha elaborado una curva dosis-respuesta , véase la imagen de arriba.
Esta figura muestra el nivel de aducto de ADN después de aplicar una determinada dosis de benzo[ c ]fluoreno en la piel de ratones. Este nivel es similar en los pulmones y en la piel, lo que implica que el benzo[ c ]fluoreno es un mutágeno sistémico . [17]
Los efectos de la exposición al benzo[ c ]fluoreno también se investigaron en ratas. En uno de estos estudios se estableció que el hígado era el principal lugar de disposición del benzo[ c ]fluoreno después de una dosis oral única, independientemente del tamaño de la dosis. Se descubrió que entre el 55 y el 69 % del benzo[ c ]fluoreno marcado se excretaba a través de las heces, mientras que entre el 8 y el 10 % se eliminaba a través de la orina. Si bien el benzo[ c ]fluoreno encontrado en las heces no se biotransformaba, las muestras de orina mostraban principalmente metabolitos polares de benzo[ c ]fluoreno. [19]
{{cite journal}}: Requiere citar revista |journal=( ayuda ){{cite journal}}: Requiere citar revista |journal=( ayuda )