La acidemia propiónica , también conocida como aciduria propiónica o deficiencia de propionil-CoA carboxilasa ( deficiencia de PCC ), [1] es un trastorno metabólico autosómico recesivo poco común , clasificado como una acidemia orgánica de cadena ramificada . [2] [3]
El trastorno se presenta en el período neonatal temprano con mala alimentación, vómitos, letargo y falta de tono muscular. [4] Sin tratamiento, la muerte puede ocurrir rápidamente, debido a hiperamonemia secundaria , infección, miocardiopatía o daño cerebral. [5]
La acidemia propiónica puede variar en gravedad. [6] La acidemia propiónica grave produce síntomas que ya se observan en los recién nacidos. [7] Los síntomas incluyen mala alimentación, vómitos , deshidratación , acidosis , bajo tono muscular ( hipotonía ), convulsiones y letargo . Los efectos de la acidemia propiónica rápidamente se vuelven potencialmente mortales.
Las complicaciones a largo plazo pueden incluir discapacidad intelectual, autismo, [8] enfermedad renal crónica, [9] miocardiopatía e intervalo QTc prolongado. [10]
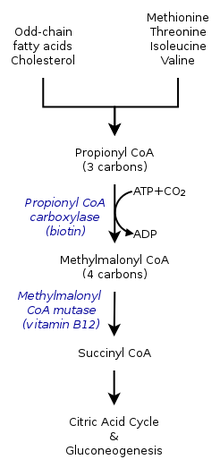

En individuos sanos, la enzima propionil-CoA carboxilasa convierte el propionil-CoA en metilmalonil-CoA . Este es uno de los muchos pasos en el proceso de convertir ciertos aminoácidos y grasas en energía. Las personas con acidemia propiónica no pueden realizar esta conversión porque la enzima propionil-CoA carboxilasa no es funcional. Los aminoácidos esenciales valina , metionina , isoleucina y treonina no pueden convertirse y esto conduce a una acumulación de propionil-CoA. En lugar de convertirse en metilmalonil-CoA, el propionil-CoA se convierte en ácido propiónico , que se acumula en el torrente sanguíneo. Esto a su vez provoca una acumulación de ácidos y toxinas peligrosas, que pueden causar daños a los órganos. [ cita requerida ]
En muchos casos, la acidemia propiónica puede dañar el cerebro, el corazón, los riñones y el hígado, provocar convulsiones y retrasos en el desarrollo normal, como caminar o hablar. Se sabe que la acumulación de ácido propiónico induce respuestas diferenciales en diferentes órganos. El corazón y el hígado son objetivos específicos de la complicación. Es posible que el paciente deba ser hospitalizado para prevenir la descomposición de las proteínas dentro del cuerpo. Las necesidades dietéticas deben controlarse de cerca. [ cita requerida ]
Las mutaciones en ambas copias de los genes PCCA o PCCB causan acidemia propiónica. [11] Estos genes contienen instrucciones para formar subunidades alfa y beta de PCC, la enzima llamada propionil-CoA carboxilasa.
La PCC es necesaria para la descomposición normal de los aminoácidos esenciales valina, isoleucina, treonina y metionina, así como de ciertos ácidos grasos de cadena impar. Las mutaciones en los genes PCCA o PCCB alteran la función de la enzima, impidiendo que estos ácidos se metabolicen. Como resultado, el propionil-CoA , el ácido propiónico, las cetonas , el amoníaco y otros compuestos tóxicos se acumulan en la sangre , lo que causa los signos y síntomas de la acidemia propiónica . La hiperamonemia se desarrolla debido a los efectos inhibidores del propionil-CoA sobre la N-acetilglutamato sintasa , lo que indirectamente resulta en la ralentización del ciclo de la urea . [12]
Se encontraron niveles elevados de metabolitos de ácido propiónico (por ejemplo, 3-hidroxipropionato, 2-metilcitrato, tiglilglicina, propionilglicina) en la sangre y la orina junto con una actividad normal de biotinidasa y niveles normales de ácido metilmalónico. [10]
Los pacientes con acidemia propiónica deben comenzar lo antes posible con una dieta baja en proteínas. Además de una mezcla de proteínas que esté libre de metionina, treonina, valina e isoleucina, el paciente también debe recibir tratamiento con L -carnitina y antibióticos 10 días al mes para eliminar la flora propiogénica intestinal. El paciente debe tener protocolos dietéticos preparados con una “dieta de día de bienestar” con bajo contenido de proteínas, una “dieta de emergencia a medias” que contenga la mitad de los requerimientos de proteínas y una “dieta de emergencia” sin contenido de proteínas. Estos pacientes corren el riesgo de sufrir hiperamonemia grave durante las infecciones que pueden conducir a estados comatosos. [13]
El trasplante de hígado está ganando un papel en el tratamiento de estos pacientes, con pequeñas series que muestran una mejor calidad de vida.
La acidemia propiónica se hereda con un patrón autosómico recesivo y se presenta en aproximadamente 1 de cada 35 000 [11] nacidos vivos en los Estados Unidos . La afección parece ser más común en Arabia Saudita , [14] con una frecuencia de aproximadamente 1 de cada 3000. [11] La afección también parece ser común en poblaciones amish , menonitas y otras con mayor frecuencia de consanguinidad. [15]
En 1957, nació un niño con un desarrollo mental deficiente, repetidos ataques de acidosis y altos niveles de cetonas y glicina en la sangre. Tras realizarle pruebas dietéticas, el Dr. Barton Childs descubrió que sus síntomas empeoraban cuando se le administraban los aminoácidos leucina, isoleucina, valina, metionina y treonina. En 1961, el equipo médico del Hospital Johns Hopkins en Baltimore , Maryland, publicó el caso y denominó al trastorno hiperglicinemia cetótica . En 1969, utilizando datos de la hermana del paciente original, los científicos establecieron que la acidemia propiónica era un trastorno recesivo y que la acidemia propiónica y la acidemia metilmalónica son causadas por deficiencias en la misma vía enzimática. [16]