Una ADN polimerasa es miembro de una familia de enzimas que catalizan la síntesis de moléculas de ADN a partir de nucleósidos trifosfatos , los precursores moleculares del ADN. Estas enzimas son esenciales para la replicación del ADN y normalmente trabajan en grupos para crear dos dúplex de ADN idénticos a partir de un único dúplex de ADN original. Durante este proceso, la ADN polimerasa "lee" las cadenas de ADN existentes para crear dos nuevas cadenas que coincidan con las existentes. [1] [2] [3] [4] [5] [6] Estas enzimas catalizan la reacción química
La ADN polimerasa agrega nucleótidos a los tres extremos principales (3') de una cadena de ADN, un nucleótido a la vez. Cada vez que una célula se divide , se requieren ADN polimerasas para duplicar el ADN de la célula, de modo que se pueda pasar una copia de la molécula de ADN original a cada célula hija. De esta forma, la información genética se transmite de generación en generación.
Antes de que pueda tener lugar la replicación, una enzima llamada helicasa desenrolla la molécula de ADN de su forma densamente tejida, rompiendo en el proceso los enlaces de hidrógeno entre las bases de nucleótidos . Esto abre o "descomprime" el ADN de doble hebra para dar dos hebras simples de ADN que pueden usarse como plantillas para la replicación en la reacción anterior.
En 1956, Arthur Kornberg y sus colegas descubrieron la ADN polimerasa I (Pol I), en Escherichia coli . Describieron el proceso de replicación del ADN mediante el cual la ADN polimerasa copia la secuencia de bases de una cadena de ADN molde. Kornberg recibió posteriormente el Premio Nobel de Fisiología o Medicina en 1959 por este trabajo. [7] La ADN polimerasa II fue descubierta por Thomas Kornberg (el hijo de Arthur Kornberg ) y Malcolm E. Gefter en 1970 mientras aclaraban aún más el papel de Pol I en la replicación del ADN de E. coli . [8] Se han encontrado tres ADN polimerasas más en E. coli , incluida la ADN polimerasa III (descubierta en la década de 1970) y las ADN polimerasas IV y V (descubiertas en 1999). [9] A partir de 1983, las ADN polimerasas se utilizaron en la reacción en cadena de la polimerasa (PCR), y desde 1988 se utilizaron en su lugar ADN polimerasas termoestables , ya que no es necesario agregarlas en cada ciclo de una PCR.

La función principal de la ADN polimerasa es sintetizar ADN a partir de desoxirribonucleótidos , los componentes básicos del ADN. Las copias de ADN se crean mediante el emparejamiento de nucleótidos con bases presentes en cada hebra de la molécula de ADN original. Este emparejamiento se produce siempre en combinaciones específicas, con citosina junto con guanina , y timina junto con adenina , formando dos pares separados, respectivamente. Por el contrario, las ARN polimerasas sintetizan ARN a partir de ribonucleótidos de ARN o ADN. [ cita necesaria ]
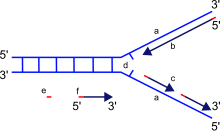
Al sintetizar ADN nuevo, la ADN polimerasa puede agregar nucleótidos libres sólo al extremo 3' de la cadena recién formada. Esto da como resultado el alargamiento de la hebra recién formada en una dirección 5'-3'. [ cita necesaria ]
Es importante señalar que la direccionalidad de la cadena recién formada (la cadena hija) es opuesta a la dirección en la que la ADN polimerasa se mueve a lo largo de la cadena plantilla. Dado que la ADN polimerasa requiere un grupo OH 3' libre para iniciar la síntesis, puede sintetizar en una sola dirección extendiendo el extremo 3' de la cadena de nucleótidos preexistente. Por lo tanto, la ADN polimerasa se mueve a lo largo de la cadena plantilla en una dirección 3'-5', y la cadena hija se forma en una dirección 5'-3'. Esta diferencia permite que el ADN de doble hebra resultante formado esté compuesto por dos hebras de ADN que son antiparalelas entre sí. [ cita necesaria ]
La función de la ADN polimerasa no es del todo perfecta: la enzima comete aproximadamente un error por cada mil millones de pares de bases copiadas. La corrección de errores es una propiedad de algunas, pero no de todas, las ADN polimerasas. Este proceso corrige errores en el ADN recién sintetizado. Cuando se reconoce un par de bases incorrecto, la ADN polimerasa retrocede un par de bases de ADN. La actividad exonucleasa 3'-5' de la enzima permite eliminar el par de bases incorrecto (esta actividad se conoce como corrección ). Después de la escisión de la base, la polimerasa puede reinsertar la base correcta y la replicación puede continuar hacia adelante. Esto preserva la integridad de la cadena de ADN original que pasa a las células hijas.
La fidelidad es muy importante en la replicación del ADN. Los desajustes en el emparejamiento de bases del ADN pueden dar como resultado proteínas disfuncionales y provocar cáncer. Muchas ADN polimerasas contienen un dominio exonucleasa, que actúa detectando desajustes de pares de bases y además actúa en la eliminación del nucleótido incorrecto para ser reemplazado por el correcto. [10] La forma y las interacciones que acomodan el par de bases de Watson y Crick son las que contribuyen principalmente a la detección o error. Los enlaces de hidrógeno juegan un papel clave en la unión e interacción de pares de bases. Se dice que la pérdida de una interacción, que se produce en un desajuste, desencadena un cambio en el equilibrio, para la unión del cebador-plantilla, de la polimerasa, al dominio exonucleasa. Además, la incorporación de un nucleótido incorrecto provoca un retraso en la polimerización del ADN. Este retraso da tiempo para que el ADN cambie del sitio de la polimerasa al sitio de la exonucleasa. Se producen diferentes cambios conformacionales y pérdida de interacción en diferentes desajustes. En un desajuste purina:pirimidina hay un desplazamiento de la pirimidina hacia el surco mayor y de la purina hacia el surco menor. En relación con la forma de la bolsa de unión de la ADN polimerasa, se producen choques estéricos entre la purina y los residuos en el surco menor, y la pirimidina pierde importantes interacciones electrostáticas y de van der Waals . [11] Los desajustes de pirimidina:pirimidina y purina:purina presentan cambios menos notables ya que las bases se desplazan hacia el surco principal y se experimenta menos impedimento estérico. Sin embargo, aunque los diferentes desajustes dan como resultado diferentes propiedades estéricas, la ADN polimerasa aún es capaz de detectarlos y diferenciarlos de manera uniforme y mantener la fidelidad en la replicación del ADN. [12] La polimerización del ADN también es fundamental para muchos procesos de mutagénesis y se emplea ampliamente en biotecnologías.
Las ADN polimerasas conocidas tienen una estructura altamente conservada, lo que significa que sus subunidades catalíticas generales varían muy poco de una especie a otra, independientemente de sus estructuras de dominio. Las estructuras conservadas suelen indicar funciones importantes e insustituibles de la célula, cuyo mantenimiento proporciona ventajas evolutivas. La forma se puede describir como una mano derecha con dominios de pulgar, dedos y palma. El dominio de la palma parece funcionar catalizando la transferencia de grupos fosforilo en la reacción de transferencia de fosforilo. El ADN se une a la palma cuando la enzima está activa. Se cree que esta reacción está catalizada por un mecanismo de dos iones metálicos. El dominio del dedo funciona para unir los nucleósidos trifosfato con la base plantilla. El dominio del pulgar juega un papel potencial en la procesividad, translocación y posicionamiento del ADN. [13]
La rápida catálisis de la ADN polimerasa debido a su naturaleza procesiva. La procesividad es una característica de las enzimas que funcionan sobre sustratos poliméricos. En el caso de la ADN polimerasa, el grado de procesividad se refiere al número promedio de nucleótidos agregados cada vez que la enzima se une a una plantilla. La ADN polimerasa promedio requiere aproximadamente un segundo para localizar y unir una unión cebador/molde. Una vez unida, una ADN polimerasa no procesiva agrega nucleótidos a una velocidad de un nucleótido por segundo. [14] : 207–208 Las ADN polimerasas procesivas, sin embargo, agregan múltiples nucleótidos por segundo, lo que aumenta drásticamente la tasa de síntesis de ADN. El grado de procesividad es directamente proporcional a la tasa de síntesis de ADN. La tasa de síntesis de ADN en una célula viva se determinó primero como la tasa de elongación del ADN del fago T4 en E. coli infectada con fagos . Durante el período de aumento exponencial del ADN a 37 °C, la velocidad fue de 749 nucleótidos por segundo. [15]
La capacidad de la ADN polimerasa para deslizarse a lo largo de la plantilla de ADN permite una mayor procesividad. Hay un aumento dramático en la procesividad en la bifurcación de replicación . Este aumento se ve facilitado por la asociación de la ADN polimerasa con proteínas conocidas como pinza deslizante del ADN . Las pinzas son múltiples subunidades proteicas asociadas en forma de anillo. Utilizando la hidrólisis de ATP, una clase de proteínas conocidas como proteínas de carga de abrazaderas deslizantes abren la estructura del anillo de las abrazaderas deslizantes de ADN, lo que permite la unión y la liberación de la cadena de ADN. La interacción proteína-proteína con la abrazadera evita que la ADN polimerasa se difunda desde la plantilla de ADN, asegurando así que la enzima se una a la misma unión cebador/plantilla y continúe la replicación. [14] : 207–208 La ADN polimerasa cambia su conformación, aumentando la afinidad por la abrazadera cuando se asocia con ella y disminuyendo la afinidad cuando completa la replicación de un tramo de ADN para permitir la liberación de la abrazadera. [ cita necesaria ]
La procesividad de la ADN polimerasa se ha estudiado con experimentos in vitro de una sola molécula (a saber, pinzas ópticas y pinzas magnéticas ) que han revelado las sinergias entre las ADN polimerasas y otras moléculas del replisoma ( helicasas y SSB ) y con la horquilla de replicación del ADN. [16] Estos resultados han llevado al desarrollo de modelos cinéticos sinérgicos para la replicación del ADN que describen el aumento resultante de la procesividad de la ADN polimerasa. [dieciséis]
Según la homología de secuencia, las ADN polimerasas se pueden subdividir en siete familias diferentes: A, B, C, D, X, Y y RT.
Algunos virus también codifican ADN polimerasas especiales, como la ADN polimerasa del virus de la hepatitis B. Estos pueden replicar selectivamente el ADN viral a través de una variedad de mecanismos. Los retrovirus codifican una ADN polimerasa inusual llamada transcriptasa inversa , que es una ADN polimerasa dependiente de ARN (RdDp). Polimeriza el ADN a partir de una plantilla de ARN .
Las polimerasas procarióticas existen en dos formas: polimerasa central y holoenzima. La polimerasa central sintetiza ADN a partir de la plantilla de ADN, pero no puede iniciar la síntesis por sí sola ni con precisión. La holoenzima inicia con precisión la síntesis.
Las polimerasas procarióticas de la familia A incluyen la enzima ADN polimerasa I (Pol I), que está codificada por el gen polA y es ubicua entre los procariotas . Esta polimerasa reparadora participa en la reparación por escisión con actividad exonucleasa 3'-5' y 5'-3' y en el procesamiento de fragmentos de Okazaki generados durante la síntesis de la cadena retrasada. [21] Pol I es la polimerasa más abundante y representa >95% de la actividad polimerasa en E. coli ; sin embargo, se han encontrado células que carecen de Pol I, lo que sugiere que la actividad de Pol I puede ser reemplazada por las otras cuatro polimerasas. Pol I agrega entre 15 y 20 nucleótidos por segundo, lo que muestra una procesividad deficiente. En cambio, Pol I comienza a agregar nucleótidos en la unión del cebador de ARN: plantilla conocida como el origen de replicación (ori). Aproximadamente 400 pb aguas abajo del origen, la holoenzima Pol III se ensambla y asume la replicación a una velocidad y naturaleza altamente procesivas. [22]
La Taq polimerasa es una enzima termoestable de esta familia que carece de capacidad de corrección. [23]
La ADN polimerasa II es una polimerasa de la familia B codificada por el gen polB. Pol II tiene actividad exonucleasa 3'-5' y participa en la reparación del ADN , el reinicio de la replicación para evitar las lesiones y su presencia celular puede saltar de ~30-50 copias por célula a ~200-300 durante la inducción de SOS. También se cree que Pol II es un respaldo de Pol III, ya que puede interactuar con proteínas holoenzimáticas y asumir un alto nivel de procesividad. Se cree que la función principal de Pol II es la capacidad de dirigir la actividad de la polimerasa en la bifurcación de replicación y ayudar a detener los desajustes terminales de Pol III. [24]
La ADN polimerasa Pfu es una enzima termoestable de esta familia que se encuentra en la arqueona hipertermófila Pyrococcus furiosus . [25] La clasificación detallada divide la familia B en arqueas en B1, B2, B3, en la que B2 es un grupo de pseudoenzimas . Pfu pertenece a la familia B3. Otros PolB encontrados en arqueas son parte de los "Casposones",transposones dependientes de Cas1 . [26] Algunos virus (incluida la ADN polimerasa Φ29 ) y plásmidos mitocondriales también portan polB. [27]
La holoenzima ADN polimerasa III es la principal enzima implicada en la replicación del ADN en E. coli y pertenece a la familia de polimerasas C. Consta de tres conjuntos: el núcleo pol III, el factor de procesividad de la abrazadera deslizante beta y el complejo de carga de la abrazadera. El núcleo consta de tres subunidades: α, el centro de actividad de la polimerasa, ɛ, corrector exonucleolítico y θ, que puede actuar como estabilizador de ɛ. El factor de procesividad de la abrazadera deslizante beta también está presente por duplicado, uno para cada núcleo, para crear una abrazadera que encierra el ADN y permite una alta procesividad. [28] El tercer conjunto es un complejo de cargador de abrazadera de siete subunidades (τ2γδδ ′ χψ).
El antiguo "modelo de trombón" del libro de texto representa un complejo de elongación con dos equivalentes de la enzima central en cada horquilla de replicación (RF), uno para cada hebra, la retrasada y la delantera. [24] Sin embargo, evidencia reciente de estudios de una sola molécula indica un promedio de tres equivalentes estequiométricos de enzima central en cada RF tanto para Pol III como para su contraparte en B. subtilis, PolC. [29] La microscopía fluorescente dentro de las células ha revelado que la síntesis de la cadena principal puede no ser completamente continua, y Pol III* (es decir, las subunidades α, ε, τ, δ y χ de la holoenzima sin la abrazadera deslizante ß2) tiene una alta frecuencia de disociación de los RF activos. [30] En estos estudios, la tasa de recambio de la horquilla de replicación fue de aproximadamente 10 s para Pol III*, 47 s para la abrazadera deslizante ß2 y 15 m para la helicasa DnaB. Esto sugiere que la helicasa DnaB puede permanecer asociada de manera estable en los RF y servir como punto de nucleación para la holoenzima competente. Los estudios in vitro de una sola molécula han demostrado que Pol III* tiene una alta tasa de recambio de RF cuando está en exceso, pero permanece asociado de manera estable con las horquillas de replicación cuando la concentración es limitante. [30] Otro estudio de una sola molécula demostró que la actividad de la helicasa DnaB y el alargamiento de la cadena pueden proceder con una cinética estocástica desacoplada. [30]
En E. coli , la ADN polimerasa IV (Pol IV) es una ADN polimerasa propensa a errores involucrada en la mutagénesis no dirigida. [31] Pol IV es una polimerasa de la familia Y expresada por el gen dinB que se activa mediante la inducción SOS causada por polimerasas estancadas en la bifurcación de replicación. Durante la inducción SOS, la producción de Pol IV aumenta diez veces y una de las funciones durante este tiempo es interferir con la procesividad de la holoenzima Pol III. Esto crea un punto de control, detiene la replicación y da tiempo para reparar las lesiones del ADN a través de la vía de reparación adecuada. [32] Otra función de Pol IV es realizar la síntesis de translesión en la bifurcación de replicación detenida, como, por ejemplo, evitando los aductos de N2-desoxiguanina a un ritmo más rápido que atravesar el ADN no dañado. Las células que carecen del gen dinB tienen una mayor tasa de mutagénesis causada por agentes que dañan el ADN. [33]
La ADN polimerasa V (Pol V) es una ADN polimerasa de la familia Y que participa en la respuesta SOS y en los mecanismos de reparación del ADN de síntesis de translesiones . [34] La transcripción de Pol V a través de los genes umuDC está altamente regulada para producir solo Pol V cuando el ADN dañado está presente en la célula generando una respuesta SOS. Las polimerasas estancadas hacen que RecA se una al ssDNA, lo que hace que la proteína LexA se autodigiera. Luego, LexA pierde su capacidad de reprimir la transcripción del operón umuDC. La misma nucleoproteína RecA-ssDNA modifica postraduccionalmente la proteína UmuD en proteína UmuD'. UmuD y UmuD' forman un heterodímero que interactúa con UmuC, lo que a su vez activa la actividad catalítica de la polimerasa de umuC en el ADN dañado. [35] En E. coli , se ha propuesto un modelo de "cinturón de herramientas" de polimerasa para cambiar pol III con pol IV en una bifurcación de replicación detenida, donde ambas polimerasas se unen simultáneamente a la abrazadera β. [36] Sin embargo, aún no se ha demostrado en E. coli la participación de más de una polimerasa TLS trabajando en sucesión para evitar una lesión . Además, Pol IV puede catalizar tanto la inserción como la extensión con alta eficiencia, mientras que pol V se considera la principal polimerasa SOS TLS. Un ejemplo es la derivación del entrecruzamiento de guanina timina intrahebra donde se demostró, basándose en la diferencia en las firmas mutacionales de las dos polimerasas, que pol IV y pol V compiten por TLS del entrecruzamiento intrahebra. [36]

En 1998, se descubrió la familia D de la ADN polimerasa en Pyrococcus furiosus y Methanococcus jannaschii . [38] El complejo PolD es un heterodímero de dos cadenas, cada una codificada por DP1 (corrección pequeña) y DP2 (catalizador grande). A diferencia de otras ADN polimerasas, la estructura y el mecanismo del núcleo catalítico de DP2 se asemejan a los de las ARN polimerasas de múltiples subunidades . La interfaz DP1-DP2 se parece a la del dedo de zinc de la polimerasa eucariota de clase B y su subunidad pequeña. [18] DP1, una exonucleasa similar a Mre11 , [39] es probablemente el precursor de la subunidad pequeña de Pol α y ε , lo que proporciona capacidades de corrección que ahora se pierden en los eucariotas. [26] Su dominio HSH N-terminal es similar a las proteínas AAA , especialmente a la subunidad δ de Pol III y a RuvB , en estructura. [40] DP2 tiene un dominio KH de Clase II . [18] Pyrococcus abyssi polD es más estable al calor y más preciso que la polimerasa Taq , pero aún no se ha comercializado. [41] Se ha propuesto que la ADN polimerasa de la familia D fue la primera en evolucionar en organismos celulares y que la polimerasa replicativa del Último Ancestro Celular Universal (LUCA) pertenecía a la familia D. [42]
Las polimerasas de la familia X contienen la conocida polimerasa eucariota pol β (beta) , así como otras polimerasas eucariotas como Pol σ (sigma), Pol λ (lambda) , Pol μ (mu) y desoxinucleotidil transferasa terminal (TdT) . Las polimerasas de la familia X se encuentran principalmente en vertebrados y algunas en plantas y hongos. Estas polimerasas tienen regiones altamente conservadas que incluyen dos motivos hélice-horquilla-hélice que son imperativos en las interacciones ADN-polimerasa. Un motivo está ubicado en el dominio de 8 kDa que interactúa con el ADN aguas abajo y un motivo está ubicado en el dominio del pulgar que interactúa con la cadena del cebador. Pol β, codificado por el gen POLB, es necesario para la reparación por escisión de bases de parche corto , una vía de reparación del ADN que es esencial para reparar bases alquiladas u oxidadas, así como sitios abásicos . Pol λ y Pol μ, codificados por los genes POLL y POLM respectivamente, participan en la unión de extremos no homólogos , un mecanismo para volver a unir roturas de doble cadena de ADN debido al peróxido de hidrógeno y la radiación ionizante, respectivamente. La TdT se expresa sólo en tejido linfoide y agrega "n nucleótidos" a las roturas de doble cadena formadas durante la recombinación de V(D)J para promover la diversidad inmunológica. [43]
Pol α (alfa) , Pol δ (delta) y Pol ε (épsilon) son miembros de la familia B de polimerasas y son las principales polimerasas involucradas en la replicación del ADN nuclear. El complejo Pol α (complejo pol α-ADN primasa) consta de cuatro subunidades: la subunidad catalítica POLA1 , la subunidad reguladora POLA2 y las subunidades de primasa pequeña y grande PRIM1 y PRIM2 respectivamente. Una vez que la primasa ha creado el cebador de ARN, Pol α comienza la replicación alargando el cebador con ~20 nucleótidos. [44] Debido a su alta procesividad, Pol δ se hace cargo de la síntesis de las cadenas delantera y trasera de Pol α. [14] : 218–219 Pol δ se expresa mediante los genes POLD1 , creando la subunidad catalítica POLD2 , POLD3 y POLD4 creando las otras subunidades que interactúan con el antígeno nuclear de células proliferantes (PCNA), que es una abrazadera de ADN que permite que Pol δ poseer procesividad. [45] Pol ε está codificado por el gen POLE1 , la subunidad catalítica, POLE2 y POLE3 . Se ha informado que la función de Pol ε es extender la cadena principal durante la replicación, [46] [47] mientras que Pol δ replica principalmente la cadena retrasada; sin embargo, evidencia reciente sugirió que Pol δ también podría desempeñar un papel en la replicación de la cadena principal de ADN. [48] La región "reliquia de polimerasa" del extremo C de Pol ε, a pesar de ser innecesaria para la actividad de la polimerasa, [49] se cree que es esencial para la vitalidad celular. Se cree que la región C-terminal proporciona un punto de control antes de entrar en anafase, proporciona estabilidad a la holoenzima y agrega proteínas a la holoenzima necesarias para el inicio de la replicación. [50] Pol ε tiene un dominio "palma" más grande que proporciona una alta procesividad independientemente de PCNA. [49]
En comparación con otras polimerasas de la familia B, la familia de exonucleasas DEDD responsable de la corrección de pruebas está inactivada en Pol α. [26] Pol ε es único porque tiene dos dominios de dedos de zinc y una copia inactiva de otra polimerasa de la familia B en su C-terminal. La presencia de este dedo de zinc tiene implicaciones en los orígenes de Eukaryota, que en este caso se ubica en el grupo Asgard con la polimerasa arqueal B3. [51]
Pol η (eta) , Pol ι (iota) y Pol κ (kappa), son ADN polimerasas de la familia Y implicadas en la reparación del ADN mediante síntesis de traducción y codificadas por los genes POLH, POLI y POLK respectivamente. Los miembros de la Familia Y tienen cinco motivos comunes para ayudar a unir el sustrato y el extremo del cebador y todos incluyen los dominios típicos del pulgar, la palma y los dedos de la mano derecha con dominios agregados como el dedo meñique (LF), el dominio asociado a la polimerasa (PAD) o muñeca. Sin embargo, el sitio activo difiere entre los miembros de la familia debido a las diferentes lesiones que se reparan. Las polimerasas de la familia Y son polimerasas de baja fidelidad, pero se ha demostrado que hacen más bien que mal, ya que las mutaciones que afectan a la polimerasa pueden causar diversas enfermedades, como cáncer de piel y variante de xeroderma pigmentoso (XPS). La importancia de estas polimerasas se evidencia por el hecho de que el gen que codifica la ADN polimerasa η se denomina XPV, porque la pérdida de este gen da como resultado la enfermedad Xeroderma Pigmentosum Variant. Pol η es particularmente importante para permitir la síntesis precisa por translesión del daño del ADN resultante de la radiación ultravioleta . La funcionalidad de Pol κ no se comprende completamente, pero los investigadores han encontrado dos funciones probables. Se cree que Pol κ actúa como extensor o insertador de una base específica en determinadas lesiones del ADN. Las tres polimerasas de síntesis de translesiones, junto con Rev1, se reclutan en las lesiones dañadas mediante ADN polimerasas replicativas estancadas. Hay dos vías de reparación de daños que llevan a los investigadores a concluir que la vía elegida depende de qué cadena contiene el daño, la cadena principal o la retrasada. [52]
Pol ζ, otra polimerasa de la familia B, está formada por dos subunidades Rev3 , la subunidad catalítica, y Rev7 ( MAD2L2 ), que aumenta la función catalítica de la polimerasa y participa en la síntesis de translesiones. Pol ζ carece de actividad exonucleasa de 3' a 5' y es único porque puede extender cebadores con desajustes terminales. Rev1 tiene tres regiones de interés en el dominio BRCT , el dominio de unión a ubiquitina y el dominio C-terminal y tiene capacidad de dCMP transferasa, que agrega desoxicitidina a las lesiones opuestas que detendrían las polimerasas replicativas Pol δ y Pol ε. Estas polimerasas estancadas activan complejos de ubiquitina que a su vez disocian las polimerasas de replicación y reclutan a Pol ζ y Rev1. Juntos, Pol ζ y Rev1 agregan desoxicitidina y Pol ζ se extiende más allá de la lesión. A través de un proceso aún indeterminado, Pol ζ se disocia y las polimerasas de replicación se reasocian y continúan la replicación. Pol ζ y Rev1 no son necesarios para la replicación, pero la pérdida del gen REV3 en la levadura en ciernes puede causar una mayor sensibilidad a los agentes que dañan el ADN debido al colapso de las horquillas de replicación donde las polimerasas de replicación se han estancado. [53]
La telomerasa es una ribonucleoproteína que funciona para replicar los extremos de los cromosomas lineales, ya que la ADN polimerasa normal no puede replicar los extremos o telómeros . El saliente 3' monocatenario del cromosoma bicatenario con la secuencia 5'-TTAGGG-3' recluta telomerasa. La telomerasa actúa como otras ADN polimerasas al extender el extremo 3', pero, a diferencia de otras ADN polimerasas, la telomerasa no requiere una plantilla. La subunidad TERT, un ejemplo de transcriptasa inversa , utiliza la subunidad de ARN para formar la unión cebador-plantilla que permite que la telomerasa extienda el extremo 3' de los extremos de los cromosomas. Se cree que la disminución gradual del tamaño de los telómeros como resultado de muchas replicaciones a lo largo de la vida está asociada con los efectos del envejecimiento. [14] : 248–249
Pol γ (gamma), Pol θ (theta) y Pol ν (nu) son polimerasas de la familia A. Durante mucho tiempo se pensó que Pol γ, codificada por el gen POLG , era la única polimerasa mitocondrial . Sin embargo, investigaciones recientes muestran que al menos Pol β (beta) , una polimerasa de la familia X, también está presente en las mitocondrias. [54] [55] Cualquier mutación que conduzca a Pol γ limitado o no funcional tiene un efecto significativo en el ADNmt y es la causa más común de trastornos mitocondriales hereditarios autosómicos. [56] Pol γ contiene un dominio de polimerasa en el extremo C y un dominio de exonucleasa 3'-5' en el extremo N que están conectados a través de la región conectora, que se une a la subunidad accesoria. La subunidad accesoria se une al ADN y es necesaria para la procesividad de Pol γ. La mutación puntual A467T en la región conectora es responsable de más de un tercio de todos los trastornos mitocondriales asociados a Pol γ. [57] Si bien muchos homólogos de Pol θ, codificado por el gen POLQ , se encuentran en eucariotas, su función no se comprende claramente. La secuencia de aminoácidos en el extremo C es lo que clasifica a Pol θ como polimerasa de la Familia A, aunque la tasa de error para Pol θ está más estrechamente relacionada con las polimerasas de la Familia Y. Pol θ extiende los extremos del cebador que no coinciden y puede evitar los sitios abásicos agregando un nucleótido. También tiene actividad desoxirribofosfodiesterasa (dRPasa) en el dominio polimerasa y puede mostrar actividad ATPasa muy cerca del ssDNA. [58] Pol ν (nu) se considera la menos eficaz de las enzimas polimerasas. [59] Sin embargo, la ADN polimerasa nu juega un papel activo en la reparación de la homología durante las respuestas celulares a los enlaces cruzados, cumpliendo su papel en un complejo con la helicasa . [59]
Las plantas utilizan dos polimerasas de la familia A para copiar los genomas mitocondrial y plástido. Son más similares al Pol I bacteriano que al Pol γ de los mamíferos. [60]
Los retrovirus codifican una ADN polimerasa inusual llamada transcriptasa inversa , que es una ADN polimerasa dependiente de ARN (RdDp) que sintetiza ADN a partir de una plantilla de ARN. La familia de la transcriptasa inversa contiene tanto la funcionalidad ADN polimerasa como la funcionalidad RNasa H, que degrada las bases del ARN emparejadas con el ADN. Un ejemplo de retrovirus es el VIH . [14] La transcriptasa inversa se emplea comúnmente en la amplificación de ARN con fines de investigación. Al utilizar una plantilla de ARN, la PCR puede utilizar la transcriptasa inversa, creando una plantilla de ADN. Esta nueva plantilla de ADN se puede utilizar luego para la amplificación por PCR típica. Los productos de tal experimento son, por tanto, productos de PCR amplificados a partir de ARN. [9]
Cada partícula de retrovirus del VIH contiene dos genomas de ARN , pero, tras una infección, cada virus genera sólo un provirus . [61] Después de la infección, la transcripción inversa va acompañada de un cambio de plantilla entre las dos copias del genoma (recombinación de elección de copia). [61] En cada ciclo de replicación se producen de 5 a 14 eventos de recombinación por genoma. [62] El cambio de plantilla (recombinación) parece ser necesario para mantener la integridad del genoma y como mecanismo de reparación para recuperar genomas dañados. [63] [61]
El bacteriófago (fago) T4 codifica una ADN polimerasa que cataliza la síntesis de ADN en dirección 5' a 3'. [64] La polimerasa del fago también tiene una actividad exonucleasa que actúa en una dirección de 3' a 5', [65] y esta actividad se emplea en la corrección y edición de bases recién insertadas. [66] Se observó que un fago mutante con una ADN polimerasa sensible a la temperatura , cuando se cultivaba a temperaturas permisivas, experimentaba recombinación a frecuencias aproximadamente dos veces mayores que las del fago de tipo salvaje. [67]
Se propuso que una alteración mutacional en la ADN polimerasa del fago puede estimular el cambio de cadena plantilla (recombinación de elección de copia) durante la replicación . [67]