El tetróxido de osmio (también óxido de osmio (VIII) ) es el compuesto químico con la fórmula OsO 4 . El compuesto destaca por sus múltiples usos, a pesar de su toxicidad y la rareza del osmio . También tiene una serie de propiedades inusuales, una de las cuales es que el sólido es volátil . El compuesto es incoloro, pero la mayoría de las muestras aparecen amarillas. [6] Esto probablemente se debe a la presencia de la impureza OsO 2 , que es de color amarillo-marrón. [7] En biología, su propiedad de unirse a lípidos lo ha convertido en una tinción ampliamente utilizada en microscopía electrónica.
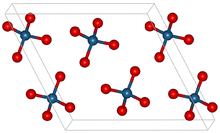
El óxido de osmio (VIII) forma cristales monoclínicos . [4] [8] Tiene un olor acre característico parecido al del cloro . El nombre del elemento osmio se deriva de osme , que en griego significa olor . El OsO 4 es volátil: se sublima a temperatura ambiente . Es soluble en una amplia gama de disolventes orgánicos. Es moderadamente soluble en agua, con la que reacciona reversiblemente para formar ácido ósmico (ver más abajo). [9] El óxido de osmio (VIII) puro es probablemente incoloro; [10] se ha sugerido que su tono amarillo es atribuible a impurezas de dióxido de osmio (OsO 2 ). [11] La molécula de tetróxido de osmio es tetraédrica y, por lo tanto, no polar. Esta no polaridad ayuda al OsO 4 a penetrar las membranas celulares cargadas.
El osmio de OsO 4 tiene un número de oxidación de VIII; sin embargo, el metal no posee una carga 8+ correspondiente ya que el enlace en el compuesto es en gran medida de carácter covalente (la energía de ionización requerida para producir una carga formal 8+ también excede con creces las energías disponibles en reacciones químicas normales). El átomo de osmio presenta dobles enlaces con los cuatro ligandos de óxido , lo que da como resultado un complejo de 16 electrones . Es isoelectrónico con iones de permanganato y cromato .
OsO 4 se forma lentamente cuando el polvo de osmio reacciona con O 2 a temperatura ambiente. La reacción del sólido a granel requiere calentamiento a 400 °C. [12]
Los alquenos se añaden al OsO 4 para dar especies de diolato que se hidrolizan a cis -dioles. El proceso neto se llama dihidroxilación. Esto procede a través de una reacción de cicloadición [3 + 2] entre el OsO 4 y el alqueno para formar un éster de osmato intermedio que se hidroliza rápidamente para producir el diol vecinal . A medida que los átomos de oxígeno se añaden en un paso concertado, la estereoquímica resultante es cis .
El OsO 4 es caro y altamente tóxico, lo que lo convierte en un reactivo poco atractivo para usar en cantidades estequiométricas . Sin embargo, sus reacciones se vuelven catalíticas agregando reoxidantes para reoxidar el subproducto Os (VI) nuevamente a Os (VIII). Los reactivos típicos incluyen H2O2 ( hidroxilación de Milas ) , N - óxido de N-metilmorfolina ( dihidroxilación de Upjohn ) y K3Fe (CN) 6 /agua. Estos reoxidantes no reaccionan por sí solos con los alquenos. Se pueden utilizar otros compuestos de osmio como catalizadores, incluidas las sales de osmato(VI) ([OsO 2 (OH) 4 )] 2− y el hidrato de tricloruro de osmio (OsCl 3 · x H 2 O). Estas especies se oxidan a osmio (VIII) en presencia de dichos oxidantes. [13]
Las bases de Lewis como las aminas terciarias y las piridinas aumentan la tasa de dihidroxilación. Esta "aceleración del ligando" surge mediante la formación del aducto OsO 4 L, que se agrega más rápidamente al alqueno. Si la amina es quiral, entonces la dihidroxilación puede proceder con enantioselectividad (ver Dihidroxilación asimétrica de Sharpless ). [14] OsO 4 no reacciona con la mayoría de los carbohidratos. [15]
El proceso se puede ampliar para dar dos aldehídos en la oxidación de Lemieux-Johnson , que utiliza peryodato para lograr la escisión del diol y regenerar la carga catalítica de OsO 4 . Este proceso es equivalente al de la ozonólisis .

OsO 4 es un ácido de Lewis y un oxidante suave. Reacciona con una solución acuosa alcalina para dar el anión perosmato OsO.
4(OH)2-2
. [17] Esta especie se reduce fácilmente al anión osmato , OsO
2(OH)2-4
.
Cuando la base de Lewis es una amina , también se forman aductos. Así, el OsO 4 se puede almacenar en forma de osmet , en la que el OsO 4 forma un complejo con hexamina . Osmeth puede disolverse en tetrahidrofurano (THF) y diluirse en una solución tampón acuosa para obtener una solución de trabajo diluida (0,25%) de OsO 4 . [18]
Con tert-BuNH 2 se produce el derivado imido :
De manera similar, con NH 3 se obtiene el complejo nitrido :
El anión [Os(N)O 3 ] − es isoelectrónico e isoestructural con OsO 4 .
OsO 4 es muy soluble en alcohol terc-butílico . En solución, el hidrógeno lo reduce fácilmente a osmio metálico. El osmio metálico suspendido se puede utilizar para catalizar la hidrogenación de una amplia variedad de sustancias químicas orgánicas que contienen enlaces dobles o triples.
OsO 4 sufre una "carbonilación reductora" con monóxido de carbono en metanol a 400 K y 200 sbar para producir el grupo triangular Os 3 (CO) 12 :
El osmio forma varios oxofluoruros, todos los cuales son muy sensibles a la humedad. Se forma cis -OsO 2 F 4 púrpura a 77 K en una solución de HF anhidro : [19]
OsO 4 también reacciona con F 2 para formar OsO 3 F 2 amarillo : [20]
OsO 4 reacciona con un equivalente de [Me 4 N]F a 298 K y 2 equivalentes a 253 K: [12]
En síntesis orgánica, el OsO 4 se utiliza ampliamente para oxidar alquenos a dioles vecinales , añadiendo dos grupos hidroxilo en el mismo lado ( adición sin ). Ver reacción y mecanismo arriba. Esta reacción se ha hecho tanto catalítica ( dihidroxilación de Upjohn ) como asimétrica ( dihidroxilación asimétrica de Sharpless ).
El óxido de osmio (VIII) también se utiliza en cantidades catalíticas en la oxiaminación Sharpless para producir aminoalcoholes vecinales .
En combinación con peryodato de sodio , el OsO 4 se utiliza para la escisión oxidativa de alquenos ( oxidación de Lemieux-Johnson ) cuando el peryodato sirve tanto para escindir el diol formado por dihidroxilación como para reoxidar el OsO 3 nuevamente a OsO 4 . La transformación neta es idéntica a la producida por ozonólisis . A continuación un ejemplo de la síntesis total de Isosteviol. [21]
OsO 4 es un agente de tinción ampliamente utilizado en microscopía electrónica de transmisión (TEM) para proporcionar contraste con la imagen. [22] Este método de tinción también puede ser conocido en la literatura como método OTO [23] [24] (osmio-tiocarbohidrazida-osmio), o técnica de impregnación con osmio [25] o simplemente como tinción con osmio. Como colorante de lípidos , también es útil en microscopía electrónica de barrido (SEM) como alternativa al recubrimiento por pulverización catódica . Incorpora un metal pesado directamente en las membranas celulares, creando una alta tasa de dispersión de electrones sin la necesidad de recubrir la membrana con una capa de metal, que puede oscurecer los detalles de la membrana celular. En la tinción de la membrana plasmática , el óxido de osmio (VIII) se une a las regiones de la cabeza de los fosfolípidos , creando así un contraste con el protoplasma vecino (citoplasma). Además, el óxido de osmio (VIII) también se utiliza para fijar muestras biológicas junto con HgCl 2 . Sus capacidades de matanza rápida se utilizan para matar rápidamente especímenes vivos como los protozoos. OsO 4 estabiliza muchas proteínas transformándolas en geles sin destruir sus características estructurales. Las proteínas tisulares estabilizadas por OsO 4 no son coaguladas por alcoholes durante la deshidratación. [15] El óxido de osmio (VIII) también se utiliza como colorante para lípidos en microscopía óptica. [26] OsO 4 también tiñe la córnea humana (ver consideraciones de seguridad).

También se utiliza preferentemente para teñir copolímeros , siendo el ejemplo más conocido los copolímeros en bloque en los que una fase puede teñirse para mostrar la microestructura del material. Por ejemplo, los copolímeros de bloques de estireno-butadieno tienen una cadena central de polibutadieno con tapas terminales de poliestireno. Cuando se trata con OsO 4 , la matriz de butadieno reacciona preferentemente y absorbe así el óxido. La presencia de un metal pesado es suficiente para bloquear el haz de electrones, por lo que los dominios de poliestireno se ven claramente en películas delgadas en TEM .
OsO 4 es un intermediario en la extracción de osmio de sus minerales. Los residuos que contienen osmio se tratan con peróxido de sodio (Na 2 O 2 ) formando Na 2 [OsO 4 (OH) 2 ], que es soluble. Cuando se expone al cloro , esta sal produce OsO 4 . En las etapas finales del refinado, el OsO 4 crudo se disuelve en NaOH alcohólico formando Na 2 [OsO 2 (OH) 4 ], que, cuando se trata con NH 4 Cl , da (NH 4 ) 4 [OsO 2 Cl 2 ]. Esta sal se reduce bajo hidrógeno para dar osmio. [9]
OsO 4 permitió la confirmación del modelo de balón de fútbol de buckminsterfullereno , un alótropo de carbono de 60 átomos . El aducto , formado a partir de un derivado de OsO 4 , era C 60 (OsO 4 )(4 - terc - butilpiridina ) 2 . El aducto rompió la simetría del fullereno, permitiendo la cristalización y confirmación de la estructura del C 60 mediante cristalografía de rayos X. [27]
El único uso clínico conocido del tetróxido de osmio es para el tratamiento de la artritis. [28] La falta de informes sobre efectos secundarios a largo plazo de la administración local de tetróxido de osmio (OsO 4 ) sugiere que el osmio en sí puede ser biocompatible , aunque esto depende del compuesto de osmio administrado.

OsO 4 manchará irreversiblemente la córnea humana , lo que puede provocar ceguera. El límite de exposición permitido para el óxido de osmio (VIII) (promedio ponderado en el tiempo de 8 horas) es de 2 µg/m 3 . [8] El óxido de osmio (VIII) puede penetrar plásticos y envases de alimentos y, por lo tanto, debe almacenarse en vidrio en refrigeración. [15]