En química , la dimerización es el proceso de unir dos entidades moleculares idénticas o similares mediante enlaces . Los enlaces resultantes pueden ser fuertes o débiles. Muchas especies químicas simétricas se describen como dímeros , incluso cuando el monómero es desconocido o altamente inestable. [1]
El término homodímero se utiliza cuando las dos subunidades son idénticas (p. ej. A–A) y heterodímero cuando no lo son (p. ej. A–B). El proceso inverso de la dimerización se suele denominar disociación . Cuando dos iones con carga opuesta se asocian para formar dímeros, se denominan pares de Bjerrum [2] , en honor al químico danés Niels Bjerrum .

Los ácidos carboxílicos anhidros forman dímeros mediante la unión de hidrógeno del hidrógeno ácido y el oxígeno del grupo carbonilo. Por ejemplo, el ácido acético forma un dímero en la fase gaseosa, donde las unidades monoméricas se mantienen unidas por enlaces de hidrógeno . [3] Muchas moléculas que contienen OH forman dímeros, por ejemplo, el dímero de agua .
Los excímeros y exciplejos son estructuras excitadas con una vida media corta. Por ejemplo, los gases nobles no forman dímeros estables, pero sí forman los excímeros Ar 2 *, Kr 2 * y Xe 2 * bajo alta presión y estimulación eléctrica. [4]

Los dímeros moleculares se forman a menudo por la reacción de dos compuestos idénticos, p. ej.: 2A → A−A . En este ejemplo, se dice que el monómero "A" se dimeriza para dar el dímero " A−A ". Un ejemplo es un diaminocarbeno , que se dimeriza para dar un tetraaminoetileno :
Los carbenos son altamente reactivos y forman enlaces fácilmente.
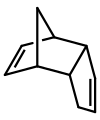
El diciclopentadieno es un dímero asimétrico de dos moléculas de ciclopentadieno que han reaccionado en una reacción de Diels-Alder para dar el producto. Al calentarse, se "craquea" (sufre una reacción retro-Diels-Alder) para dar monómeros idénticos:
Muchos elementos no metálicos se presentan como dímeros: hidrógeno , nitrógeno , oxígeno y los halógenos (es decir , flúor , cloro , bromo y yodo ). Los gases nobles pueden formar dímeros unidos por enlaces de van der Waals , como el dihelio o el diargón . El mercurio se presenta como un catión mercurio(I) ( Hg2+2), formalmente un ion dimérico. Otros metales pueden formar una proporción de dímeros en su fase de vapor. Los dímeros metálicos conocidos incluyen dilitio ( Li 2 ), disodio ( Na 2 ), dipotasio ( K 2 ), dirubidio ( Rb 2 ) y dicaesio ( Cs 2 ). Dichos dímeros elementales son moléculas diatómicas homonucleares .
Muchas moléculas orgánicas pequeñas , en particular el formaldehído , forman dímeros con facilidad. El dímero del formaldehído ( CH2O ) es el dioxetano ( C2H4O2 ) .
El borano ( BH 3 ) se presenta como el dímero diborano ( B 2 H 6 ), debido a la alta acidez de Lewis del centro de boro .
En el contexto de los polímeros , "dímero" también se refiere al grado de polimerización 2, independientemente de la estequiometría o de las reacciones de condensación .
Un caso en el que esto es aplicable es el de los disacáridos . Por ejemplo, la celobiosa es un dímero de la glucosa , aunque la reacción de formación produce agua :
Aquí, el dímero resultante tiene una estequiometría diferente del par inicial de monómeros.
Los disacáridos no necesitan estar compuestos por los mismos monosacáridos para ser considerados dímeros. Un ejemplo es la sacarosa , un dímero de fructosa y glucosa, que sigue la misma ecuación de reacción que la presentada anteriormente.
Los aminoácidos también pueden formar dímeros, que se denominan dipéptidos . Un ejemplo es la glicilglicina , que consiste en dos moléculas de glicina unidas por un enlace peptídico . Otros ejemplos son el aspartamo y la carnosina .
Muchas moléculas e iones se describen como dímeros, incluso cuando el monómero es difícil de encontrar.

El diborano ( B2H6 ) es un dímero inorgánico del borano . El B2H6 existe como una estructura en la que dos átomos de hidrógeno forman un puente entre los dos átomos de boro . [5]
Los compuestos de trialquilaluminio pueden existir como monómeros o dímeros, dependiendo del volumen estérico de los grupos unidos. Por ejemplo, el trimetilaluminio existe como dímero, pero el trimesitalluminio adopta una estructura monomérica. [6]
Los dímeros de pirimidina (también conocidos como dímeros de timina) se forman mediante una reacción fotoquímica a partir de bases de ADN de pirimidina cuando se exponen a la luz ultravioleta. [6] Esta reticulación provoca mutaciones del ADN , que pueden ser cancerígenas , causando cánceres de piel . [6] Cuando los dímeros de pirimidina están presentes, pueden bloquear las polimerasas , disminuyendo la funcionalidad del ADN hasta que se repare. [6]

Los dímeros de proteínas surgen de la interacción entre dos proteínas que pueden interactuar aún más para formar oligómeros más grandes y complejos . [7] Por ejemplo, la tubulina se forma por la dimerización de la α-tubulina y la β-tubulina y este dímero puede luego polimerizarse aún más para formar microtúbulos . [8] Para las proteínas simétricas, el complejo proteico más grande se puede descomponer en subunidades proteicas idénticas más pequeñas , que luego se dimerizan para disminuir el código genético requerido para formar la proteína funcional. [7]
Los receptores acoplados a proteína G (GPCR), la familia de receptores más grande y diversa del genoma humano, han sido estudiados ampliamente y estudios recientes respaldan su capacidad para formar dímeros. [9] Los dímeros de GPCR incluyen tanto homodímeros como heterodímeros formados a partir de miembros relacionados de la familia GPCR. [10] Si bien no todos, algunos GPCR requieren dimerización para funcionar, como el receptor GABA B , lo que enfatiza la importancia de los dímeros en los sistemas biológicos. [11]

Al igual que para los receptores acoplados a proteína G, la dimerización es esencial para que las tirosina quinasas del receptor (RTK) realicen su función en la transducción de señales , lo que afecta a muchos procesos celulares diferentes. [12] Las RTK normalmente existen como monómeros, pero experimentan un cambio conformacional al unirse al ligando , lo que les permite dimerizarse con RTK cercanos. [13] [14] La dimerización activa los dominios de quinasa citoplasmáticos que son responsables de una mayor transducción de señales . [12]