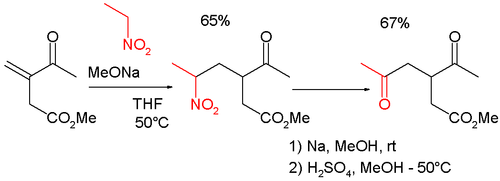
Reacción de Nef
[1][2][3][4] El nitroalcano 1, "relativamente ácido" debido al grupo nitro -NO2 atractor de electrones, se desprotona con bases como el hidróxido o un alcóxido.
En la actualidad, la alternativa de McMurry[7][8] es mucho más suave, en la que se produce la reducción directamente del nitroalcano primario o secundario empleando TiCl3 a imina, que hidroliza a continuación al grupo carbonilo.
Por el camino b, se produce la protonación sobre 5 del nitrógeno dando el intermedio 6 que por pérdida de HN(OH)2, etapa lenta, conduce al carbonilo protonado 7 que se desprotona al producto final carbonílico 8.
La relativa acidez, pKa≈10 para el nitrometano, de los hidrógenos del carbono unido al grupo nitro hace que se obtengan con cierta facilidad los nitronatos.
Estos pueden actuar como nucleófilos sobre electrófilos tales como, por ejemplo, haloalcanos, grupos carbonilo y aceptores de Michael.