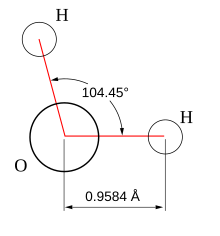
Geometría molecular
Las geometrías moleculares se determinan mejor cuando las muestras están próximas al cero absoluto porque a temperaturas más altas las moléculas presentarán un movimiento rotacional considerable.
En el estado sólido la geometría molecular puede ser medida por difracción de rayos X.
Las geometrías se pueden calcular por procedimientos mecánico cuánticos ab initio o por métodos semiempíricos de modelamiento molecular.
Los movimientos cuánticos (externos) de traslación y rotación cambian fuertemente la geometría molecular.
A temperaturas mayores, los modos vibracionales pueden ser excitados térmicamente (en un interpretación clásica, esto se expresa al enunciar que «las moléculas vibrarán más rápido»), pero siempre oscilan alrededor de una geometría reconocible para la molécula.
Pero, como movimiento mecánico cuántico, se excita a bajas temperaturas (comparada con la vibración).
Desde un punto de vista clásico, puede decirse que más moléculas rotan más rápidamente a temperatura ambiente, esto es que tienen mayor velocidad angular y momentum angular.
Otro método de unión entre átomos se denomina enlace iónico en el que intervienen cationes positivos y aniones negativos, sin que se formen moléculas sino redes iónicas.
Los isómeros son tipos de moléculas que comparten la misma fórmula química, pero que tienen diferentes geometrías, resultando en propiedades muy distintas: La geometría molecular se representa en una pirámide en la cual en la punta inicial hay una molécula de oxígeno con carga negativa, quedando en las otras dos puntas dos moléculas de hidrógeno con carga positiva, que son separadas por un ángulo de 104.5º; el enlace que une los hidrógenos con el oxígeno se llama enlace covalente, y también existe un enlace que une a otra pirámide idéntica a la anteriormente nombrada llamado enlace puente.