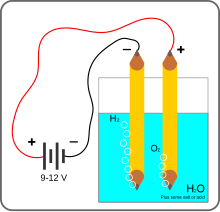
Electrólisis del agua
Una fuente de energía eléctrica se conecta a dos electrodos, o dos platos (típicamente hechos de algún metal inerte como el platino o el acero inoxidable), los cuales son puestos en el agua.
Esto se debe en parte a la escasa disociación del agua pura.
Sin esa energía extra, o sobrevoltaje, la electrólisis de agua pura ocurre muy lentamente si es que logra suceder.
Como aplicación específica es interesante comentar que la electrólisis del agua se utiliza también para generar oxígeno en la Estación Espacial Internacional que obviamente sirve para mantener la atmósfera de la estación y el hidrógeno se puede utilizar más adelante en una célula de combustible como método para almacenar energía y usar el agua que se genera en la célula para consumo de los astronautas.
El tubo vertical cilíndrico interior está abierto en la parte superior para permitir la adición de agua y el electrolito.
Cuando la corriente se hace pasar a través del voltámetro de Hofmann, el oxígeno gaseoso se forma en el ánodo (electrodo positivo) y el hidrógeno gaseoso en el cátodo (electrodo negativo).
Un electrolizador teórico 100% eficiente consumiría 39,4 kilovatios-hora por kilogramo (142 MJ/kg) de hidrógeno, 12749 julios por litro (12,75 MJ/m³).
En la práctica, la electrólisis (utilizando un electrolizador giratorio a una presión de 15 bar) puede llegar a consumir 50 kilovatios-hora por kilogramo (180 MJ/kg) y otros 15 kilovatios-hora (54 MJ) si el hidrógeno se comprime para su uso en coches de hidrógeno.
La eficiencia teórica para los electrolizadores de tipo PEM se supone que pueden llegar hasta el 94%.
Los electrolizadores de agua real requieren voltajes más altos para que la reacción continúe.
La parte que excede de 1,23 V con respecto al potencial real requerido se denomina sobrepotencial o sobrevoltaje, y representa cualquier tipo de pérdida y no finalidad en el proceso electroquímico.
Si se utilizan otros materiales menos eficaces para el cátodo (por ejemplo, grafito), aparecerán grandes sobrepotenciales.
Esto permite que el electrolizador funcione a una eficiencia eléctrica superior al 100%.
En los sistemas electroquímicos esto significa que se debe suministrar calor al reactor para sostener la reacción.
Potencialmente, un electrolizador que funcionara a una tensión de 1,48 V sería 100% eficiente.