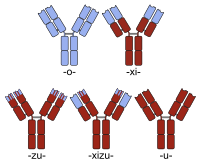
Anticuerpo humanizado
[1][2] El proceso de "humanización" se aplica generalmente a los anticuerpos monoclonales desarrollados para su administración a seres humanos (por ejemplo, anticuerpos desarrollados como fármacos contra el cáncer).
El paso que implica el ADN recombinante proporciona un punto de intervención que puede aprovecharse fácilmente para alterar la secuencia proteica del anticuerpo expresado.
Por lo tanto, todas las alteraciones de la estructura del anticuerpo que se consiguen en el proceso de humanización se efectúan mediante técnicas a nivel del ADN.
Ejemplos de anticuerpos quiméricos aprobados para terapia humana incluyen abciximab (ReoPro), basiliximab (Simulect), cetuximab (Erbitux), infliximab (Remicade) y rituximab (MabThera).
El proceso de alteración debe ser "selectivo" para conservar la especificidad para la que se desarrolló originalmente el anticuerpo.
Esto se consigue a nivel del ADN mediante mutagénesis.
El Alemtuzumab es un ejemplo temprano de un anticuerpo cuya humanización no incluyó un intermediario quimérico.
Por lo tanto, se utilizan procesos esencialmente idénticos a la humanización para incorporar y expresar las afinidades derivadas dentro de un anticuerpo completo.
[9][10] Es posible explotar la reacción inmunitaria humana en el descubrimiento de anticuerpos monoclonales.
Por lo tanto, las personas que experimentan un desafío a su sistema inmunitario, como una enfermedad infecciosa, un cáncer o una vacuna, son una fuente potencial de anticuerpos monoclonales dirigidos a ese desafío.