El reordenamiento de Beckmann , llamado así en honor al químico alemán Ernst Otto Beckmann (1853-1923), es un reordenamiento de un grupo funcional oxima a amidas sustituidas . [1] [2] El reordenamiento también se ha realizado con éxito en haloiminas y nitronas . Las oximas cíclicas y las haloiminas producen lactamas .
El reordenamiento de Beckmann es a menudo catalizado por ácido; sin embargo, se sabe que otros reactivos promueven el reordenamiento. Estos incluyen cloruro de tosilo , cloruro de tionilo , pentacloruro de fósforo , pentóxido de fósforo , trietilamina , hidróxido de sodio , yoduro de trimetilsililo , entre otros. [3] La fragmentación de Beckmann es otra reacción que a menudo compite con el reordenamiento, aunque la selección cuidadosa de las condiciones del reactivo promotor y del disolvente puede favorecer la formación de uno sobre el otro, a veces dando casi exclusivamente un producto. El reordenamiento ocurre estereoespecíficamente para cetoximas y N-cloro/N-fluoro iminas, siendo el grupo migratorio antiperiplanar al grupo saliente en el nitrógeno. Se sabe que ciertas condiciones racemizan la geometría de la oxima, lo que lleva a la formación de ambos regioisómeros . El reordenamiento de aldoximas ocurre con estereoespecificidad en la fase gaseosa y sin estereoespecificidad en la fase de solución. Algunas metodologías permiten la reorganización de aldoximas para formar amidas primarias, pero la fragmentación suele competir en estos sistemas. La reorganización de nitrona también ocurre sin estereoespecificidad; el regioisómero formado tiene el nitrógeno de la amida sustituido por el grupo que posee la mayor aptitud migratoria .
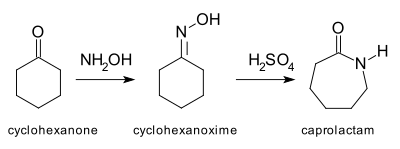
El reordenamiento de Beckmann arquetípico [4] es la conversión de ciclohexanona en caprolactama a través de la oxima. La caprolactama es la materia prima en la producción de nailon 6. [ 5]
La solución de Beckmann consta de ácido acético , ácido clorhídrico y anhídrido acético , y se utilizó ampliamente para catalizar la transposición. Se han utilizado otros ácidos, como el ácido sulfúrico , el ácido polifosfórico y el fluoruro de hidrógeno . El ácido sulfúrico es el ácido más comúnmente utilizado para la producción comercial de lactama debido a su formación de un subproducto de sulfato de amonio cuando se neutraliza con amoníaco . El sulfato de amonio es un fertilizante agrícola común que proporciona nitrógeno y azufre.
El mecanismo de reacción más común de la transposición de Beckmann consiste generalmente en una migración de alquilo antiperiplanar a la expulsión de un grupo saliente para formar un ion nitrilio . A esto le sigue una solvólisis para formar un imidato y luego una tautomerización para formar la amida: [6]
Se sabe que este ion nitrilio es interceptado por otros nucleófilos, incluido el grupo saliente de la oxima. [3]

Se supone que después de que el grupo fenilo migra y expulsa el cianato , este último ataca al ion nitrilio formado. En el tetracloruro de carbono se puede aislar el isocianato , mientras que en el etanol , el uretano se forma después de la solvólisis del isocianato.
Un estudio computacional ha establecido el mecanismo que explica las moléculas de disolvente y los sustituyentes. [7] La reorganización de la oxima de acetona en la solución de Beckmann involucró tres moléculas de ácido acético y un protón (presente como un ion oxonio ). En el estado de transición que conduce al ion iminio (complejo σ), el grupo metilo migra al átomo de nitrógeno en una reacción concertada a medida que se expulsa el grupo hidroxilo. El átomo de oxígeno en el grupo hidroxilo es estabilizado por tres moléculas de ácido acético. En el siguiente paso, el átomo de carbono electrófilo en el ion nitrilio es atacado por agua y un protón es donado de nuevo al ácido acético. En el estado de transición que conduce al imidato, el átomo de oxígeno del agua está coordinado con otros 4 átomos. En el tercer paso, un paso de isomerización protona el átomo de nitrógeno que conduce a la amida .
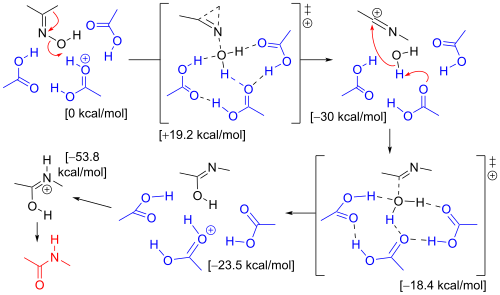
El mismo cálculo con un ion hidroxonio y 6 moléculas de agua tiene el mismo resultado, pero cuando el sustituyente migratorio es un grupo fenilo, el mecanismo favorece la formación de un complejo π intermedio de tres miembros. Este complejo π no se encuentra en el H 3 O + (H 2 O) 6 .

Con la ciclohexanona-oxima, el alivio de la tensión del anillo da lugar a un tercer mecanismo de reacción, que conduce directamente a la caprolactama protonada en un único paso concertado sin la formación intermedia de un complejo π o un complejo σ.
La transposición de Beckmann se puede convertir en catalítica utilizando cloruro cianúrico y cloruro de cinc como cocatalizador . Por ejemplo, la ciclododecanona se puede convertir en la lactama correspondiente , el monómero utilizado en la producción de nailon 12. [ 8] [9]
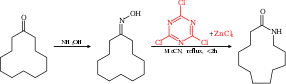
El mecanismo de reacción para esta reacción se basa en un ciclo catalítico en el que el cloruro cianúrico activa el grupo hidroxilo mediante una sustitución aromática nucleofílica . El producto de reacción se desprende y se reemplaza por un nuevo reactivo mediante un complejo de Meisenheimer intermedio .

La fragmentación de Beckmann es una reacción que frecuentemente compite con el reordenamiento de Beckmann. [3] Cuando el grupo α de la oxima es capaz de estabilizar la formación del carbocatión , la fragmentación se convierte en una vía de reacción viable. La reacción genera un nitrilo y un carbocatión, que se intercepta rápidamente para formar una variedad de productos. El nitrilo también se puede hidrolizar en condiciones de reacción para dar ácidos carboxílicos . Diferentes condiciones de reacción pueden favorecer la fragmentación sobre el reordenamiento.

Los centros de carbono cuaternario promueven la fragmentación al estabilizar la formación de carbocationes mediante hiperconjugación . Como se muestra en la imagen anterior, se forma el carbocatión "estable", que luego pierde un hidrógeno para dar lugar a un sitio de insaturación . Los átomos de oxígeno y nitrógeno también promueven la fragmentación mediante la formación de cetonas e iminas respectivamente.

El azufre también es capaz de promover la fragmentación, aunque a mayor distancia que el oxígeno o el nitrógeno.

El silicio es capaz de dirigir la fragmentación a través del efecto beta-silicio .
El intermedio carbocatión en esta reacción es interceptado por fluoruro nucleofílico de trifluoruro de dietilaminoazufre ( DAST ): [10]
La oxima de ciclohexenona con ácido forma anilina en una reacción de deshidratación- aromatización llamada reacción de Semmler-Wolff o aromatización de Wolff [11] [12] [13] [14]

El mecanismo se puede mostrar de la siguiente manera:

La reacción es intrínsecamente un caso especial del reordenamiento de Beckmann combinado con la participación del grupo vecino .
Una síntesis industrial de paracetamol desarrollada por Hoechst - Celanese implica la conversión de una metilcetona en una acetanilida a través de un reordenamiento de Beckmann. [15]
Se afirmó que el reordenamiento térmico que ocurre en la síntesis de ketamina era un reordenamiento de Beckmann según: url.