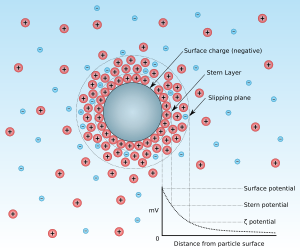
El potencial zeta es el potencial eléctrico en el plano de deslizamiento. Este plano es la interfaz que separa el fluido móvil del fluido que permanece adherido a la superficie.
Potencial zeta es un término científico para el potencial electrocinético [1] [2] en dispersiones coloidales . En la literatura de química coloidal , generalmente se denota con la letra griega zeta (ζ) , de ahí el potencial ζ . Las unidades habituales son voltios (V) o, más comúnmente, milivoltios (mV). Desde un punto de vista teórico, el potencial zeta es el potencial eléctrico en la doble capa interfacial (DL) en la ubicación del plano de deslizamiento con respecto a un punto del fluido a granel alejado de la interfaz. En otras palabras, el potencial zeta es la diferencia de potencial entre el medio de dispersión y la capa estacionaria de fluido unida a la partícula dispersada .
El potencial zeta es causado por la carga eléctrica neta contenida dentro de la región delimitada por el plano de deslizamiento y también depende de la ubicación de ese plano . Por tanto, es ampliamente utilizado para cuantificar la magnitud de la carga. Sin embargo, el potencial zeta no es igual al potencial de Stern o al potencial eléctrico de superficie en la doble capa, [3] [4] [5] [6] porque estos se definen en diferentes ubicaciones. Estos supuestos de igualdad deben aplicarse con cautela. Sin embargo, el potencial zeta es a menudo el único camino disponible para la caracterización de propiedades de doble capa.
El potencial zeta es un indicador importante y fácilmente mensurable de la estabilidad de las dispersiones coloidales. La magnitud del potencial zeta indica el grado de repulsión electrostática entre partículas adyacentes con carga similar en una dispersión. Para moléculas y partículas que son lo suficientemente pequeñas, un potencial zeta alto conferirá estabilidad, es decir, la solución o dispersión resistirá la agregación. Cuando el potencial es pequeño, las fuerzas de atracción pueden superar esta repulsión y la dispersión puede romperse y flocular . Por lo tanto, los coloides con potencial zeta alto (negativo o positivo) se estabilizan eléctricamente, mientras que los coloides con potenciales zeta bajos tienden a coagularse o flocularse como se describe en la tabla. [7]

El potencial Zeta también se puede utilizar para la estimación de pKa de polímeros complejos que, de otro modo, sería difícil de medir con precisión mediante métodos convencionales. Esto puede ayudar a estudiar el comportamiento de ionización de varios polímeros sintéticos y naturales en diversas condiciones y puede ayudar a establecer umbrales estandarizados de pH de disolución para polímeros sensibles al pH. [8]
Existen algunas técnicas de instrumentación nuevas que permiten medir el potencial zeta. El analizador de potencial Zeta puede medir materiales sólidos, fibras o polvo. El motor que se encuentra en el instrumento crea un flujo oscilante de solución electrolítica a través de la muestra. Varios sensores en el instrumento monitorean otros factores, por lo que el software adjunto puede realizar cálculos para encontrar el potencial zeta. Por este motivo, el instrumento mide la temperatura, el pH, la conductividad, la presión y el potencial de flujo.
El potencial Zeta también se puede calcular utilizando modelos teóricos y una movilidad electroforética determinada experimentalmente o una movilidad electroforética dinámica .
Los fenómenos electrocinéticos y los fenómenos electroacústicos son las fuentes habituales de datos para el cálculo del potencial zeta. (Ver valoración del potencial Zeta ).
La electroforesis se utiliza para estimar el potencial zeta de partículas , mientras que el potencial/corriente de flujo se utiliza para cuerpos porosos y superficies planas. En la práctica, el potencial zeta de dispersión se mide aplicando un campo eléctrico a través de la dispersión. Las partículas dentro de la dispersión con potencial zeta migrarán hacia el electrodo de carga opuesta con una velocidad proporcional a la magnitud del potencial zeta.
Esta velocidad se mide mediante la técnica del anemómetro láser Doppler . El cambio de frecuencia o cambio de fase de un rayo láser incidente causado por estas partículas en movimiento se mide como la movilidad de las partículas, y esta movilidad se convierte en potencial zeta ingresando la viscosidad del dispersante y la permitividad dieléctrica , y la aplicación de las teorías de Smoluchowski. [10]
La movilidad electroforética es proporcional a la velocidad electroforética, que es el parámetro medible. Existen varias teorías que vinculan la movilidad electroforética con el potencial zeta. Se describen brevemente en el artículo sobre electroforesis y en detalle en muchos libros sobre coloides y ciencia de interfaces.[3] [4] [5] [11] Existe un Informe Técnico IUPAC [12] elaborado por un grupo de expertos mundiales sobre los fenómenos electrocinéticos. Desde el punto de vista instrumental, existen tres técnicas experimentales diferentes: microelectroforesis , dispersión de luz electroforética y detección de pulso resistivo sintonizable . La microelectroforesis tiene la ventaja de producir una imagen de las partículas en movimiento. Por otro lado, esto se complica por la electroósmosis en las paredes de la celda de muestra. La dispersión de luz electroforética se basa en la dispersión de luz dinámica . Permite la medición en una celda abierta lo que elimina el problema del flujo electroosmótico excepto en el caso de una celda capilar. Y puede usarse para caracterizar partículas muy pequeñas, pero al precio de la pérdida de la capacidad de mostrar imágenes de partículas en movimiento. La detección de pulso resistivo sintonizable (TRPS) es una técnica de medición basada en impedancia que mide el potencial zeta de partículas individuales en función de la duración de la señal de pulso resistivo. [13] La duración de la translocación de nanopartículas se mide en función del voltaje y la presión aplicada. A partir del tiempo de translocación inverso frente a la movilidad electroforética dependiente del voltaje, se calculan los potenciales zeta. La principal ventaja del método TRPS es que permite mediciones simultáneas de tamaño y carga superficial partícula por partícula, lo que permite el análisis de un amplio espectro de nano/micropartículas sintéticas y biológicas y sus mezclas. [14]
Todas estas técnicas de medición pueden requerir dilución de la muestra. A veces, esta dilución puede afectar las propiedades de la muestra y cambiar el potencial zeta. Sólo hay una forma justificada de realizar esta dilución: utilizando sobrenadante de equilibrio . En este caso, el equilibrio interfacial entre la superficie y el líquido a granel se mantendría y el potencial zeta sería el mismo para todas las fracciones de volumen de partículas en la suspensión. Cuando se conoce el diluyente (como es el caso de una formulación química), se puede preparar diluyente adicional. Si se desconoce el diluyente, el sobrenadante de equilibrio se obtiene fácilmente mediante centrifugación .
El potencial de flujo es un potencial eléctrico que se desarrolla durante el flujo de líquido a través de un capilar. En la naturaleza, puede ocurrir un potencial de flujo de magnitud significativa en áreas con actividad volcánica. [15] El potencial de flujo es también el fenómeno electrocinético principal para la evaluación del potencial zeta en la interfaz material sólido-agua. Una muestra sólida correspondiente se dispone de tal manera que forme un canal de flujo capilar. Los materiales con una superficie plana se montan como muestras duplicadas que se alinean como placas paralelas. Las superficies de la muestra están separadas por una pequeña distancia para formar un canal de flujo capilar. Los materiales con forma irregular, como fibras o medios granulares, se montan como un tapón poroso para proporcionar una red de poros que sirve como capilares para la medición del potencial de flujo. Al aplicar presión sobre una solución de prueba, el líquido comienza a fluir y a generar un potencial eléctrico. Este potencial de flujo está relacionado con el gradiente de presión entre los extremos de un único canal de flujo (para muestras con una superficie plana) o del tapón poroso (para fibras y medios granulares) para calcular el potencial zeta de la superficie.
Como alternativa al potencial de transmisión, la medición de la corriente de transmisión ofrece otra aproximación al potencial zeta de superficie. Más comúnmente, las ecuaciones clásicas derivadas por Maryan Smoluchowski se utilizan para convertir el potencial de transmisión o los resultados de la corriente de transmisión en potencial zeta de superficie. [dieciséis]
Las aplicaciones del método de potencial de flujo y corriente de flujo para la determinación del potencial zeta de superficie consisten en la caracterización de la carga superficial de membranas poliméricas, [17] biomateriales y dispositivos médicos, [18] [19] y minerales. [20]
Hay dos efectos electroacústicos que se utilizan ampliamente para caracterizar el potencial zeta: la corriente de vibración coloidal y la amplitud sónica eléctrica . [5] Hay instrumentos disponibles comercialmente que explotan estos efectos para medir la movilidad electroforética dinámica, que depende del potencial zeta.
Las técnicas electroacústicas tienen la ventaja de poder realizar mediciones en muestras intactas, sin dilución. Las teorías publicadas y bien verificadas permiten tales mediciones en fracciones de volumen de hasta el 50%. El cálculo del potencial zeta a partir de la movilidad electroforética dinámica requiere información sobre las densidades de partículas y líquidos. Además, para partículas más grandes que superen aproximadamente los 300 nm de tamaño, también se requiere información sobre el tamaño de partícula. [ cita necesaria ]
The most known and widely used theory for calculating zeta potential from experimental data is that developed by Marian Smoluchowski in 1903.[21] This theory was originally developed for electrophoresis; however, an extension to electroacoustics is now also available.[5] Smoluchowski's theory is powerful because it is valid for dispersed particles of any shape and any concentration. However, it has its limitations:
The development of electrophoretic and electroacoustic theories with a wider range of validity was a purpose of many studies during the 20th century. There are several analytical theories that incorporate surface conductivity and eliminate the restriction of the small Dukhin number for both the electrokinetic and electroacoustic applications.
Early pioneering work in that direction dates back to Overbeek[22] and Booth.[23]
Modern, rigorous electrokinetic theories that are valid for any zeta potential, and often any , stem mostly from Soviet Ukrainian (Dukhin, Shilov, and others) and Australian (O'Brien, White, Hunter, and others) schools. Historically, the first one was Dukhin–Semenikhin theory.[24] A similar theory was created ten years later by O'Brien and Hunter.[25] Assuming a thin double layer, these theories would yield results that are very close to the numerical solution provided by O'Brien and White.[26] There are also general electroacoustic theories that are valid for any values of Debye length and Dukhin number.[5][11]
Cuando κa se encuentra entre valores grandes donde se encuentran disponibles modelos analíticos simples y valores bajos donde los cálculos numéricos son válidos, la ecuación de Henry se puede utilizar cuando el potencial zeta es bajo. Para una esfera no conductora, la ecuación de Henry es , donde f 1 es la función de Henry, una de una colección de funciones que varían suavemente de 1,0 a 1,5 a medida que κa se acerca al infinito. [12]