
Los bifosfonatos son una clase de medicamentos que previenen la pérdida de densidad ósea y se utilizan para tratar la osteoporosis y enfermedades similares. Son los medicamentos que se recetan con más frecuencia para tratar la osteoporosis. [1] Se denominan bifosfonatos porque tienen dos fosfonatos ( PO(OH)
2) grupos. Por ello también se les llama difosfonatos ( bis- o di- + fosfonato ).
La evidencia muestra que reducen el riesgo de fractura en mujeres posmenopáusicas con osteoporosis. [2] [3] [4] [5] [6]
El tejido óseo sufre una remodelación constante y se mantiene en equilibrio ( homeostasis ) gracias a los osteoblastos que crean hueso y a los osteoclastos que lo destruyen. Los bifosfonatos inhiben la digestión del hueso al estimular a los osteoclastos a sufrir apoptosis , o muerte celular, lo que ralentiza la pérdida ósea. [7]
Los usos de los bifosfonatos incluyen la prevención y el tratamiento de la osteoporosis, la enfermedad ósea de Paget , la metástasis ósea (con o sin hipercalcemia ), el mieloma múltiple , el hiperparatiroidismo primario , la osteogénesis imperfecta , la displasia fibrosa y otras afecciones que presentan fragilidad ósea.
Los bifosfonatos se utilizan para tratar la osteoporosis, la osteítis deformante (enfermedad de Paget del hueso), la metástasis ósea (con o sin hipercalcemia), el mieloma múltiple y otras afecciones que involucran huesos frágiles y quebradizos.
En la osteoporosis y la enfermedad de Paget, los fármacos bifosfonatos de primera línea más populares son el alendronato y el risedronato . Si estos son ineficaces o si la persona desarrolla problemas del tracto digestivo, se puede utilizar pamidronato intravenoso. El ranelato de estroncio o la teriparatida se utilizan para la enfermedad refractaria. El uso de ranelato de estroncio está restringido debido al aumento del riesgo de tromboembolia venosa , embolia pulmonar y trastornos cardiovasculares graves, incluido el infarto de miocardio . [8] En mujeres posmenopáusicas, el modulador selectivo del receptor de estrógeno raloxifeno se administra ocasionalmente en lugar de bifosfonatos. Los bifosfonatos son beneficiosos para reducir el riesgo de fractura vertebral en la osteoporosis inducida por esteroides . [9]
Los bifosfonatos se recomiendan como tratamiento de primera línea para la osteoporosis posmenopáusica. [5] [10] [11] [12]
El tratamiento a largo plazo con bifosfonatos produce efectos antifracturas y de densidad mineral ósea que persisten durante 3 a 5 años después de un tratamiento inicial de 3 a 5 años. [2] El bifosfonato alendronato reduce el riesgo de fracturas de cadera, vértebras y muñeca en un 35-39%; el zoledronato reduce el riesgo de fracturas de cadera en un 38% y de fracturas vertebrales en un 62%. [3] [4] También se ha demostrado que el risedronato reduce el riesgo de fracturas de cadera. [5] [6]
Después de cinco años de medicación por vía oral o tres años de medicación intravenosa en aquellos con bajo riesgo, se puede suspender el tratamiento con bifosfonatos. [13] En aquellos con mayor riesgo se pueden utilizar diez años de medicación por vía oral o seis años de tratamiento intravenoso. [13]
Los bifosfonatos reducen el riesgo de fractura y dolor óseo [14] en personas con cáncer de mama, [15] pulmón, [16] y otros cánceres metastásicos, así como en personas con mieloma múltiple. [17] En el cáncer de mama hay evidencia mixta sobre si los bifosfonatos mejoran la supervivencia. [15] [18] [19] [20] Una revisión Cochrane de 2017 encontró que para las personas con cáncer de mama temprano, el tratamiento con bifosfonatos puede reducir el riesgo de que el cáncer se propague al hueso de la persona, sin embargo, para las personas que tenían cáncer de mama avanzado, el tratamiento con bifosfonatos no pareció reducir el riesgo de que el cáncer se propague al hueso. [15] Los efectos secundarios asociados con el tratamiento con bifosfonatos para personas con cáncer de mama son leves y raros. [15]
Los bifosfonatos también pueden reducir la mortalidad en pacientes con mieloma múltiple y cáncer de próstata. [20]
La evidencia sugiere que el uso de bifosfonatos sería útil en el tratamiento del síndrome de dolor regional complejo , un problema neuroinmune con puntuaciones altas en el MPQ, baja eficacia del tratamiento y síntomas que pueden incluir osteoporosis regional. En 2009, los bifosfonatos estaban "entre la única clase de medicamentos que ha sobrevivido a estudios controlados con placebo que mostraron una mejoría estadísticamente significativa (en el CRPS) con la terapia". [21]
Los bifosfonatos se han utilizado para reducir las tasas de fracturas en niños con osteogénesis imperfecta [22] y para tratar la otosclerosis [23] minimizando la pérdida ósea.
Otros bifosfonatos, incluidos el medronato (R 1 =H, R 2 =H) y el oxidronato (R 1 =H, R 2 =OH), se mezclan con tecnecio radiactivo y se inyectan como una forma de obtener imágenes de los huesos y detectar enfermedades óseas.
Los bifosfonatos orales pueden causar malestar estomacal , inflamación y erosiones del esófago , que es el principal problema de las preparaciones orales que contienen N [ se necesita más explicación ] , es decir, las que contienen cadenas no ramificadas "normales". Esto se puede prevenir permaneciendo sentado en posición vertical durante 30 a 60 minutos después de tomar el medicamento. Los bifosfonatos intravenosos pueden producir fiebre y síntomas similares a los de la gripe después de la primera infusión, lo que se cree que ocurre debido a su potencial para activar las células T γδ humanas .
Los bifosfonatos, cuando se administran por vía intravenosa para el tratamiento del cáncer, se han asociado con osteonecrosis de la mandíbula (ONM), siendo la mandíbula afectada con el doble de frecuencia que el maxilar y la mayoría de los casos se producen después de la administración intravenosa de dosis altas utilizada para algunos pacientes con cáncer. La mandíbula fosfatasa alcalina se ha descrito desde la época victoriana. Alrededor del 60% de los casos son precedidos por un procedimiento quirúrgico dental (que afecta al hueso), y se ha sugerido que el tratamiento con bifosfonatos debe posponerse hasta después de cualquier trabajo dental para eliminar posibles sitios de infección (el uso de antibióticos puede estar indicado antes de cualquier cirugía). [24]
Se han notificado varios casos de dolor intenso en huesos, articulaciones o músculos esqueléticos, lo que ha motivado cambios en el etiquetado. [25]
Algunos estudios han identificado el uso de bifosfonatos como un factor de riesgo para la fibrilación auricular (FA), aunque el meta-análisis de ellos encuentra informes contradictorios. A partir de 2008 [actualizar], la Administración de Alimentos y Medicamentos de los EE. UU. no recomendó ninguna modificación en la prescripción de bifosfonatos en función de las preocupaciones por la FA. [26] Los meta-análisis más recientes han encontrado fuertes correlaciones entre el uso de bifosfonatos y el desarrollo de FA, especialmente cuando se administra por vía intravenosa, [27] pero que un riesgo significativamente mayor de FA que requirió hospitalización no tuvo un riesgo asociado mayor de accidente cerebrovascular o mortalidad cardiovascular. [28]
En estudios a gran escala, las mujeres que toman bifosfonatos para la osteoporosis han tenido fracturas inusuales ("fracturas por bifosfonatos") en el fémur (hueso del muslo) en la diáfisis o región subtrocantérea del hueso, en lugar de en el cuello femoral, que es el sitio más común de fractura. Sin embargo, estas fracturas son raras (12 en 14.195 mujeres) en comparación con las fracturas de cadera comunes (272 en 14.195 mujeres), y la reducción general de las fracturas de cadera causadas por bifosfonatos es mayor que el aumento de las fracturas inusuales de la diáfisis. [29] [ fuente obsoleta ] Existe la preocupación de que el uso prolongado de bifosfonatos pueda resultar en una supresión excesiva del recambio óseo . Se plantea la hipótesis de que las microfisuras en el hueso no pueden curarse y eventualmente se unen y propagan, lo que resulta en fracturas atípicas. Dichas fracturas tienden a curarse mal y a menudo requieren alguna forma de estimulación ósea, por ejemplo, un injerto óseo como procedimiento secundario. Esta complicación no es común y el beneficio de la reducción general de la fractura aún se mantiene. [29] [30] [ se necesita una fuente no primaria ] En los casos en los que existe la preocupación de que se produzcan dichas fracturas, la teriparatida es potencialmente una buena alternativa porque no causa tanto daño como un bifosfonato al suprimir el recambio óseo. [31]
Tres metanálisis han evaluado si el uso de bifosfonatos está asociado con un mayor riesgo de cáncer de esófago. Dos estudios concluyeron que no había evidencia de un mayor riesgo. [32] [33] [34]
Todos los medicamentos bifosfonatos comparten una "columna vertebral" común de fósforo-carbono-fósforo:
Los dos PO
3Los grupos ( fosfonatos ) unidos covalentemente al carbono determinan tanto el nombre "bisfosfonato " como la función de los fármacos. El término bis se refiere al hecho de que existen dos grupos de este tipo en la molécula.
La cadena lateral larga (R 2 en el diagrama) determina las propiedades químicas, el modo de acción y la potencia de los bisfosfonatos. La cadena lateral corta (R 1 ), a menudo llamada "gancho", influye principalmente en las propiedades químicas y la farmacocinética .
Consulte las secciones nitrogenadas y no nitrogenadas en el Mecanismo de acción a continuación.
Del bisfosfonato que se reabsorbe (a partir de la preparación oral) o se infunde (para fármacos intravenosos ), aproximadamente el 50% se excreta sin cambios por el riñón. El resto tiene una afinidad muy alta por el tejido óseo y se adsorbe rápidamente en la superficie ósea. Una vez que los bisfosfonatos están en el hueso, tienen una vida media de eliminación muy larga que puede superar los diez años. [35]
Los bisfosfonatos son estructuralmente similares al pirofosfato , pero con un carbono central que puede tener hasta dos sustituyentes (R 1 y R 2 ) en lugar de un átomo de oxígeno. Debido a que un grupo bisfosfonato imita la estructura del pirofosfato, puede inhibir la activación de las enzimas que utilizan pirofosfato.
La especificidad de los fármacos a base de bisfosfonatos proviene de los dos grupos de fosfonatos (y posiblemente un hidroxilo en R 1 ) que trabajan juntos para coordinar los iones de calcio. Las moléculas de bisfosfonatos se unen preferentemente a los iones de calcio . La mayor reserva de calcio en el cuerpo humano se encuentra en los huesos, por lo que los bisfosfonatos se acumulan en una alta concentración solo en los huesos.
Los bifosfonatos, cuando se adhieren al tejido óseo, son liberados por los osteoclastos , las células óseas que descomponen el tejido óseo. Las moléculas de bifosfonato se adhieren a los osteoclastos y entran en ellos, donde alteran las funciones enzimáticas intracelulares necesarias para la resorción ósea . [36]
Existen dos clases de compuestos de bisfosfonatos: no nitrogenados (sin nitrógeno en R 2 ) y nitrogenados (R 2 contiene nitrógeno). Los dos tipos de bisfosfonatos actúan de forma diferente en la inhibición de los osteoclastos.
Los bisfosfonatos no nitrogenados (difosfonatos) se metabolizan en la célula a compuestos que reemplazan la porción terminal pirofosfato del ATP, formando una molécula no funcional que compite con el trifosfato de adenosina (ATP) en el metabolismo energético celular. El osteoclasto inicia la apoptosis y muere, lo que conduce a una disminución general de la degradación ósea. Este tipo de bisfosfonato tiene en general más efectos negativos que el grupo que contiene nitrógeno y se prescribe con mucha menos frecuencia. [37]
Los bifosfonatos nitrogenados actúan sobre el metabolismo óseo uniéndose y bloqueando la enzima farnesil difosfato sintasa (FPPS) en la vía de la HMG-CoA reductasa (también conocida como vía del mevalonato). [38]
Los bifosfonatos que contienen cadenas de isopreno en la posición R 1 o R 2 pueden impartir especificidad para la inhibición de GGPS1 . [39]
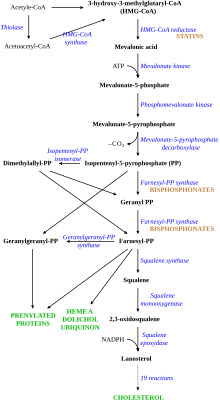
La alteración de la vía de la HMG CoA-reductasa a nivel de FPPS impide la formación de dos metabolitos ( farnesol y geranilgeraniol ) que son esenciales para conectar algunas proteínas pequeñas a la membrana celular . Este fenómeno se conoce como prenilación y es importante para el tráfico adecuado de proteínas subcelulares (consulte " proteína anclada a lípidos " para conocer los principios de este fenómeno). [40]
Si bien la inhibición de la prenilación de proteínas puede afectar a muchas proteínas que se encuentran en un osteoclasto , se ha especulado que la alteración de la modificación lipídica de las proteínas Ras , Rho y Rac es la base de los efectos de los bifosfonatos. Estas proteínas pueden afectar tanto a la osteoclastogénesis, como a la supervivencia celular y a la dinámica del citoesqueleto. En particular, el citoesqueleto es vital para mantener el "borde ondulado" que se requiere para el contacto entre un osteoclasto en reabsorción y una superficie ósea.
Las estatinas son otra clase de fármacos que inhiben la vía de la HMG-CoA reductasa. A diferencia de los bifosfonatos, las estatinas no se unen a las superficies óseas con alta afinidad y, por lo tanto, no son específicas para el hueso. Sin embargo, algunos estudios han informado de una disminución de la tasa de fracturas (un indicador de osteoporosis ) y/o un aumento de la densidad mineral ósea en los usuarios de estatinas. La eficacia general de las estatinas en el tratamiento de la osteoporosis sigue siendo controvertida. [41]
Los bifosfonatos se desarrollaron en el siglo XIX, pero se investigaron por primera vez en la década de 1960 para su uso en trastornos del metabolismo óseo. Su uso no médico era para ablandar el agua en los sistemas de riego utilizados en los naranjales. La razón inicial para su uso en humanos fue su potencial para prevenir la disolución de la hidroxiapatita , el principal mineral óseo, deteniendo así la pérdida ósea. En la década de 1990, su mecanismo de acción real se demostró con el lanzamiento inicial del alendronato por parte de Merck & Co. [42]