El meristemo es un tipo de tejido que se encuentra en las plantas. Está formado por células indiferenciadas ( células meristemáticas ) capaces de dividirse celularmente . Las células del meristemo pueden convertirse en todos los demás tejidos y órganos que se encuentran en las plantas. Estas células continúan dividiéndose hasta un momento en que se diferencian y luego pierden la capacidad de dividirse.
Las células vegetales diferenciadas generalmente no pueden dividirse ni producir células de un tipo diferente. Las células meristemáticas no están diferenciadas o están incompletamente diferenciadas. Son totipotentes y capaces de continuar la división celular . La división de las células meristemáticas proporciona nuevas células para la expansión y diferenciación de los tejidos y la iniciación de nuevos órganos, proporcionando la estructura básica del cuerpo vegetal. Las células son pequeñas, con vacuolas pequeñas o ninguna, y el protoplasma llena la célula por completo. Los plastidios ( cloroplastos o cromoplastos ), son indiferenciados, pero están presentes en forma rudimentaria ( proplastidios ). Las células meristemáticas están muy juntas sin espacios intercelulares. La pared celular es una pared celular primaria muy delgada .
El término meristemo fue utilizado por primera vez en 1858 por Carl Wilhelm von Nägeli (1817-1891) en su libro Beiträge zur Wissenschaftlichen Botanik ("Contribuciones a la botánica científica"). [1] Se deriva de la palabra griega merizein (μερίζειν), que significa dividir, en reconocimiento de su función inherente. [ cita necesaria ]
Hay tres tipos de tejidos meristemáticos: apical (en las puntas), intercalar o basal (en el medio) y lateral (en los lados también conocido como cambium). En la cima del meristemo, hay un pequeño grupo de células que se dividen lentamente, lo que comúnmente se denomina zona central. Las células de esta zona tienen una función de células madre y son esenciales para el mantenimiento del meristemo. Las tasas de proliferación y crecimiento en la cima del meristemo suelen diferir considerablemente de las de la periferia.
Los meristemas apicales son los meristemas completamente indiferenciados (indeterminados) de una planta. Estos se diferencian en tres tipos de meristemas primarios. Los meristemas primarios a su vez producen los dos tipos de meristemas secundarios. Estos meristemas secundarios también se conocen como meristemas laterales porque participan en el crecimiento lateral.

Hay dos tipos de tejido de meristemo apical: el meristemo apical del brote ( SAM ), que da lugar a órganos como las hojas y las flores, y el meristemo apical de la raíz ( RAM ), que proporciona las células meristemáticas para el futuro crecimiento de las raíces. Las células SAM y RAM se dividen rápidamente y se consideran indeterminadas, ya que no poseen ningún estado final definido. En ese sentido, las células meristemáticas se comparan frecuentemente con las células madre de los animales, que tienen un comportamiento y función análogos.
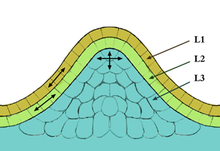
Los meristemas apicales están estratificados y el número de capas varía según el tipo de planta. En general la capa más externa se llama túnica mientras que las capas más internas son el cuerpo . En las monocotiledóneas , la túnica determina las características físicas del borde y margen de la hoja. En las dicotiledóneas , la capa dos del corpus determina las características del borde de la hoja. El cuerpo y la túnica desempeñan un papel fundamental en la apariencia física de la planta, ya que todas las células vegetales se forman a partir de los meristemas. Los meristemas apicales se encuentran en dos ubicaciones: la raíz y el tallo. Algunas plantas árticas tienen un meristemo apical en la parte media/inferior de la planta. Se cree que este tipo de meristemo evolucionó porque resulta ventajoso en las condiciones del Ártico. [ cita necesaria ]

Los meristemas apicales de los brotes son la fuente de todos los órganos aéreos, como las hojas y las flores. Las células en la cima del meristemo apical del brote sirven como células madre para la región periférica circundante, donde proliferan rápidamente y se incorporan a los primordios diferenciados de hojas o flores.
El meristemo apical del brote es el sitio de la mayor parte de la embriogénesis en las plantas con flores. [ cita necesaria ] Los primordios de hojas, sépalos, pétalos, estambres y ovarios se inician aquí a razón de uno en cada intervalo de tiempo, lo que se denomina plastocrón . Es donde se manifiestan los primeros indicios de que se ha evocado el desarrollo floral. Uno de estos indicios podría ser la pérdida de la dominancia apical y la liberación de células que de otro modo estarían inactivas para desarrollarse como meristemas de brotes auxiliares, en algunas especies en las axilas de los primordios tan cerca como a dos o tres de la cúpula apical.
El meristemo apical del brote consta de cuatro grupos celulares distintos:
Estas cuatro zonas distintas se mantienen mediante una compleja vía de señalización. En Arabidopsis thaliana , se requieren tres genes CLAVATA que interactúan para regular el tamaño del reservorio de células madre en el meristemo apical del vástago controlando la tasa de división celular . [2] Se prevé que CLV1 y CLV2 formen un complejo receptor (de la familia de quinasas similares a receptores LRR) del cual CLV3 es un ligando . [3] [4] [5] CLV3 comparte cierta homología con las proteínas ESR del maíz, con una región corta de 14 aminoácidos conservada entre las proteínas. [6] [7] Las proteínas que contienen estas regiones conservadas se han agrupado en la familia de proteínas CLE. [6] [7]
Se ha demostrado que CLV1 interactúa con varias proteínas citoplasmáticas que probablemente estén involucradas en la señalización posterior . Por ejemplo, se ha descubierto que el complejo CLV está asociado con pequeñas proteínas relacionadas con la GTPasa Rho/Rac . [2] Estas proteínas pueden actuar como intermediario entre el complejo CLV y una proteína quinasa activada por mitógenos (MAPK), que a menudo participa en cascadas de señalización. [8] KAPP es una proteína fosfatasa asociada a quinasa que se ha demostrado que interactúa con CLV1. [9] Se cree que KAPP actúa como un regulador negativo de CLV1 al desfosforilarlo. [9]
Otro gen importante en el mantenimiento del meristemo de las plantas es WUSCHEL (abreviado como WUS ), que es un objetivo de la señalización del CLV además de regular positivamente el CLV, formando así un circuito de retroalimentación. [10] WUS se expresa en las células debajo de las células madre del meristemo y su presencia previene la diferenciación de las células madre. [10] CLV1 actúa para promover la diferenciación celular reprimiendo la actividad WUS fuera de la zona central que contiene las células madre. [2]
La función de WUS en el meristemo apical del brote está relacionada con la fitohormona citoquinina . La citoquinina activa las histidina quinasas que luego fosforilan las proteínas de histidina fosfotransferencia. [11] Posteriormente, los grupos fosfato se transfieren a dos tipos de reguladores de respuesta de Arabidopsis (ARR): ARRS tipo B y ARR tipo A. Los ARR tipo B funcionan como factores de transcripción para activar genes aguas abajo de la citoquinina , incluidos los A-ARR. Los A-ARR son similares a los B-ARR en estructura; sin embargo, los A-ARR no contienen los dominios de unión al ADN que tienen los B-ARR y que son necesarios para funcionar como factores de transcripción. [12] Por lo tanto, los A-ARR no contribuyen a la activación de la transcripción y, al competir por los fosfatos de las proteínas de fosfotransferencia, inhiben la función de los B-ARR. [13] En el SAM, los B-ARR inducen la expresión de WUS , que induce la identidad de las células madre. [14] WUS luego suprime los A-ARR. [15] Como resultado, los B-ARR ya no se inhiben, lo que provoca una señalización sostenida de citoquininas en el centro del meristemo apical del brote. Junto con la señalización CLAVATA, este sistema funciona como un circuito de retroalimentación negativa. La señalización de citoquininas se ve reforzada positivamente por WUS para prevenir la inhibición de la señalización de citoquininas, mientras que WUS promueve su propio inhibidor en forma de CLV3, que en última instancia mantiene bajo control a WUS y la señalización de citoquininas. [dieciséis]
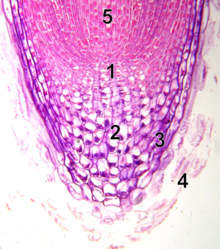
A diferencia del meristemo apical del brote, el meristemo apical de la raíz produce células en dos dimensiones. Alberga dos grupos de células madre alrededor de un centro organizador llamado células del centro inactivo (QC) y juntas producen la mayoría de las células en una raíz adulta. [17] [18] En su ápice, el meristemo de la raíz está cubierto por la cofia de la raíz, que protege y guía su trayectoria de crecimiento. Las células se desprenden continuamente de la superficie exterior de la cofia de la raíz . Las células QC se caracterizan por su baja actividad mitótica. La evidencia sugiere que el control de calidad mantiene las células madre circundantes impidiendo su diferenciación, a través de señales que aún están por descubrir. Esto permite un suministro constante de nuevas células en el meristemo necesarias para el crecimiento continuo de las raíces. Hallazgos recientes indican que el control de calidad también puede actuar como un reservorio de células madre para reponer lo que se pierda o dañe. [19] El meristemo apical de la raíz y los patrones de tejido se establecen en el embrión en el caso de la raíz primaria, y en el nuevo primordio de la raíz lateral en el caso de las raíces secundarias.
En las angiospermas, los meristemas intercalares (a veces llamados basales) se encuentran en tallos monocotiledóneas (en particular, de pasto ) en la base de los nudos y las láminas de las hojas. La cola de caballo y la Welwitschia también presentan crecimiento intercalar. Los meristemas intercalares son capaces de dividirse celular y permiten un rápido crecimiento y rebrote de muchas monocotiledóneas. Los meristemas intercalares en los nudos del bambú permiten un rápido alargamiento del tallo, mientras que los de la base de la mayoría de las hojas de la hierba permiten que las hojas dañadas vuelvan a crecer rápidamente. Este rebrote de hojas en los pastos evolucionó en respuesta al daño causado por los herbívoros que pastaban.
Cuando las plantas comienzan a florecer, el meristemo apical del brote se transforma en un meristemo de inflorescencia, que luego produce el meristemo floral, que produce los sépalos, pétalos, estambres y carpelos de la flor.
A diferencia de los meristemas apicales vegetativos y algunos meristemas de eflorescencia, los meristemas florales no pueden continuar creciendo indefinidamente. Su crecimiento se limita a la flor con un tamaño y forma particular. La transición del meristemo del brote al meristemo floral requiere genes de identidad del meristemo floral, que especifican los órganos florales y causan la terminación de la producción de células madre. AGAMOUS ( AG ) es un gen homeótico floral requerido para la terminación del meristemo floral y necesario para el desarrollo adecuado de los estambres y carpelos . [2] AG es necesario para evitar la conversión de meristemas florales en meristemas de brotes de inflorescencia, pero es el gen de identidad LEAFY ( LFY ) y WUS y está restringido al centro del meristemo floral o a los dos verticilos internos. [20] De esta manera se logra la identidad floral y la especificidad de la región. WUS activa AG uniéndose a una secuencia consenso en el segundo intrón de AG y LFY se une a sitios de reconocimiento adyacentes. [20] Una vez que se activa AG, reprime la expresión de WUS, lo que lleva a la terminación del meristemo. [20]
A lo largo de los años, los científicos han manipulado los meristemas florales por razones económicas. Un ejemplo es la planta de tabaco mutante "Maryland Mammoth". En 1936, el departamento de agricultura de Suiza realizó varias pruebas científicas con esta planta. "Maryland Mammoth" se caracteriza por el hecho de que crece mucho más rápido que otras plantas de tabaco.
La dominancia apical es donde un meristemo previene o inhibe el crecimiento de otros meristemas. Como resultado, la planta tendrá un tronco principal claramente definido. Por ejemplo, en los árboles, la punta del tronco principal lleva el meristemo del brote dominante. Por lo tanto, la punta del tronco crece rápidamente y no queda sombreada por las ramas. Si se corta el meristemo dominante, una o más puntas de las ramas asumirán la dominancia. La rama empezará a crecer más rápido y el nuevo crecimiento será vertical. Con el paso de los años, la rama puede empezar a parecerse cada vez más a una extensión del tronco principal. A menudo, varias ramas mostrarán este comportamiento después de la eliminación del meristemo apical, lo que dará lugar a un crecimiento tupido.
El mecanismo de dominancia apical se basa en las auxinas , tipos de reguladores del crecimiento de las plantas. Estos se producen en el meristemo apical y se transportan hacia las raíces en el cambium . Si la dominancia apical es completa, impiden que se formen ramas mientras el meristemo apical esté activo. Si la dominancia es incompleta, se desarrollarán ramas laterales. [ cita necesaria ]
Investigaciones recientes sobre la dominancia apical y el control de la ramificación han revelado una nueva familia de hormonas vegetales denominada estrigolactonas . Anteriormente se sabía que estos compuestos estaban involucrados en la germinación de semillas y la comunicación con hongos micorrízicos y ahora se ha demostrado que están involucrados en la inhibición de la ramificación. [21]
El SAM contiene una población de células madre que también producen los meristemas laterales mientras el tallo se alarga. Resulta que el mecanismo de regulación del número de células madre podría conservarse evolutivamente. El gen CLAVATA CLV2 responsable del mantenimiento de la población de células madre en Arabidopsis thaliana está muy relacionado con el gen del maíz FASCIATION EAR 2 ( FEA2 ) también implicado en la misma función. [22] De manera similar, en el arroz, el sistema FON1-FON2 parece tener una estrecha relación con el sistema de señalización CLV en Arabidopsis thaliana . [23] Estos estudios sugieren que la regulación del número, la identidad y la diferenciación de las células madre podría ser un mecanismo conservado evolutivamente en las monocotiledóneas , si no en las angiospermas . El arroz también contiene otro sistema genético distinto de FON1-FON2 , que participa en la regulación del número de células madre . [23] Este ejemplo subraya la innovación que se produce en el mundo de los vivos todo el tiempo.


Los cribados genéticos han identificado genes pertenecientes a la familia KNOX en esta función. Básicamente, estos genes mantienen las células madre en un estado indiferenciado. La familia KNOX ha experimentado bastante diversificación evolutiva manteniendo el mecanismo general más o menos similar. Se han encontrado miembros de la familia KNOX en plantas tan diversas como Arabidopsis thaliana , arroz, cebada y tomate. Los genes similares a KNOX también están presentes en algunas algas , musgos, helechos y gimnospermas . La expresión errónea de estos genes conduce a la formación de características morfológicas interesantes. Por ejemplo, entre los miembros de Antirrhineae , sólo las especies del género Antirrhinum carecen de una estructura llamada espolón en la región floral. Un estímulo se considera una innovación evolutiva porque define la especificidad y la atracción de los polinizadores . Los investigadores llevaron a cabo mutagénesis de transposones en Antirrhinum majus y vieron que algunas inserciones conducían a la formación de espolones que eran muy similares a los otros miembros de Antirrhineae , [24] lo que indica que la pérdida de espolón en las poblaciones silvestres de Antirrhinum majus probablemente podría ser una innovación evolutiva. .
La familia KNOX también ha estado implicada en la evolución de la forma de las hojas (consulte a continuación una discusión más detallada) . Un estudio examinó el patrón de expresión del gen KNOX en A. thaliana , que tiene hojas simples, y Cardamine hirsuta , una planta que tiene hojas complejas . En A. thaliana , los genes KNOX están completamente desactivados en las hojas, pero en C.hirsuta , la expresión continuó, generando hojas complejas. [25] Además, se ha propuesto que el mecanismo de acción del gen KNOX se conserva en todas las plantas vasculares , porque existe una estrecha correlación entre la expresión de KNOX y una morfología foliar compleja . [26]
Los meristemas apicales pueden diferenciarse en tres tipos de meristemas primarios:
Estos meristemas son responsables del crecimiento primario , o un aumento en longitud o altura, llamados meristemas. [28] [29]
Hay dos tipos de meristemas secundarios, también llamados meristemas laterales porque rodean el tallo establecido de una planta y hacen que crezca lateralmente (es decir, de mayor diámetro).
Aunque cada planta crece de acuerdo con un cierto conjunto de reglas, cada nuevo meristemo de raíz y brote puede seguir creciendo mientras esté vivo. En muchas plantas, el crecimiento meristemático es potencialmente indeterminado , lo que hace que la forma general de la planta no esté determinada de antemano. Este es el crecimiento primario . El crecimiento primario conduce al alargamiento del cuerpo de la planta y a la formación de órganos. Todos los órganos vegetales surgen en última instancia de divisiones celulares en los meristemas apicales, seguidas de expansión y diferenciación celular. El crecimiento primario da origen a la parte apical de muchas plantas.
El crecimiento de nódulos radiculares fijadores de nitrógeno en leguminosas como la soja y los guisantes es determinado o indeterminado. Así, la soja (o la judía y el Lotus japonicus) producen determinados nódulos (esféricos), con un sistema vascular ramificado que rodea la zona central infectada. A menudo, las células infectadas por Rhizobium sólo tienen pequeñas vacuolas. En cambio, los nódulos de los guisantes, los tréboles y Medicago truncatula son indeterminados, para mantener (al menos durante algún tiempo) un meristemo activo que produce nuevas células para la infección por Rhizobium. Por tanto, existen zonas de madurez en el nódulo. Las células infectadas suelen poseer una gran vacuola. El sistema vascular de la planta es ramificado y periférico.
En condiciones apropiadas, cada meristemo de brote puede convertirse en una nueva planta o clon completo . Estas nuevas plantas se pueden cultivar a partir de esquejes que contienen un meristemo apical. Sin embargo, los meristemas apicales de las raíces no se clonan fácilmente. Esta clonación se llama reproducción asexual o reproducción vegetativa y se practica ampliamente en horticultura para producir en masa plantas de un genotipo deseable . Se ha demostrado que este proceso conocido como mericloning reduce o elimina los virus presentes en la planta madre en múltiples especies de plantas. [30] [31]
La propagación a través de esquejes es otra forma de propagación vegetativa que inicia la producción de raíces o brotes a partir de células cambiales meristemáticas secundarias. Esto explica por qué las "heridas" basales de los esquejes de los brotes a menudo ayudan a la formación de raíces. [32]
También se pueden inducir meristemas en las raíces de leguminosas como la soja , Lotus japonicus , guisantes y Medicago truncatula después de la infección con bacterias del suelo comúnmente llamadas Rhizobia . [ cita necesaria ] Las células de la corteza interna o externa en la llamada "ventana de nodulación" justo detrás de la punta de la raíz en desarrollo se inducen a dividirse. La sustancia señal crítica es el factor Nod lipooligosacárido , decorado con grupos laterales para permitir la especificidad de la interacción. Las proteínas receptoras del factor Nod NFR1 y NFR5 se clonaron a partir de varias legumbres, incluidas Lotus japonicus , Medicago truncatula y soja ( Glycine max ). La regulación de los meristemas de los nódulos utiliza una regulación a larga distancia conocida como autorregulación de la nodulación (AON). Este proceso involucra quinasas receptoras LRR ubicadas en el tejido vascular de la hoja (LjHAR1, GmNARK y MtSUNN), señalización peptídica CLE e interacción KAPP, similar a la observada en el sistema CLV1,2,3. LjKLAVIER también exhibe un fenotipo de regulación de nódulos , aunque aún no se sabe cómo se relaciona con las otras quinasas receptoras de AON.
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )