Las células T son uno de los tipos importantes de glóbulos blancos del sistema inmunológico y desempeñan un papel central en la respuesta inmune adaptativa . Las células T se pueden distinguir de otros linfocitos por la presencia de un receptor de células T (TCR) en su superficie celular .
Las células T nacen de células madre hematopoyéticas , [1] que se encuentran en la médula ósea . Las células T en desarrollo luego migran a la glándula del timo para desarrollarse (o madurar). Las células T derivan su nombre del timo . [2] [3] Después de la migración al timo, las células precursoras maduran y se convierten en varios tipos distintos de células T. La diferenciación de las células T también continúa después de que han abandonado el timo. Los grupos de subtipos de células T diferenciados y específicos tienen una variedad de funciones importantes en el control y la configuración de la respuesta inmune .
Una de estas funciones es la muerte celular mediada por el sistema inmunitario y la llevan a cabo dos subtipos principales: células T CD8+ "asesinas" (citotóxicas) y CD4+ "auxiliares" . (Estos reciben su nombre por la presencia de las proteínas de la superficie celular CD8 o CD4 ). Las células T CD8+, también conocidas como "células T asesinas", son citotóxicas , lo que significa que pueden matar directamente las células infectadas por virus, así como células cancerosas. Las células T CD8+ también pueden utilizar pequeñas proteínas de señalización, conocidas como citoquinas , para reclutar otros tipos de células cuando desarrollan una respuesta inmune. Una población diferente de células T, las células T CD4+, funcionan como "células auxiliares". A diferencia de las células T asesinas CD8+, las células T auxiliares (T H ) CD4+ funcionan activando aún más las células B de memoria y las células T citotóxicas, lo que conduce a una mayor respuesta inmune. La respuesta inmune adaptativa específica regulada por las células T H depende de su subtipo (como T-helper1, T-helper2, T-helper17, células T reguladoras), [4] que se distingue por los tipos de citoquinas que secretan. [2]
Las células T reguladoras son otra población distinta de células T que proporcionan el mecanismo crítico de tolerancia , mediante el cual las células inmunes pueden distinguir las células invasoras de las "propias". Esto evita que las células inmunes reaccionen de manera inapropiada contra las propias células, lo que se conoce como respuesta " autoinmune ". Por esta razón, estas células T reguladoras también han sido denominadas células T "supresoras". Estas mismas células T reguladoras también pueden ser cooptadas por las células cancerosas para prevenir el reconocimiento de las células tumorales y una respuesta inmune contra ellas.
Todas las células T se originan a partir de células madre hematopoyéticas (HSC) c-kit + Sca1 + que residen en la médula ósea. En algunos casos, el origen podría ser el hígado fetal durante el desarrollo embrionario . Luego, las HSC se diferencian en progenitores multipotentes (MPP) que conservan el potencial de convertirse en células mieloides y linfoides . El proceso de diferenciación continúa hacia un progenitor linfoide común (CLP), que sólo puede diferenciarse en células T, B o NK. [5] Estas células CLP luego migran a través de la sangre al timo, donde se injertan:. En adelante se les conoce como timocitos , el estadio inmaduro de una célula T.
Las primeras células que llegaron al timo se denominan comúnmente doble negativas , ya que no expresan ni el correceptor CD4 ni el CD8 . Las células CLP recién llegadas son células CD4 - CD8 - CD44 + CD25 - ckit + y se denominan células progenitoras tímicas tempranas (ETP). [6] Estas células luego se someterán a una ronda de división y regularán negativamente el c-kit y se denominan células doble negativas (DN1). Para convertirse en células T, los timocitos deben pasar por múltiples etapas de DN, así como por selección positiva y selección negativa.
Los timocitos doblemente negativos pueden identificarse mediante la expresión superficial de CD2 , CD5 y CD7 . Aún durante las etapas doble negativas, la expresión de CD34 se detiene y se expresa CD1 . La expresión tanto de CD4 como de CD8 los hace doblemente positivos y maduran en células CD4+ o CD8+.
Un paso crítico en la maduración de las células T es crear un receptor de células T funcional (TCR). Cada célula T madura contendrá en última instancia un TCR único que reacciona a un patrón aleatorio, lo que permite al sistema inmunológico reconocer muchos tipos diferentes de patógenos . Este proceso es esencial para desarrollar inmunidad a amenazas que el sistema inmunológico no ha encontrado antes, ya que debido a la variación aleatoria siempre habrá al menos un TCR que coincida con cualquier patógeno nuevo.
Un timocito sólo puede convertirse en una célula T activa cuando sobrevive al proceso de desarrollo de un TCR funcional. El TCR consta de dos componentes principales, las cadenas alfa y beta. Ambos contienen elementos aleatorios diseñados para producir una amplia variedad de TCR diferentes, pero debido a esta gran variedad deben probarse para asegurarse de que funcionen. Primero, los timocitos intentan crear una cadena beta funcional, probándola con una cadena alfa "simulada". Luego intentan crear una cadena alfa funcional. Una vez que se ha producido un TCR funcional, las células deben probar si su TCR identificará las amenazas correctamente y, para ello, es necesario reconocer el complejo principal de histocompatibilidad (MHC) del cuerpo en un proceso conocido como selección positiva. El timocito también debe asegurarse de no reaccionar adversamente a los antígenos "propios" , lo que se denomina selección negativa. Si tanto la selección positiva como la negativa tienen éxito, el TCR se vuelve completamente operativo y el timocito se convierte en una célula T.
En la etapa DN2 (CD44 + CD25 + ), las células regulan positivamente los genes de recombinación RAG1 y RAG2 y reorganizan el locus TCRβ , combinando genes de recombinación VDJ y de región constante en un intento de crear una cadena TCRβ funcional. A medida que el timocito en desarrollo avanza hasta la etapa DN3 (CD44 - CD25 + ), el timocito expresa una cadena α invariante llamada pre-Tα junto con el gen TCRβ. Si la cadena β reordenada se empareja exitosamente con la cadena α invariante, se producen señales que dejan de reordenar la cadena β (y silencian el alelo alternativo). [7] Aunque estas señales requieren el pre-TCR en la superficie celular, son independientes de la unión del ligando al pre-TCR. Si las cadenas se emparejan con éxito, se forma un pre-TCR y la célula regula negativamente el CD25 y se denomina célula DN4 (CD25 - CD44 - ). Luego, estas células experimentan una ronda de proliferación y comienzan a reorganizar el locus TCRα durante la etapa doble positiva .
El proceso de selección positiva dura de 3 a 4 días y ocurre en la corteza tímica. [8] Los timocitos doblemente positivos (CD4 + /CD8 + ) migran profundamente hacia la corteza tímica , donde se les presentan autoantígenos . Estos autoantígenos son expresados por células epiteliales corticales tímicas en moléculas MHC, que residen en la superficie de las células epiteliales corticales. Sólo los timocitos que interactúan bien con MHC-I o MHC-II recibirán una "señal de supervivencia" vital, mientras que aquellos que no puedan interactuar con suficiente fuerza no recibirán ninguna señal y morirán por negligencia. Este proceso garantiza que los timocitos supervivientes tendrán una "afinidad por el MHC", lo que significa que pueden desempeñar funciones útiles en el cuerpo, respondiendo a las moléculas del MHC para ayudar a las respuestas inmunitarias. La gran mayoría de los timocitos en desarrollo no pasarán la selección positiva y morirán durante este proceso. [9]
El destino de un timocito se determina durante la selección positiva. Las células doblemente positivas (CD4 + /CD8 + ) que interactúan bien con las moléculas del MHC de clase II eventualmente se convertirán en células "auxiliares" CD4 + , mientras que los timocitos que interactúan bien con las moléculas del MHC de clase I maduran hasta convertirse en células "asesinas" CD8 + . Un timocito se convierte en una célula CD4 + al regular negativamente la expresión de sus receptores de superficie celular CD8. Si la célula no pierde su señal, continuará regulando negativamente CD8 y se convertirá en CD4 + ; tanto las células CD8 + como las CD4 + son ahora células positivas únicas . [10]
Este proceso no filtra los timocitos que pueden causar autoinmunidad . Las células potencialmente autoinmunes se eliminan mediante el siguiente proceso de selección negativa, que ocurre en la médula tímica.
La selección negativa elimina los timocitos que son capaces de unirse fuertemente a las moléculas "propias" del MHC. Los timocitos que sobreviven a la selección positiva migran hacia el límite de la corteza y la médula en el timo. Mientras están en la médula, se les presenta nuevamente un autoantígeno presentado en el complejo MHC de células epiteliales del timo medular (mTEC). [11] Los mTEC deben tener un regulador autoinmune positivo (AIRE + ) para expresar adecuadamente los autoantígenos de todos los tejidos del cuerpo en sus péptidos MHC de clase I. Algunas mTEC son fagocitadas por células dendríticas del timo ; esto las convierte en AIRE - células presentadoras de antígenos (APC), lo que permite la presentación de autoantígenos en moléculas de MHC de clase II (las células CD4 + seleccionadas positivamente deben interactuar con estas moléculas de MHC de clase II, por lo que las APC, que poseen MHC de clase II, deben ser presente para la selección negativa de células T CD4 + ). Los timocitos que interactúan demasiado fuertemente con el autoantígeno reciben una señal apoptótica que conduce a la muerte celular. Sin embargo, algunas de estas células se seleccionan para convertirse en células Treg . Las células restantes salen del timo como células T maduras vírgenes , también conocidas como emigrantes tímicos recientes. [12] Este proceso es un componente importante de la tolerancia central y sirve para prevenir la formación de células T autorreactivas que son capaces de inducir enfermedades autoinmunes en el huésped.
La selección β es el primer punto de control, donde a los timocitos que pueden formar un pre-TCR funcional (con una cadena alfa invariante y una cadena beta funcional) se les permite continuar desarrollándose en el timo. A continuación, la selección positiva comprueba que los timocitos hayan reorganizado con éxito su locus TCRα y sean capaces de reconocer moléculas de MHC con la afinidad adecuada. La selección negativa en la médula elimina los timocitos que se unen con demasiada fuerza a los autoantígenos expresados en las moléculas del MHC. Estos procesos de selección permiten la tolerancia de uno mismo por parte del sistema inmunológico. Las células T vírgenes típicas que abandonan el timo (a través de la unión corticomedular) son autorrestringidas, autotolerantes y positivas únicas.
Aproximadamente el 98% de los timocitos muere durante los procesos de desarrollo en el timo al fallar la selección positiva o negativa, mientras que el otro 2% sobrevive y abandona el timo para convertirse en células T maduras inmunocompetentes. [13] El timo aporta menos células a medida que una persona envejece. A medida que el timo se contrae aproximadamente un 3% [14] por año durante la mediana edad, se produce una caída correspondiente en la producción tímica de células T vírgenes, lo que deja que la expansión y regeneración de las células T periféricas desempeñen un papel más importante en la protección de las personas mayores.
Las células T se agrupan en una serie de subconjuntos según su función. Las células T CD4 y CD8 se seleccionan en el timo, pero se diferencian aún más en la periferia hasta convertirse en células especializadas que tienen diferentes funciones. Los subconjuntos de células T se definieron inicialmente por su función, pero también tienen patrones de expresión de genes o proteínas asociados.

Las células T colaboradoras (células T H ) ayudan a otros linfocitos, incluida la maduración de las células B en células plasmáticas y células B de memoria , y la activación de células T citotóxicas y macrófagos . Estas células también se conocen como células T CD4 + ya que expresan la glicoproteína CD4 en sus superficies. Las células T auxiliares se activan cuando se les presentan antígenos peptídicos mediante moléculas MHC de clase II , que se expresan en la superficie de las células presentadoras de antígenos (APC). Una vez activados, se dividen rápidamente y secretan citoquinas que regulan o ayudan a la respuesta inmune. Estas células pueden diferenciarse en uno de varios subtipos, que tienen diferentes funciones. Las citoquinas dirigen las células T hacia subtipos particulares. [15]
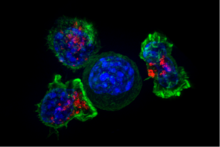
Las células T citotóxicas (células T C , CTL, células T asesinas, células T asesinas) destruyen las células infectadas por virus y las células tumorales y también están implicadas en el rechazo de trasplantes . Estas células se definen por la expresión de la proteína CD8 en su superficie celular. Las células T citotóxicas reconocen sus objetivos uniéndose a péptidos cortos (de 8 a 11 aminoácidos de longitud) asociados con moléculas MHC de clase I , presentes en la superficie de todas las células nucleadas. Las células T citotóxicas también producen las citoquinas clave IL-2 e IFNγ. Estas citocinas influyen en las funciones efectoras de otras células, en particular de los macrófagos y las células NK.
Las células T sin antígeno se expanden y se diferencian en células T de memoria y efectoras después de encontrar su antígeno afín dentro del contexto de una molécula MHC en la superficie de una célula presentadora de antígeno profesional (por ejemplo, una célula dendrítica). Debe estar presente una coestimulación adecuada en el momento del encuentro con el antígeno para que se produzca este proceso. Históricamente, se pensaba que las células T de memoria pertenecían a los subtipos de memoria efectora o central, cada uno con su propio conjunto distintivo de marcadores de superficie celular (ver más abajo). [19] Posteriormente, se descubrieron numerosas poblaciones nuevas de células T de memoria, incluidas células T de memoria residentes en tejidos (Trm), células TSCM de memoria madre y células T de memoria virtual. El único tema unificador para todos los subtipos de células T de memoria es que son de larga vida y pueden expandirse rápidamente a un gran número de células T efectoras al volver a exponerse a su antígeno afín. Mediante este mecanismo proporcionan al sistema inmunológico "memoria" contra patógenos encontrados previamente. Las células T de memoria pueden ser CD4 + o CD8 + y normalmente expresan CD45RO . [20]
Subtipos de células T de memoria:
Las células T reguladoras son cruciales para el mantenimiento de la tolerancia inmunológica . Su función principal es desactivar la inmunidad mediada por células T hacia el final de una reacción inmunitaria y suprimir las células T autorreactivas que escaparon del proceso de selección negativa en el timo.
Se han descrito dos clases principales de células T reg CD4 + : células T reg FOXP3 + y células T reg FOXP3 − .
Las células T reguladoras pueden desarrollarse durante el desarrollo normal en el timo, y luego se conocen como células Treg tímicas, o pueden inducirse periféricamente y se denominan células Treg derivadas periféricamente. Estos dos subconjuntos se denominaban anteriormente "naturales" y "adaptativos" (o "inducidos"), respectivamente. [26] Ambos subconjuntos requieren la expresión del factor de transcripción FOXP3 que puede usarse para identificar las células. Las mutaciones del gen FOXP3 pueden impedir el desarrollo de células T reguladoras, lo que provoca la enfermedad autoinmune mortal IPEX .
Varios otros tipos de células T tienen actividad supresora, pero no expresan FOXP3 de forma constitutiva. Estas incluyen las células Tr1 y Th3 , que se cree que se originan durante una respuesta inmune y actúan produciendo moléculas supresoras. Las células Tr1 están asociadas con IL-10 y las células Th3 están asociadas con TGF-beta . Recientemente, se han agregado células Th17 a esta lista. [27]
Las células T de tipo innato o las células T no convencionales representan algunos subconjuntos de células T que se comportan de manera diferente en la inmunidad. Desencadenan respuestas inmunitarias rápidas, independientemente de la expresión del complejo principal de histocompatibilidad (MHC), a diferencia de sus homólogos convencionales (células T auxiliares CD4 y células T citotóxicas CD8), que dependen del reconocimiento de antígenos peptídicos en el contexto de la molécula MHC. En general, existen tres grandes poblaciones de células T no convencionales: células NKT, células MAIT y células T gammadelta. Actualmente, sus funciones funcionales ya están bien establecidas en el contexto de las infecciones y el cáncer. [28] Además, estos subconjuntos de células T se están traduciendo en muchas terapias contra enfermedades malignas como la leucemia, por ejemplo. [29]
Las células T asesinas naturales (células NKT, que no deben confundirse con las células asesinas naturales del sistema inmunológico innato) unen el sistema inmunológico adaptativo con el sistema inmunológico innato . A diferencia de las células T convencionales que reconocen antígenos peptídicos proteicos presentados por moléculas del complejo principal de histocompatibilidad (MHC), las células NKT reconocen antígenos glicolípidos presentados por CD1d . Una vez activadas, estas células pueden realizar funciones atribuidas tanto a las células T colaboradoras como a las citotóxicas: producción de citocinas y liberación de moléculas citolíticas/destructoras de células. También son capaces de reconocer y eliminar algunas células tumorales y células infectadas con virus del herpes. [30]
Las células T invariantes asociadas a las mucosas (MAIT) muestran cualidades innatas similares a las de los efectores. [31] [32] En los seres humanos, las células MAIT se encuentran en la sangre, el hígado, los pulmones y las mucosas , defendiendo contra la actividad microbiana y las infecciones. [31] La proteína similar al MHC de clase I , MR1 , es responsable de presentar metabolitos de vitamina B producidos por bacterias a las células MAIT. [33] [34] [35] Después de la presentación del antígeno extraño por MR1, las células MAIT secretan citoquinas proinflamatorias y son capaces de lisar células infectadas bacterianamente. [31] [35] Las células MAIT también se pueden activar mediante señalización independiente de MR1. [35] Además de poseer funciones similares a las innatas, este subconjunto de células T apoya la respuesta inmune adaptativa y tiene un fenotipo similar a la memoria. [31] Además, se cree que las células MAIT desempeñan un papel en enfermedades autoinmunes , como la esclerosis múltiple , la artritis y la enfermedad inflamatoria intestinal , [36] [37] aunque aún no se han publicado pruebas definitivas. [38] [39] [40] [41]
Las células T gamma delta (células T γδ) representan un pequeño subconjunto de células T que poseen un TCR γδ en lugar del TCR αβ en la superficie celular. La mayoría de las células T expresan cadenas de TCR αβ. Este grupo de células T es mucho menos común en humanos y ratones (alrededor del 2 % del total de células T) y se encuentran principalmente en la mucosa intestinal , dentro de una población de linfocitos intraepiteliales . En conejos, ovejas y pollos, el número de células T γδ puede llegar al 60% del total de células T. Las moléculas antigénicas que activan las células T γδ aún se desconocen en gran medida. Sin embargo, las células T γδ no están restringidas al MHC y parecen ser capaces de reconocer proteínas completas en lugar de requerir que las moléculas del MHC presenten péptidos en las APC . Algunas células T γδ murinas reconocen moléculas MHC de clase IB. Las células T γδ humanas que utilizan los fragmentos de los genes Vγ9 y Vδ2 constituyen la principal población de células T γδ en la sangre periférica. Estas células son únicas porque responden específica y rápidamente a un conjunto de precursores isoprenoides fosforilados no peptídicos , denominados colectivamente fosfoantígenos , que son producidos por prácticamente todas las células vivas. Los fosfoantígenos más comunes de células animales y humanas (incluidas las células cancerosas) son el pirofosfato de isopentenilo (IPP) y su isómero pirofosfato de dimetilalilo (DMPP). Muchos microbios producen el compuesto activo hidroxi-DMAPP ( HMB-PP ) y los correspondientes conjugados de mononucleótidos, además de IPP y DMAPP. Las células vegetales producen ambos tipos de fosfoantígenos. Los fármacos que activan las células T humanas Vγ9/Vδ2 comprenden fosfoantígenos sintéticos y aminobifosfonatos , que regulan positivamente el IPP/DMAPP endógeno.
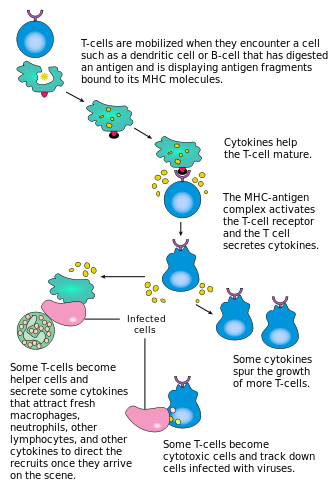
La activación de las células T CD4 + se produce mediante la participación simultánea del receptor de células T y una molécula coestimuladora (como CD28 o ICOS ) en la célula T por el péptido del complejo principal de histocompatibilidad (MHCII) y moléculas coestimuladoras en la célula T. APC . Ambos son necesarios para la producción de una respuesta inmune eficaz; en ausencia de coestimulación , la señalización del receptor de células T por sí sola produce anergia . Las vías de señalización aguas abajo de las moléculas coestimuladoras generalmente interactúan con la vía PI3K , generando PIP3 en la membrana plasmática y reclutando el dominio PH que contiene moléculas de señalización como PDK1 , que son esenciales para la activación de PKC-θ y, finalmente , la producción de IL-2 . La respuesta óptima de las células T CD8 + depende de la señalización de CD4 + . [43] Las células CD4 + son útiles en la activación antigénica inicial de las células T CD8+ vírgenes y en el mantenimiento de las células T CD8 + de memoria después de una infección aguda. Por tanto, la activación de las células T CD4 + puede ser beneficiosa para la acción de las células T CD8 + . [44] [45] [46]
La primera señal la proporciona la unión del receptor de células T a su péptido afín presentado en MHCII en una APC. MHCII está restringido a las llamadas células presentadoras de antígenos profesionales , como células dendríticas, células B y macrófagos, por nombrar algunas. Los péptidos presentados a las células T CD8 + por las moléculas del MHC de clase I tienen entre 8 y 13 aminoácidos de longitud; Los péptidos presentados a las células CD4 + por las moléculas del MHC de clase II son más largos, generalmente de 12 a 25 aminoácidos de longitud, [47] ya que los extremos de la hendidura de unión de la molécula del MHC de clase II están abiertos.
La segunda señal proviene de la coestimulación, en la que los receptores de superficie de la APC son inducidos por un número relativamente pequeño de estímulos, generalmente productos de patógenos, pero a veces productos de degradación de las células, como cuerpos necróticos o proteínas de choque térmico . El único receptor coestimulador expresado constitutivamente por las células T vírgenes es el CD28, por lo que la coestimulación de estas células proviene de las proteínas CD80 y CD86 , que juntas constituyen la proteína B7 (B7.1 y B7.2, respectivamente) en el APC. Otros receptores se expresan tras la activación de la célula T, como OX40 e ICOS, pero estos dependen en gran medida de CD28 para su expresión. La segunda señal autoriza a las células T a responder a un antígeno. Sin él, la célula T se vuelve anérgica y le resulta más difícil activarse en el futuro. Este mecanismo previene respuestas inapropiadas hacia uno mismo, ya que los autopéptidos generalmente no se presentan con una coestimulación adecuada. Una vez que una célula T se ha activado adecuadamente (es decir, ha recibido la señal uno y la señal dos), altera la expresión de una variedad de proteínas en la superficie celular. Los marcadores de activación de células T incluyen CD69, CD71 y CD25 (también un marcador de células Treg) y HLA-DR (un marcador de activación de células T humanas). La expresión de CTLA-4 también está regulada positivamente en las células T activadas, que a su vez superan a CD28 en la unión a las proteínas B7. Este es un mecanismo de control para prevenir la sobreactivación de las células T. Las células T activadas también cambian su perfil de glicosilación de la superficie celular. [48]
El receptor de células T existe como un complejo de varias proteínas. El receptor de células T real está compuesto por dos cadenas peptídicas separadas, que se producen a partir de los genes alfa y beta del receptor de células T independientes ( TCRα y TCRβ ). Las otras proteínas del complejo son las proteínas CD3 : heterodímeros CD3εγ y CD3εδ y, lo más importante, un homodímero CD3ζ, que tiene un total de seis motivos ITAM . Los motivos ITAM en CD3ζ pueden ser fosforilados por Lck y, a su vez, reclutar ZAP-70 . Lck y/o ZAP-70 también pueden fosforilar las tirosinas en muchas otras moléculas, entre ellas CD28, LAT y SLP-76 , lo que permite la agregación de complejos de señalización alrededor de estas proteínas.
LAT fosforilada recluta SLP-76 en la membrana, donde luego puede incorporar PLC-γ , VAV1 , Itk y potencialmente PI3K . PLC-γ escinde PI(4,5)P2 en la valva interna de la membrana para crear los intermediarios activos diacilglicerol ( DAG ), inositol-1,4,5-trifosfato ( IP3 ); PI3K también actúa sobre PIP2, fosforilándolo para producir fosfatidlyinositol-3,4,5-trifosfato (PIP3). DAG se une y activa algunas PKC. Lo más importante en las células T es la PKC-θ, fundamental para activar los factores de transcripción NF-κB y AP-1. IP3 se libera de la membrana mediante PLC-γ y se difunde rápidamente para activar los receptores de los canales de calcio en el RE , lo que induce la liberación de calcio en el citosol. El nivel bajo de calcio en el retículo endoplásmico provoca la acumulación de STIM1 en la membrana del RE y conduce a la activación de los canales CRAC de la membrana celular que permiten que fluya calcio adicional hacia el citosol desde el espacio extracelular. Este calcio citosólico agregado se une a la calmodulina, que luego puede activar la calcineurina . La calcineurina, a su vez, activa NFAT , que luego se traslada al núcleo. NFAT es un factor de transcripción que activa la transcripción de un conjunto pleiotrópico de genes, el más notable, IL-2, una citocina que promueve la proliferación a largo plazo de células T activadas.
PLC-γ también puede iniciar la vía NF-κB . DAG activa PKC-θ, que luego fosforila CARMA1, lo que hace que se despliegue y funcione como un andamio. Los dominios citosólicos se unen a un adaptador BCL10 a través de dominios CARD (dominios de activación y reclutamiento de caspasas); que luego se une a TRAF6, que está ubiquitinado en K63. : 513–523 [49] Esta forma de ubiquitinación no conduce a la degradación de las proteínas diana. Más bien, sirve para reclutar NEMO, IKKα y -β, y TAB1-2/TAK1. [50] TAK 1 fosforila IKK-β, que luego fosforila IκB permitiendo la ubiquitinación de K48: conduce a la degradación proteasomal. Luego, Rel A y p50 pueden ingresar al núcleo y unirse al elemento de respuesta NF-κB. Esto, junto con la señalización NFAT, permite la activación completa del gen IL-2. [49]
Si bien en la mayoría de los casos la activación depende del reconocimiento del antígeno por parte del TCR, se han descrito vías alternativas para la activación. Por ejemplo, se ha demostrado que las células T citotóxicas se activan cuando son atacadas por otras células T CD8, lo que conduce a la tolerización de estas últimas. [51]
En la primavera de 2014, el experimento de Activación de Células T en el Espacio (TCAS) se lanzó a la Estación Espacial Internacional en la misión SpaceX CRS-3 para estudiar cómo "las deficiencias en el sistema inmunológico humano se ven afectadas por un entorno de microgravedad". [52]
La activación de las células T está modulada por especies reactivas de oxígeno . [53]
Una característica única de las células T es su capacidad para discriminar entre células sanas y anormales (por ejemplo, infectadas o cancerosas) en el cuerpo. [54] Las células sanas normalmente expresan una gran cantidad de pMHC propios en su superficie celular y, aunque el receptor del antígeno de las células T puede interactuar con al menos un subconjunto de estos pMHC propios, las células T generalmente ignoran estas células sanas. Sin embargo, cuando estas mismas células contienen incluso cantidades mínimas de pMHC derivado de patógenos, las células T pueden activarse e iniciar respuestas inmunes. La capacidad de las células T de ignorar las células sanas pero responder cuando estas mismas células contienen pMHC derivado de patógenos (o cáncer) se conoce como discriminación de antígenos. Los mecanismos moleculares que subyacen a este proceso son controvertidos. [54] [55]
.jpg/440px-HIV-infected_T_cell_(6813384933).jpg)
Las causas de la deficiencia de células T incluyen linfocitopenia de las células T y/o defectos en la función de las células T individuales. La insuficiencia completa de la función de las células T puede deberse a afecciones hereditarias como la inmunodeficiencia combinada grave (SCID), el síndrome de Omenn y la hipoplasia cartílago-cabello . [56] Las causas de las insuficiencias parciales de la función de las células T incluyen el síndrome de inmunodeficiencia adquirida (SIDA) y afecciones hereditarias como el síndrome de DiGeorge (DGS), los síndromes de rotura cromosómica (CBS) y los trastornos combinados de células B y T como la ataxia. telangiectasia (AT) y síndrome de Wiskott-Aldrich (WAS). [56]
Los principales patógenos que preocupan en las deficiencias de células T son los patógenos intracelulares , incluidos el virus del herpes simple , Mycobacterium y Listeria . [57] Además, las infecciones por hongos también son más comunes y graves en las deficiencias de células T. [57]
El cáncer de células T se denomina linfoma de células T y representa quizás uno de cada diez casos de linfoma no Hodgkin . [58] Las principales formas de linfoma de células T son:
El agotamiento de las células T es un término mal definido o ambiguo. [59] [60] Hay tres enfoques para su definición. [59] "El primer enfoque define principalmente como agotadas las células que presentan la misma disfunción celular (típicamente, la ausencia de una respuesta efectora esperada). El segundo enfoque define principalmente como agotadas las células que se producen por una causa determinada (típicamente, (pero no necesariamente, la exposición crónica a un antígeno). Finalmente, el tercer enfoque define principalmente como agotadas las células que presentan los mismos marcadores moleculares (típicamente, la proteína de muerte celular programada 1 [PD-1])". [59]
Las células T disfuncionales se caracterizan por una pérdida progresiva de función, cambios en los perfiles transcripcionales y expresión sostenida de receptores inhibidores. Al principio, las células pierden su capacidad de producir IL-2 y TNFα , lo que es seguido por la pérdida de una alta capacidad proliferativa y potencial citotóxico, y eventualmente conduce a su deleción. Las células T agotadas suelen indicar niveles más altos de CD43 , CD69 y receptores inhibidores combinados con una menor expresión de CD62L y CD127 . El agotamiento puede desarrollarse durante infecciones crónicas, sepsis y cáncer. [61] Las células T agotadas conservan su agotamiento funcional incluso después de una exposición repetida al antígeno. [62]
El agotamiento de las células T puede ser provocado por varios factores, como la exposición persistente al antígeno y la falta de ayuda de las células T CD4. [63] La exposición al antígeno también tiene efecto en el curso del agotamiento porque un tiempo de exposición más prolongado y una mayor carga viral aumentan la gravedad del agotamiento de las células T. Se necesitan al menos 2 a 4 semanas de exposición para establecer el agotamiento. [64] Otro factor capaz de inducir el agotamiento son los receptores inhibidores que incluyen la proteína de muerte celular programada 1 (PD1), CTLA-4 , la proteína de membrana de células T-3 (TIM3) y la proteína del gen 3 de activación de linfocitos (LAG3). [65] [66] Las moléculas solubles como las citoquinas IL-10 o TGF-β también pueden desencadenar el agotamiento. [67] [68] Los últimos factores conocidos que pueden desempeñar un papel en el agotamiento de las células T son las células reguladoras. Las células Treg pueden ser una fuente de IL-10 y TGF-β y, por tanto, pueden desempeñar un papel en el agotamiento de las células T. [69] Además, el agotamiento de las células T se revierte después del agotamiento de las células Treg y el bloqueo de PD1. [70] El agotamiento de las células T también puede ocurrir durante la sepsis como resultado de una tormenta de citoquinas. Más tarde, después del encuentro séptico inicial, las citoquinas antiinflamatorias y las proteínas proapoptóticas toman el control para proteger al cuerpo del daño. La sepsis también conlleva una alta carga de antígenos e inflamación. En esta etapa de la sepsis aumenta el agotamiento de las células T. [71] [72] Actualmente existen estudios que apuntan a utilizar bloqueos de receptores inhibidores en el tratamiento de la sepsis. [73] [74] [75]
Mientras que durante la infección se puede desarrollar el agotamiento de las células T después de una exposición persistente al antígeno después del trasplante de injerto, surge una situación similar con la presencia de aloantígeno. [76] Se demostró que la respuesta de las células T disminuye con el tiempo después del trasplante de riñón. [77] Estos datos sugieren que el agotamiento de las células T desempeña un papel importante en la tolerancia de un injerto, principalmente mediante el agotamiento de las células T CD8 alorreactivas. [72] [78] Varios estudios mostraron un efecto positivo de la infección crónica sobre la aceptación del injerto y su supervivencia a largo plazo mediada en parte por el agotamiento de las células T. [79] [80] [81] También se demostró que el agotamiento de las células T del receptor proporciona condiciones suficientes para la transferencia de células NK . [82] Si bien hay datos que muestran que la inducción del agotamiento de las células T puede ser beneficiosa para el trasplante, también conlleva desventajas, entre las que se pueden contar el mayor número de infecciones y el riesgo de desarrollo de tumores. [83]
Durante el cáncer, el agotamiento de las células T desempeña un papel en la protección del tumor. Según la investigación, algunas células asociadas al cáncer, así como las propias células tumorales, pueden inducir activamente el agotamiento de las células T en el sitio del tumor. [84] [85] [86] El agotamiento de las células T también puede desempeñar un papel en las recaídas del cáncer, como se demostró en el caso de la leucemia. [87] Algunos estudios han sugerido que es posible predecir la recaída de la leucemia basándose en la expresión de los receptores inhibidores PD-1 y TIM-3 por parte de las células T. [88] Muchos experimentos y ensayos clínicos se han centrado en bloqueadores de puntos de control inmunitarios en la terapia contra el cáncer, y algunos de ellos han sido aprobados como terapias válidas que ahora se encuentran en uso clínico. [89] Los receptores inhibidores a los que se dirigen esos procedimientos médicos son vitales en el agotamiento de las células T y bloquearlos puede revertir estos cambios. [90]
Las células T... derivan su [nombre] de los órganos en los que se desarrollan. Las células T se desarrollan [maduras] en el timo.