La coenzima A ( CoA , SHCoA , CoASH ) es una coenzima , notable por su papel en la síntesis y oxidación de ácidos grasos , y la oxidación del piruvato en el ciclo del ácido cítrico . Todos los genomas secuenciados hasta la fecha codifican enzimas que utilizan la coenzima A como sustrato , y alrededor del 4% de las enzimas celulares la utilizan (o un tioéster ) como sustrato. En humanos, la biosíntesis de CoA requiere cisteína , pantotenato (vitamina B 5 ) y trifosfato de adenosina (ATP). [2]
En su forma acetilada , la coenzima A es una molécula muy versátil que cumple funciones metabólicas tanto en la vía anabólica como en la catabólica . La acetil-CoA se utiliza en la regulación postraduccional y alostérica de la piruvato deshidrogenasa y la carboxilasa para mantener y apoyar la división de la síntesis y degradación del piruvato . [3]

La coenzima A fue identificada por Fritz Lipmann en 1946, [4] quien más tarde también le dio su nombre. Su estructura fue determinada a principios de la década de 1950 en el Instituto Lister , Londres, junto con Lipmann y otros trabajadores de la Facultad de Medicina de Harvard y el Hospital General de Massachusetts . [5] Lipmann inicialmente tenía la intención de estudiar la transferencia de acetilo en animales, y a partir de estos experimentos notó un factor único que no estaba presente en los extractos de enzimas pero que era evidente en todos los órganos de los animales. Pudo aislar y purificar el factor del hígado de cerdo y descubrió que su función estaba relacionada con una coenzima que era activa en la acetilación de la colina . [6] El trabajo con Beverly Guirard , Nathan Kaplan y otros determinó que el ácido pantoténico era un componente central de la coenzima A. [7] [8] La coenzima fue nombrada coenzima A para representar "activación del acetato". En 1953, Fritz Lipmann ganó el Premio Nobel de Fisiología o Medicina "por su descubrimiento de la coenzima A y su importancia para el metabolismo intermediario". [6] [9]
La coenzima A se sintetiza de forma natural a partir del pantotenato (vitamina B 5 ), que se encuentra en alimentos como la carne, las verduras, los cereales, las legumbres, los huevos y la leche. [10] En los seres humanos y en la mayoría de los organismos vivos, el pantotenato es una vitamina esencial que tiene diversas funciones. [11] En algunas plantas y bacterias, incluida la Escherichia coli , el pantotenato se puede sintetizar de novo y, por lo tanto, no se considera esencial. Estas bacterias sintetizan el pantotenato a partir del aminoácido aspartato y un metabolito en la biosíntesis de valina. [12]
En todos los organismos vivos, la coenzima A se sintetiza en un proceso de cinco pasos que requiere cuatro moléculas de ATP, pantotenato y cisteína [13] (ver figura):

Las abreviaturas de la nomenclatura de las enzimas entre paréntesis representan enzimas de mamíferos, otras enzimas eucariotas y procariotas respectivamente. En los mamíferos, los pasos 4 y 5 son catalizados por una enzima bifuncional llamada COASY . [14] Esta vía está regulada por la inhibición del producto. La CoA es un inhibidor competitivo de la pantotenato quinasa, que normalmente se une al ATP. [12] La coenzima A, tres ADP, un monofosfato y un difosfato se obtienen de la biosíntesis. [13]
La coenzima A se puede sintetizar a través de rutas alternativas cuando el nivel intracelular de coenzima A se reduce y la vía de novo se ve afectada. [15] En estas vías, la coenzima A debe obtenerse de una fuente externa, como los alimentos, para producir 4'-fosfopanteteína . Los pirofosfatos de ectonucleótidos (ENPP) degradan la coenzima A a 4'-fosfopanteteína, una molécula estable en los organismos. Las proteínas transportadoras de acilo (ACP) (como la sintasa de ACP y la degradación de ACP) también se utilizan para producir 4'-fosfopanteteína. Esta vía permite que la 4'-fosfopanteteína se reponga en la célula y permite la conversión a coenzima A a través de las enzimas PPAT y PPCK. [16]
Un artículo de 2024 [ cita requerida ] detalló un mecanismo de síntesis química plausible para el componente panteteína (la parte funcional principal) de la coenzima A en un mundo prebiótico primordial .
La coenzima A se produce comercialmente mediante extracción a partir de levadura, pero se trata de un proceso ineficiente (rinde aproximadamente 25 mg/kg) y el resultado es un producto caro. Se han investigado varias formas de producir CoA de forma sintética o semisintética, aunque actualmente ninguna funciona a escala industrial. [17]
Dado que la coenzima A es, en términos químicos, un tiol , puede reaccionar con ácidos carboxílicos para formar tioésteres , funcionando así como un transportador de grupos acilo . Ayuda a transferir ácidos grasos del citoplasma a las mitocondrias . Una molécula de coenzima A que porta un grupo acilo también se denomina acil-CoA . Cuando no está unida a un grupo acilo, se suele denominar "CoASH" o "HSCoA". Este proceso facilita la producción de ácidos grasos en las células, que son esenciales en la estructura de la membrana celular.
La coenzima A también es la fuente del grupo fosfopanteteína que se agrega como grupo prostético a proteínas como la proteína transportadora de acilo y la formiltetrahidrofolato deshidrogenasa . [18] [19]
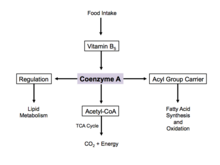
La coenzima A es una de las cinco coenzimas cruciales que son necesarias en el mecanismo de reacción del ciclo del ácido cítrico . Su forma acetil-coenzima A es el insumo principal en el ciclo del ácido cítrico y se obtiene de la glucólisis , el metabolismo de los aminoácidos y la betaoxidación de los ácidos grasos. Este proceso es la vía catabólica principal del cuerpo y es esencial para descomponer los componentes básicos de la célula, como los carbohidratos , los aminoácidos y los lípidos . [20]
Cuando hay un exceso de glucosa, la coenzima A se utiliza en el citosol para la síntesis de ácidos grasos. [21] Este proceso se lleva a cabo mediante la regulación de la acetil-CoA carboxilasa , que cataliza el paso comprometido en la síntesis de ácidos grasos. La insulina estimula la acetil-CoA carboxilasa, mientras que la epinefrina y el glucagón inhiben su actividad. [22]
Durante la inanición celular, se sintetiza la coenzima A, que transporta los ácidos grasos del citosol a las mitocondrias, donde se genera acetil-CoA para la oxidación y la producción de energía. [21] En el ciclo del ácido cítrico, la coenzima A actúa como regulador alostérico en la estimulación de la enzima piruvato deshidrogenasa .
El descubrimiento de la nueva función antioxidante de la coenzima A destaca su papel protector durante el estrés celular. Las células de mamíferos y bacterias sometidas a estrés oxidativo y metabólico muestran un aumento significativo en la modificación covalente de los residuos de cisteína de la proteína por la coenzima A. [23] [24] Esta modificación reversible se denomina CoAlación de proteínas (Proteína-S-SCoA), que desempeña un papel similar a la S -glutatión de la proteína al prevenir la oxidación irreversible del grupo tiol de los residuos de cisteína.
Utilizando el anticuerpo anti-coenzima A [25] y las metodologías de cromatografía líquida y espectrometría de masas en tándem ( LC-MS/MS ), se identificaron más de 2000 proteínas CoAlated de células bacterianas y de mamíferos estresadas. [26] La mayoría de estas proteínas están involucradas en el metabolismo celular y la respuesta al estrés. [26] Diferentes estudios de investigación se han centrado en descifrar la regulación de proteínas mediada por la coenzima A. Tras la CoAlación de proteínas, se ha informado de la inhibición de la actividad catalítica de diferentes proteínas (por ejemplo, el supresor de metástasis NME1 , la peroxirredoxina 5 , la GAPDH , entre otras). [27] [28] [24] [29] Para restaurar la actividad de la proteína, las enzimas antioxidantes que reducen el enlace disulfuro entre la coenzima A y el residuo de cisteína de la proteína desempeñan un papel importante. Este proceso se denomina deCoAlación de proteínas. Hasta el momento, se ha demostrado que dos proteínas bacterianas, la tiorredoxina A y la proteína similar a la tiorredoxina (YtpP), descodifican las proteínas. [30]
La coenzima A está disponible en varios proveedores químicos como ácido libre y sales de litio o sodio . El ácido libre de la coenzima A es detectablemente inestable, con una degradación de alrededor del 5% observada después de 6 meses cuando se almacena a −20 °C, [1] y una degradación casi completa después de 1 mes a 37 °C. [31] Las sales de litio y sodio de CoA son más estables, con una degradación insignificante observada durante varios meses a varias temperaturas. [32] Las soluciones acuosas de coenzima A son inestables por encima de pH 8, con un 31% de pérdida de actividad después de 24 horas a 25 °C y pH 8. Las soluciones madre de CoA son relativamente estables cuando se congelan a pH 2-6. La principal vía de pérdida de actividad de CoA es probablemente la oxidación del aire de CoA a disulfuros de CoA. Los disulfuros mixtos de CoA, como CoA- S – S -glutatión, son contaminantes comúnmente observados en preparaciones comerciales de CoA. [1] El CoA libre se puede regenerar a partir de disulfuro de CoA y disulfuros de CoA mixtos con agentes reductores como ditiotreitol o 2-mercaptoetanol .