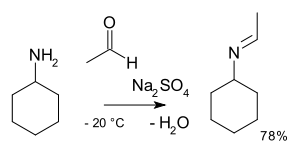
En química orgánica , la bisustitución de alquilimino-de-oxo es la reacción orgánica de compuestos carbonílicos con aminas para formar iminas . [2] El nombre de la reacción se basa en la Nomenclatura IUPAC para Transformaciones . La reacción está catalizada por ácido y el tipo de reacción es la adición nucleofílica de la amina al compuesto carbonílico seguida de la transferencia de un protón del nitrógeno al oxígeno para formar un hemiaminal o carbinolamina estable . Con aminas primarias, se pierde agua en una reacción de eliminación para formar una imina . Con aminas ariladas , se forman bases de Schiff especialmente estables .
Los pasos de reacción son reacciones reversibles y la reacción se completa mediante la eliminación del agua, por ejemplo, mediante destilación azeotrópica , tamices moleculares o tetracloruro de titanio . Las aminas primarias reaccionan a través de un intermediario hemiaminal inestable que luego separa el agua.
Las aminas secundarias no pierden agua fácilmente porque no tienen un protón disponible y, en cambio, a menudo reaccionan aún más con un aminal :
o cuando un protón α-carbonilo está presente en una enamina :
En ambiente ácido el producto de reacción es una sal de iminio por pérdida de agua.
Este tipo de reacción se encuentra en muchas preparaciones de heterociclos , por ejemplo, la reacción de Povarov y la síntesis de Friedländer de quinolinas .
Los compuestos que contienen tanto una amina primaria o secundaria como un grupo funcional carbonilo suelen ser lábiles. Esta directriz se aplica a los aminoaldehídos, aminocetonas y aminoésteres; de hecho, una molécula no puede llevar simultáneamente ( sin protección ) grupos aldehído y amina. La aminoacetona , la aminocetona más simple, no se puede aislar como líquido o sólido, [3] y el 2-aminobenzaldehído se oligomeriza en solución o en estado fundido. [4] Una α- formil aziridina , reducida con DIBAL a partir del éster , se dimeriza reversiblemente [Nota 1] a [Nota 2] una oxazolidina : [5]

Las hidrazinas y las hidroxilaminas desplazan los oxígenos carbonílicos mucho más fácilmente que las aminas. Sus equilibrios favorecen fuertemente al producto deshidratado y el carbonilo se recupera sólo con dificultad. [6]