La isoquinolina es una muestra química individual, un compuesto orgánico aromático heterocíclico , así como el nombre de una familia de muchos miles de alcaloides vegetales naturales, cualquiera de los cuales podría denominarse "isoquinolina". Es un isómero estructural de la quinolina . La isoquinolina y la quinolina son benzopiridinas , que están compuestas por un anillo de benceno fusionado a un anillo de piridina . En un sentido más amplio, el término isoquinolina se utiliza para hacer referencia a los derivados de isoquinolina . La 1-bencilisoquinolina es la columna vertebral estructural de muchos alcaloides naturales como la papaverina . El anillo de isoquinolina en estos compuestos naturales deriva del aminoácido aromático tirosina . [3] [4] [5] [6] [7] [8]
La isoquinolina es un líquido higroscópico incoloro a temperaturas superiores a su punto de fusión con un olor penetrante y desagradable . Las muestras impuras pueden tener un color marrón, como es típico de los heterociclos de nitrógeno. Cristaliza en forma de plaquetas que tienen baja solubilidad en agua pero se disuelven bien en etanol , acetona , éter dietílico , disulfuro de carbono y otros disolventes orgánicos comunes . También es soluble en ácidos diluidos como derivado protonado.
Al ser un análogo de la piridina, la isoquinolina es una base débil , con una p K a de 5,14. [2] Protona para formar sales tras el tratamiento con ácidos fuertes , como el HCl. Forma aductos con ácidos de Lewis , como el BF 3 .
La isoquinolina fue aislada por primera vez del alquitrán de hulla en 1885 por Hoogewerf y van Dorp. [9] Lo aislaron mediante cristalización fraccionada del sulfato ácido. Weissgerber desarrolló una ruta más rápida en 1914 mediante la extracción selectiva de alquitrán de hulla, aprovechando el hecho de que la isoquinolina es más básica que la quinolina. A continuación se puede aislar la isoquinolina de la mezcla mediante cristalización fraccionada del sulfato ácido.
Aunque los derivados de isoquinolina se pueden sintetizar mediante varios métodos, relativamente pocos métodos directos liberan la isoquinolina no sustituida. La reacción de Pomeranz-Fritsch proporciona un método eficaz para la preparación de isoquinolina. Esta reacción utiliza un dietil acetal de benzaldehído y aminoacetoaldehído, que en un medio ácido reaccionan para formar isoquinolina. [10] Alternativamente, se pueden usar bencilamina y un acetal de glioxal para producir el mismo resultado usando la modificación de Schlittler-Müller. [11]
Varios otros métodos son útiles para la preparación de diversos derivados de isoquinolina.
En la reacción de Bischler-Napieralski, una β-feniletilamina es acilada y ciclodeshidratada por un ácido de Lewis, como el cloruro de fosforilo o el pentóxido de fósforo . La 3,4-dihidroisoquinolina 1-sustituida resultante se puede deshidrogenar usando paladio. La siguiente reacción de Bischler-Napieralski produce papaverina.
La reacción de Pictet-Gams y la reacción de Pictet-Spengler son variaciones de la reacción de Bischler-Napieralski. Una reacción de Pictet-Gams funciona de manera similar a la reacción de Bischler-Napieralski; la única diferencia es que un grupo hidroxi adicional en el reactivo proporciona un sitio para la deshidratación en las mismas condiciones de reacción que la ciclación para dar la isoquinolina en lugar de requerir una reacción separada para convertir un intermedio de dihidroisoquinolina.
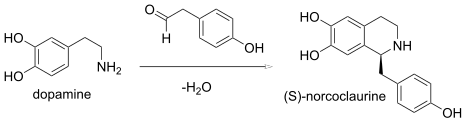
En una reacción de Pictet-Spengler, una condensación de una β- feniletilamina y un aldehído forma una imina, que sufre una ciclación para formar una tetrahidroisoquinolina en lugar de la dihidroisoquinolina. En enzimología , la (S) -norcoclaurina sintasa ( EC 4.2.1.78) es una enzima que cataliza una síntesis biológica de Pictect-Spengler:
Las reacciones intramoleculares de aza Wittig también producen isoquinolinas.
Las isoquinolinas encuentran muchas aplicaciones, entre ellas:
Se cree que la enfermedad de Parkinson , un trastorno del movimiento que progresa lentamente, es causada por ciertas neurotoxinas . En la década de 1980 se encontró una neurotoxina llamada MPTP (1[ N ]-metil-4-fenil-1,2,3,6- tetrahidropiridina ), precursora de MPP + , que se vinculó con la enfermedad de Parkinson. Las neurotoxinas activas destruyen las neuronas dopaminérgicas , lo que provoca parkinsonismo y enfermedad de Parkinson. Se ha descubierto que varios derivados de tetrahidroisoquinolina tienen las mismas propiedades neuroquímicas que el MPTP. Estos derivados pueden actuar como precursores de neurotoxinas activas. [13]
Las isoquinolinas se utilizan en la fabricación de tintes , pinturas , insecticidas y fungicidas . También se utiliza como disolvente para la extracción líquido-líquido de resinas y terpenos , y como inhibidor de la corrosión .
. Enciclopedia Británica . vol. 22 (11ª ed.). 1911, págs. 758–759.