Los anticuerpos humanizados son anticuerpos de especies no humanas cuyas secuencias de proteínas han sido modificadas para aumentar su similitud con las variantes de anticuerpos producidas naturalmente en humanos. [1] [2] El proceso de "humanización" se aplica generalmente a los anticuerpos monoclonales desarrollados para su administración a humanos (por ejemplo, anticuerpos desarrollados como medicamentos contra el cáncer). La humanización puede ser necesaria cuando el proceso de desarrollo de un anticuerpo específico implica la generación en un sistema inmunológico no humano (como el de los ratones). Las secuencias de proteínas de los anticuerpos producidos de esta manera son parcialmente distintas de los anticuerpos homólogos que se producen naturalmente en los humanos y, por lo tanto, son potencialmente inmunogénicos cuando se administran a pacientes humanos (véase también Anticuerpo humano antirratón ). Los nombres comunes internacionales de los anticuerpos humanizados terminan en -zumab , como en omalizumab (véase Nomenclatura de anticuerpos monoclonales ).
Los anticuerpos humanizados son distintos de los anticuerpos quiméricos . Estos últimos también tienen secuencias de proteínas más similares a las de los anticuerpos humanos, pero contienen una mayor cantidad de proteína no humana.
Existen otras formas de desarrollar anticuerpos monoclonales. Esta lista incluye muchos de los anticuerpos monoclonales desarrollados para su uso en seres humanos.
El proceso de humanización aprovecha el hecho de que la producción de anticuerpos monoclonales se puede lograr utilizando ADN recombinante para crear construcciones [3] capaces de expresarse en cultivos de células de mamíferos . Es decir, los segmentos de genes capaces de producir anticuerpos se aíslan y clonan en células que se pueden cultivar en un biorreactor de modo que las proteínas de anticuerpos producidas a partir del ADN de los genes clonados se pueden recolectar en masa . El paso que implica ADN recombinante proporciona un punto de intervención que se puede explotar fácilmente para alterar la secuencia de proteína del anticuerpo expresado. Por lo tanto, las alteraciones de la estructura del anticuerpo que se logran en el proceso de humanización se efectúan todas a través de técnicas a nivel de ADN. No todos los métodos para derivar anticuerpos destinados a la terapia humana requieren un paso de humanización (por ejemplo, visualización de fagos ), pero esencialmente todos dependen de técnicas que permiten de manera similar la "inserción" o "intercambio" de porciones de la molécula de anticuerpo.
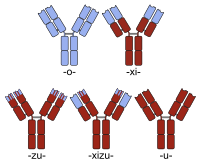
La humanización suele considerarse distinta de la creación de una quimera de anticuerpos de ratón y humano . Por lo tanto, aunque la creación de una quimera de anticuerpos normalmente se lleva a cabo para lograr un anticuerpo más parecido al humano (reemplazando la región constante del anticuerpo de ratón por la del humano), las quimeras simples de este tipo no suelen denominarse humanizadas. Más bien, la secuencia proteica de un anticuerpo humanizado es esencialmente idéntica a la de una variante humana, a pesar del origen no humano de algunos de sus segmentos de la región determinante de complementariedad (CDR) responsables de la capacidad del anticuerpo para unirse a su antígeno diana.
Los nombres de los anticuerpos quiméricos contienen la raíz -xi- . Entre los ejemplos de anticuerpos quiméricos aprobados para terapia humana se incluyen abciximab (ReoPro), basiliximab (Simulect), cetuximab (Erbitux), infliximab (Remicade) y rituximab (MabThera). También hay varios ejemplos de anticuerpos quiméricos actualmente en ensayos clínicos (por ejemplo, bavituximab ; consulte la lista ordenable para ver ejemplos adicionales).
El proceso de humanización también puede incluir la creación de una quimera de ratón y humano como paso inicial. En este caso, se empalma una región variable de ratón con una región constante humana. La quimera puede luego humanizarse aún más alterando selectivamente la secuencia de aminoácidos en la región variable de la molécula.
El proceso de alteración debe ser "selectivo" para conservar la especificidad para la que se desarrolló originalmente el anticuerpo. Es decir, dado que las porciones CDR de la región variable son esenciales para la capacidad del anticuerpo de unirse a su objetivo previsto, los aminoácidos de estas porciones no se pueden alterar sin el riesgo de socavar el propósito del desarrollo. Aparte de los segmentos CDR, las porciones de las regiones variables que difieren de las de los humanos se pueden corregir intercambiando los aminoácidos individuales adecuados. Esto se logra a nivel del ADN mediante mutagénesis .
La denominación de las quimeras humanizadas incluye la raíz de ambas designaciones ( -xi- + -zu- ). Otelixizumab es un ejemplo de una quimera humanizada que actualmente se encuentra en ensayos clínicos para el tratamiento de la artritis reumatoide y la diabetes mellitus . [4]
Es posible producir un anticuerpo humanizado sin crear un intermedio quimérico. La creación "directa" de un anticuerpo humanizado se puede lograr insertando los segmentos codificantes de CDR apropiados (los llamados "donantes", responsables de las propiedades de unión deseadas) en un "andamio" de anticuerpo humano (los llamados "aceptores"). Como se discutió anteriormente, esto se logra a través de métodos de ADN recombinante utilizando un vector apropiado [3] y expresión en células de mamífero. Es decir, después de que se desarrolla un anticuerpo para que tenga las propiedades deseadas en un ratón (u otro no humano), el ADN que codifica para ese anticuerpo se puede aislar, clonar en un vector y secuenciar (o el ADN se puede secuenciar directamente utilizando métodos de una sola célula). Luego se puede determinar la secuencia de ADN correspondiente a los CDR del anticuerpo. Una vez que se conoce la secuencia precisa de los CDR deseados, se puede idear una estrategia para insertar estas secuencias de manera apropiada en una construcción que contenga el ADN para una variante de anticuerpo humano. [5] [6] [7] [8] [9] La estrategia también puede emplear la síntesis de fragmentos de ADN lineales basados en la lectura de secuencias CDR. El proceso requiere un software de modelado informático para determinar cuáles de los aminoácidos del anticuerpo se pueden cambiar de secuencia murina a secuencia humana sin que los cambios comprometan la conformación del sitio de unión. En los Estados Unidos, este software fue desarrollado, patentado y demostrado por Protein Design Labs, Inc. en Mountain View, California, en los años 1980 y 1990. [10]
El alemtuzumab es un ejemplo temprano de un anticuerpo cuya humanización no incluyó un intermediario quimérico. En este caso, se desarrolló un anticuerpo monoclonal denominado "Campath-1" para unirse a CD52 utilizando un sistema de ratón. Luego se extrajeron los bucles hipervariables de Campath-1 (que contienen sus CDR y, por lo tanto, le confieren su capacidad para unirse a CD52) y se insertaron en un marco de anticuerpo humano. [1] El alemtuzumab está aprobado para el tratamiento de la leucemia linfocítica crónica de células B [11] y actualmente se encuentra en ensayos clínicos para una variedad de otras afecciones, incluida la esclerosis múltiple . [12]
Existen tecnologías que evitan por completo el uso de ratones u otros mamíferos no humanos en el proceso de descubrimiento de anticuerpos para terapias humanas. Ejemplos de tales sistemas incluyen varios métodos de "exhibición" (principalmente la exhibición de fagos ), así como métodos que aprovechan los niveles elevados de células B que se producen durante una respuesta inmune humana.
Estos sistemas emplean los principios selectivos de producción de anticuerpos específicos pero aprovechan microorganismos (como en la visualización de fagos ) o incluso extractos libres de células (como en la visualización de ribosomas ). Estos sistemas se basan en la creación de "bibliotecas" de genes de anticuerpos que pueden derivarse completamente de ARN humano aislado de sangre periférica . Los productos inmediatos de estos sistemas son fragmentos de anticuerpos, normalmente Fab o scFv .
Esto significa que, aunque los fragmentos de anticuerpos creados mediante métodos de visualización son de secuencia completamente humana, no son anticuerpos completos. Por lo tanto, se utilizan procesos en esencia idénticos a la humanización para incorporar y expresar las afinidades derivadas dentro de un anticuerpo completo.
Adalimumab (Humira) es un ejemplo de un anticuerpo aprobado para terapia humana que se creó a través de la visualización de fagos. [13] [14]
Es posible aprovechar la reacción inmunitaria humana para descubrir anticuerpos monoclonales. En pocas palabras, la respuesta inmunitaria humana funciona de la misma manera que la de un ratón o de otro mamífero no humano. Por lo tanto, las personas que experimentan un desafío a su sistema inmunitario, como una enfermedad infecciosa, un cáncer o una vacuna, son una fuente potencial de anticuerpos monoclonales dirigidos a ese desafío. Este enfoque parece especialmente adecuado para el desarrollo de terapias antivirales que aprovechen los principios de la inmunidad pasiva . Se han demostrado variantes de este enfoque en principio [15] y algunas están encontrando su camino hacia el desarrollo comercial. [16]