(2 S ,4 R )-4-Hidroxiprolina , o L- hidroxiprolina ( C 5 H 9 O 3 N ), es un aminoácido , abreviado como Hyp u O , por ejemplo , en Protein Data Bank .
En 1902, Hermann Emil Fischer aisló la hidroxiprolina a partir de gelatina hidrolizada . En 1905, Hermann Leuchs sintetizó una mezcla racémica de 4-hidroxiprolina. [1]
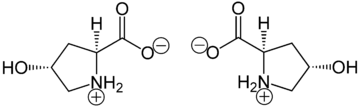
La hidroxiprolina se diferencia de la prolina por la presencia de un grupo hidroxilo (OH) unido al átomo de carbono gamma.
La hidroxiprolina se produce por hidroxilación del aminoácido prolina por la enzima prolil hidroxilasa después de la síntesis de proteínas (como una modificación postraduccional ). La reacción catalizada por enzimas tiene lugar en la luz del retículo endoplásmico . Aunque no se incorpora directamente a las proteínas, la hidroxiprolina comprende aproximadamente el 4% de todos los aminoácidos que se encuentran en el tejido animal, una cantidad mayor que otros siete aminoácidos que se incorporan de forma traduccional. [2]
La hidroxiprolina es un componente importante de la proteína colágeno , [3] que comprende aproximadamente el 13,5% del colágeno de los mamíferos. La hidroxiprolina y la prolina desempeñan funciones clave para la estabilidad del colágeno. [4] Permiten la torsión brusca de la hélice de colágeno. [5] En la tríada canónica de colágeno Xaa-Yaa-Gly (donde Xaa y Yaa son cualquier aminoácido), una prolina que ocupa la posición Yaa se hidroxila para dar una secuencia Xaa-Hyp-Gly. Esta modificación del residuo de prolina aumenta la estabilidad de la triple hélice de colágeno . Inicialmente se propuso que la estabilización se debía a que las moléculas de agua formaban una red de enlaces de hidrógeno que unía los grupos prolil hidroxilo y los grupos carbonilo de la cadena principal. [6] Posteriormente se demostró que el aumento de la estabilidad se debe principalmente a efectos estereoelectrónicos y que la hidratación de los residuos de hidroxiprolina proporciona poca o ninguna estabilidad adicional. [7]
La hidroxiprolina se encuentra en pocas proteínas además del colágeno. Por esta razón, el contenido de hidroxiprolina se ha utilizado como indicador para determinar la cantidad de colágeno y/o gelatina . Sin embargo, las proteínas de los mamíferos elastina y argonauta 2 tienen dominios similares al colágeno en los que se forma hidroxiprolina. Algunos venenos para caracoles, las conotoxinas , contienen hidroxiprolina, pero carecen de secuencias similares al colágeno. [2]
Se ha demostrado que la hidroxilación de prolina está involucrada en atacar la subunidad alfa del factor inducible por hipoxia (HIF) ( HIF-1 alfa ) para su degradación mediante proteólisis . En normoxia (condiciones normales de oxígeno), la proteína EGLN1 [1] hidroxila la prolina en la posición 564 de HIF-1 alfa, lo que permite la ubiquitilación por parte del supresor de tumores von Hippel-Lindau (pVHL) y la posterior orientación para la degradación del proteosoma . [8]
Las glicoproteínas ricas en hidroxiprolina (HRGP) también se encuentran en las paredes celulares de las plantas . [9] Estas hidroxiprolinas sirven como puntos de unión para cadenas de glicano que se agregan como modificaciones postraduccionales . [9]
La hidroxilación de prolina requiere ácido ascórbico ( vitamina C ). Los primeros efectos más evidentes (problemas gingivales y capilares) de la ausencia de ácido ascórbico en el ser humano provienen del defecto resultante en la hidroxilación de los residuos de prolina del colágeno , con una estabilidad reducida de la molécula de colágeno, provocando el escorbuto .
También se ha demostrado un aumento de los niveles séricos y urinarios de hidroxiprolina en la enfermedad de Paget . [10]
Otras hidroxiprolinas también existen en la naturaleza. Los más notables son 2,3- cis- , 3,4- trans- y 3,4-dihidroxiprolina, que se encuentran en las paredes celulares de las diatomeas [11] y se postula que desempeñan un papel en la deposición de sílice . La hidroxiprolina también se encuentra en las paredes de los oomicetos , protistas parecidos a hongos relacionados con las diatomeas. [12] (2 S , 4 S ) -cis - 4-hidroxiprolina se encuentra en los péptidos cíclicos tóxicos de los hongos Amanita ( por ejemplo , faloidina ). [13]
{{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )