La hepatotoxicidad (por toxicidad hepática ) implica daño hepático provocado por sustancias químicas . La lesión hepática inducida por fármacos es una causa de enfermedad hepática aguda y crónica causada específicamente por medicamentos y la razón más común por la que un fármaco se retira del mercado después de su aprobación.
El hígado desempeña un papel central en la transformación y eliminación de sustancias químicas y es susceptible a la toxicidad de estos agentes. Ciertos agentes medicinales, cuando se toman en sobredosis (por ejemplo, paracetamol ) y, a veces, incluso cuando se introducen dentro de rangos terapéuticos (por ejemplo, halotano ), pueden dañar el órgano. Otros agentes químicos, como los utilizados en laboratorios e industrias, productos químicos naturales (p. ej., microcistinas ) y remedios a base de hierbas (dos ejemplos destacados son la kava , de mecanismo desconocido, y la consuelda , por su contenido de alcaloide pirrolizidina) también pueden inducir hepatotoxicidad. Las sustancias químicas que causan daño hepático se llaman hepatotoxinas .
Más de 900 medicamentos han sido implicados en causar daño hepático [1] (ver LiverTox, enlace externo, a continuación) y es la razón más común por la que un medicamento se retira del mercado. La hepatotoxicidad y la lesión hepática inducida por fármacos también representan un número sustancial de fallos de los compuestos, lo que destaca la necesidad de modelos de predicción de la toxicidad (por ejemplo, DTI), [2] y ensayos de detección de fármacos, como células similares a hepatocitos derivadas de células madre , que son capaz de detectar la toxicidad en las primeras etapas del proceso de desarrollo del fármaco . [3] Los productos químicos a menudo causan lesiones subclínicas en el hígado, que se manifiestan únicamente como pruebas anormales de las enzimas hepáticas .
La lesión hepática inducida por fármacos es responsable del 5% de todos los ingresos hospitalarios y del 50% de todas las insuficiencias hepáticas agudas . [4] [5]
Las reacciones adversas a los medicamentos se clasifican en tipo A (intrínsecas o farmacológicas) o tipo B (idiosincrásicas). [6] La reacción a medicamentos de tipo A representa el 80% de todas las toxicidades. [7]
Los fármacos o toxinas que tienen hepatotoxicidad farmacológica (tipo A) son aquellos que tienen curvas dosis-respuesta predecibles (concentraciones más altas causan más daño hepático) y mecanismos de toxicidad bien caracterizados, como dañar directamente el tejido hepático o bloquear un proceso metabólico. Como en el caso de la sobredosis de paracetamol , este tipo de lesión se produce poco después de que se alcanza cierto umbral de toxicidad. El tetracloruro de carbono se utiliza habitualmente para inducir una lesión hepática aguda de tipo A en modelos animales.
La lesión idiosincrásica (tipo B) ocurre sin previo aviso, cuando los agentes causan hepatotoxicidad no predecible en individuos susceptibles, que no está relacionada con la dosis y tiene un período de latencia variable. [8] Este tipo de lesión no tiene una relación dosis-respuesta ni temporal clara y, en la mayoría de los casos, no cuenta con modelos predictivos. La hepatotoxicidad idiosincrásica ha llevado al retiro de varios medicamentos del mercado incluso después de pruebas clínicas rigurosas como parte del proceso de aprobación de la FDA; La troglitazona (Rezulin) [2] [9] y la trovafloxacina (Trovan) son dos ejemplos principales de hepatotoxinas idiosincrásicas extraídas del mercado.
La hierba kava ha causado varios casos de lesión hepática idiosincrásica, que van desde asintomáticas hasta fatales.
El uso oral del antimicótico ketoconazol se ha asociado con toxicidad hepática, incluidas algunas muertes; [10] sin embargo, tales efectos parecen limitarse a dosis tomadas durante un período superior a 7 días. [11]
El paracetamol , también conocido como acetaminofén y con las marcas Tylenol y Panadol, suele ser bien tolerado en la dosis prescrita, pero la sobredosis es la causa más común de enfermedad hepática inducida por fármacos e insuficiencia hepática aguda en todo el mundo. [12] El daño al hígado no se debe al fármaco en sí, sino a un metabolito tóxico ( N -acetil- p -benzoquinona imina (NAPQI)) producido por las enzimas del citocromo P-450 en el hígado. [13] En circunstancias normales, este metabolito se desintoxica mediante la conjugación con glutatión en la reacción de fase 2. En caso de sobredosis, se genera una gran cantidad de NAPQI, lo que anula el proceso de desintoxicación y provoca daño a las células hepáticas. El óxido nítrico también juega un papel en la inducción de toxicidad. [14] El riesgo de lesión hepática está influenciado por varios factores, incluida la dosis ingerida, la ingesta simultánea de alcohol u otras drogas, el intervalo entre la ingestión y el antídoto, etc. La dosis tóxica para el hígado varía bastante de persona a persona y a menudo se piensa que ser menor en alcohólicos crónicos. [15] [16] La medición del nivel en sangre es importante para evaluar el pronóstico; los niveles más altos predicen un peor pronóstico. La administración de acetilcisteína , un precursor del glutatión, puede limitar la gravedad del daño hepático al capturar el NAPQI tóxico. Aquellos que desarrollan insuficiencia hepática aguda aún pueden recuperarse espontáneamente, pero pueden requerir un trasplante si hay signos de mal pronóstico , como encefalopatía o coagulopatía (consulte los Criterios de King's College ). [17]
Aunque los analgésicos individuales rara vez inducen daño hepático debido a su uso generalizado, los AINE han surgido como un grupo importante de fármacos que exhiben hepatotoxicidad. Se han documentado reacciones idiosincrásicas y dependientes de la dosis. [18] La aspirina y la fenilbutazona están asociadas con hepatotoxicidad intrínseca; Se ha asociado una reacción idiosincrásica con ibuprofeno, sulindac, fenilbutazona, piroxicam, diclofenaco e indometacina.
Los glucocorticoides reciben este nombre debido a su efecto sobre el mecanismo de los carbohidratos. Promueven el almacenamiento de glucógeno en el hígado. El agrandamiento del hígado es un efecto secundario poco común del uso prolongado de esteroides en niños. [19] El efecto clásico del uso prolongado tanto en población adulta como pediátrica es la esteatosis . [20]
La isoniazida (INH) es uno de los fármacos más utilizados para la tuberculosis; se asocia con una elevación leve de las enzimas hepáticas en hasta el 20% de los pacientes y con hepatotoxicidad grave en el 1-2% de los pacientes. [21]
También hay casos en los que otros fármacos derivados de la hidracina , como el antidepresivo IMAO iproniazida , se asocian con daño hepático. [22] [23] La fenelzina se ha asociado con pruebas hepáticas anormales. [24] Los antibióticos pueden desarrollar efectos tóxicos. [25]

Los ejemplos incluyen hongos que contienen alfa-amanitina , kava y mohos productores de aflatoxinas. Los alcaloides de pirrolizidina , que se encuentran en algunas plantas, pueden ser tóxicos. [26] [27] El extracto de té verde es una causa creciente de insuficiencia hepática debido a su inclusión en más productos. [28] [29] [30]
Los ejemplos incluyen: fruta de ackee , bajiaolian , alcanfor , copaltra, cicasina , garcinia , [31] hojas de kava , alcaloides de pirrolizidina , hojas de castaño de indias , valeriana , consuelda . [32] [33] Remedios herbales chinos: Jin Bu Huan, Efedra , Shou Wu Pian , Bai Xian Pi . [34] [35]
Los ejemplos incluyen arsénico , tetracloruro de carbono y cloruro de vinilo . [36]
Se siguen retirando medicamentos del mercado debido al descubrimiento tardío de hepatotoxicidad. Debido a su metabolismo único y su estrecha relación con el tracto gastrointestinal , el hígado es susceptible a sufrir daños por fármacos y otras sustancias. El 75% de la sangre que llega al hígado llega directamente desde los órganos gastrointestinales y el bazo a través de las venas porta , que transportan fármacos y xenobióticos casi sin diluir. Varios mecanismos son responsables de inducir daño hepático o empeorar el proceso de daño.
Muchas sustancias químicas dañan las mitocondrias , un orgánulo intracelular que produce energía. Su disfunción libera una cantidad excesiva de oxidantes que, a su vez, dañan las células hepáticas. La activación de algunas enzimas en el sistema del citocromo P-450, como CYP2E1, también provoca estrés oxidativo. [37] La lesión de los hepatocitos y las células de los conductos biliares provoca la acumulación de ácidos biliares dentro del hígado . Esto promueve un mayor daño hepático. [38] Las células no parenquimatosas como las células de Kupffer , las células estrelladas productoras de colágeno y los leucocitos (es decir, neutrófilos y monocitos ) también desempeñan un papel en el mecanismo.
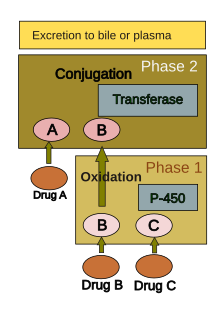
El cuerpo humano somete la mayoría de los compuestos, pero no todos, a diversos procesos químicos (es decir, metabolismo ) para hacerlos aptos para la eliminación. Esto implica transformaciones químicas para (a) reducir la solubilidad de las grasas y (b) cambiar la actividad biológica. Aunque casi todos los tejidos del cuerpo tienen cierta capacidad para metabolizar sustancias químicas, el retículo endoplásmico liso del hígado es el principal "centro de compensación metabólico" tanto para sustancias químicas endógenas (p. ej., colesterol, hormonas esteroides, ácidos grasos, proteínas) como para sustancias exógenas (p. ej., colesterol , hormonas esteroides, ácidos grasos , proteínas ). , drogas, alcohol). [39] El papel central que desempeña el hígado en la eliminación y transformación de sustancias químicas lo hace susceptible a lesiones inducidas por fármacos.
El metabolismo de los fármacos suele dividirse en dos fases: fase 1 y fase 2 . La reacción de la fase 1 generalmente sirve para preparar un fármaco para la fase 2. Sin embargo, muchos compuestos pueden metabolizarse directamente en la fase 2 o excretarse sin que se produzca ninguna reacción de la fase 2. La reacción de la fase 1 implica oxidación , reducción , hidrólisis , hidratación y muchas otras reacciones químicas raras. Estos procesos tienden a aumentar la solubilidad en agua del fármaco y pueden generar metabolitos que son químicamente más activos y/o potencialmente tóxicos. La mayoría de las reacciones de la fase 2 tienen lugar en el citosol e implican la conjugación con compuestos endógenos mediante enzimas transferasas . La fase 1 suele ser más adecuada para la eliminación.
Un grupo de enzimas ubicadas en el retículo endoplásmico, conocido como citocromo P-450 , es la familia más importante de enzimas metabolizadoras en el hígado. El citocromo P-450 no es una única enzima, sino que consta de una familia estrechamente relacionada de 50 isoformas ; seis de ellos metabolizan el 90% de los fármacos. [40] [41] Existe una enorme diversidad de productos individuales del gen P-450, y esta heterogeneidad permite que el hígado realice la oxidación de una amplia gama de sustancias químicas (incluida la mayoría de los medicamentos) en la fase 1. Tres características importantes del gen P-450 El sistema 450 tiene funciones en la toxicidad inducida por fármacos:
Cada una de las proteínas P-450 es única y explica (hasta cierto punto) la variación en el metabolismo de los fármacos entre individuos. Se deben considerar las variaciones genéticas ( polimorfismo ) en el metabolismo del P-450 cuando los pacientes presentan una sensibilidad o resistencia inusual a los efectos del fármaco en dosis normales. Este polimorfismo también es responsable de la respuesta variable a los medicamentos entre pacientes de diferentes orígenes étnicos.
Muchas sustancias pueden influir en el mecanismo de la enzima P-450. Los medicamentos interactúan con la familia de enzimas de varias maneras. [44] Los fármacos que modifican la enzima citocromo P-450 se denominan inhibidores o inductores. Los inhibidores de enzimas bloquean la actividad metabólica de una o varias enzimas P-450. Este efecto suele producirse de forma inmediata. Por otro lado, los inductores aumentan la actividad de P-450 aumentando la producción de enzimas o, en el caso de CYP2E1, impidiendo la degradación en el proteosoma . Generalmente hay un retraso antes de que aumente la actividad enzimática. [41]
Algunos fármacos pueden compartir la misma especificidad de P-450 y, por tanto, bloquear competitivamente su biotransformación. Esto puede conducir a la acumulación de fármacos metabolizados por la enzima. Este tipo de interacción farmacológica también puede reducir la tasa de generación de metabolitos tóxicos.
Los productos químicos producen una amplia variedad de lesiones hepáticas clínicas y patológicas . Los marcadores bioquímicos (p. ej., alanina transferasa , fosfatasa alcalina y bilirrubina ) se utilizan a menudo para indicar daño hepático. La lesión hepática se define como un aumento de (a) el nivel de ALT más de tres veces el límite superior normal (LSN), (b) el nivel de ALP más de dos veces el LSN, o (c) el nivel de bilirrubina total más de dos veces el LSN cuando está asociado con aumento de ALT o ALP. [45] [46] El daño hepático se caracteriza además en tipos hepatocelular (predominantemente elevación inicial de alanina transferasa ) y colestásico (aumento inicial de fosfatasa alcalina). Sin embargo, no son mutuamente excluyentes y a menudo se encuentran tipos mixtos de lesiones.
A continuación se analizan los patrones histopatológicos específicos de lesión hepática por daño inducido por fármacos.
Este es el tipo más común de necrosis de las células hepáticas inducida por fármacos , en el que la lesión se limita en gran medida a una zona particular del lóbulo hepático . Puede manifestarse como un nivel muy alto de ALT y una alteración grave de la función hepática que conduce a una insuficiencia hepática aguda .
En este patrón, la necrosis hepatocelular se asocia con infiltración de células inflamatorias. Puede haber tres tipos de hepatitis inducida por fármacos. (A) la hepatitis viral es la más común, donde las características histológicas son similares a las de la hepatitis viral aguda. (B) en la hepatitis focal o inespecífica, la infiltración linfocítica puede acompañarse de focos dispersos de necrosis celular . (C) la hepatitis crónica es muy similar a la hepatitis autoinmune desde el punto de vista clínico, serológico e histológico.
La lesión hepática provoca alteración del flujo de bilis y en los casos predominan el prurito y la ictericia. La histología puede mostrar inflamación (hepatitis colestásica) o puede ser suave (sin inflamación parenquimatosa ). En raras ocasiones, puede producir características similares a la cirrosis biliar primaria debido a la destrucción progresiva de los pequeños conductos biliares ( síndrome del conducto evanescente ).
La hepatotoxicidad puede manifestarse como acumulación de triglicéridos, lo que da lugar a hígado graso en gotas pequeñas (microvesicular) o en gotas grandes (macrovesicular). Existe un tipo separado de esteatosis por el cual la acumulación de fosfolípidos conduce a un patrón similar a las enfermedades con defectos hereditarios del metabolismo de los fosfolípidos (p. ej., enfermedad de Tay-Sachs ).
Los granulomas hepáticos inducidos por fármacos suelen asociarse con granulomas en otros tejidos y los pacientes suelen presentar características de vasculitis sistémica e hipersensibilidad. Más de 50 drogas han estado implicadas.
Estos resultan de una lesión del endotelio vascular.
Se han descrito neoplasias con exposición prolongada a algunos medicamentos o toxinas. Los más habituales son el carcinoma hepatocelular, el angiosarcoma y los adenomas hepáticos.

Esto sigue siendo un desafío en la práctica clínica debido a la falta de marcadores confiables. [47] Muchas otras condiciones conducen a cuadros clínicos y patológicos similares. Para diagnosticar la hepatotoxicidad, se debe establecer una relación causal entre el uso de la toxina o fármaco y el daño hepático posterior, pero puede resultar difícil, especialmente cuando se sospecha una reacción idiosincrásica. [48] El uso simultáneo de múltiples medicamentos puede aumentar la complejidad. Al igual que en la toxicidad del paracetamol, la hepatotoxicidad farmacológica bien establecida, dependiente de la dosis, es más fácil de detectar. Se han propuesto varias escalas clínicas, como la escala CIOMS /RUCAM y los criterios de María y Victorino, para establecer una relación causal entre el fármaco nocivo y el daño hepático. La escala CIOMS/RUCAM implica un sistema de puntuación que clasifica la sospecha en "definitiva o altamente probable" (puntuación > 8), "probable" (puntuación 6-8), "posible" (puntuación 3-5), "improbable" (puntuación 1–2) y "excluido" (puntuación ≤ 0). En la práctica clínica, los médicos ponen más énfasis en la presencia o ausencia de similitud entre el perfil bioquímico del paciente y el perfil bioquímico conocido de la toxicidad sospechada (p. ej., daño colestásico en amoxicilina-ácido clauvónico ). [47]
En la mayoría de los casos, la función hepática volverá a la normalidad si se suspende temprano el fármaco causante. Además, el paciente puede necesitar tratamiento de apoyo. Sin embargo, en la toxicidad por paracetamol , la agresión inicial puede ser fatal. La insuficiencia hepática fulminante por hepatotoxicidad inducida por fármacos puede requerir un trasplante de hígado. En el pasado se habían utilizado glucocorticoides en cuadros alérgicos y ácido ursodesoxicólico en casos colestásicos, pero no existe buena evidencia que respalde su eficacia. [ cita necesaria ]
Una elevación del nivel de bilirrubina sérica de más de 2 veces el LSN con aumento asociado de transaminasas es un signo ominoso. Esto indica hepatotoxicidad grave y es probable que provoque la mortalidad en entre el 10% y el 15% de los pacientes, especialmente si no se suspende el fármaco causante ( Ley de Hy ). [49] [50] Esto se debe a que se requiere un daño significativo al hígado para alterar la excreción de bilirrubina, por lo que una alteración menor (en ausencia de obstrucción biliar o síndrome de Gilbert ) no provocaría ictericia. Otros malos predictores del resultado son la vejez, el sexo femenino y la AST elevada . [51] [52]
Los siguientes fármacos terapéuticos fueron retirados del mercado principalmente debido a hepatotoxicidad: troglitazona , bromfenaco , trovafloxacino , ebrotidina , nimesulida , nefazodona , ximelagatrán y pemolina . [47] [53] [54]