Una hemicelulosa (también conocida como poliosa ) es uno de varios heteropolímeros (polisacáridos de la matriz), como los arabinoxilanos , presentes junto con la celulosa en casi todas las paredes celulares de las plantas terrestres . [1] La celulosa es cristalina, fuerte y resistente a la hidrólisis . Las hemicelulosas son ramificadas, más cortas que la celulosa y también muestran una propensión a cristalizar. [2] Pueden hidrolizarse mediante ácido o base diluidos, así como mediante una gran variedad de enzimas hemicelulasas .
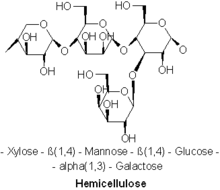
Se conocen diversos tipos de hemicelulosas. Algunos ejemplos importantes son el xilano , el glucuronoxilano , el arabinoxilano , el glucomanano y el xiloglucano .
Las hemicelulosas son polisacáridos que se asocian a menudo con la celulosa , pero con composiciones y estructuras distintas. Mientras que la celulosa se deriva exclusivamente de la glucosa , las hemicelulosas se componen de diversos azúcares y pueden incluir los azúcares de cinco carbonos xilosa y arabinosa , los azúcares de seis carbonos glucosa, manosa y galactosa , y el azúcar desoxirribonucleico de seis carbonos ramnosa . Las hemicelulosas contienen la mayoría de los azúcares D- pentosa y, ocasionalmente, también pequeñas cantidades de azúcares L. La xilosa es en la mayoría de los casos el monómero de azúcar presente en mayor cantidad, aunque en las maderas blandas la manosa puede ser el azúcar más abundante. No solo se pueden encontrar azúcares regulares en la hemicelulosa, sino también sus formas acidificadas, por ejemplo, el ácido glucurónico y el ácido galacturónico . [3] [4]
A diferencia de la celulosa, las hemicelulosas están formadas por cadenas más cortas (500 a 3000 unidades de azúcar). Por el contrario, cada polímero de celulosa comprende entre 7000 y 15 000 moléculas de glucosa. [5] Además, las hemicelulosas pueden ser polímeros ramificados , mientras que la celulosa no lo es. Las hemicelulosas están incrustadas en las paredes celulares de las plantas, a veces en cadenas que forman una " base ": se unen con pectina a la celulosa para formar una red de fibras reticuladas. [ cita requerida ]

En función de las diferencias estructurales, como los enlaces de la cadena principal y los grupos laterales, así como otros factores, como la abundancia y la distribución en las plantas, las hemicelulosas se pueden clasificar en cuatro grupos como sigue: [4] 1) xilanos, 2) mananos ; 3) β-glucanos de enlace mixto ; 4) xiloglucanos.
Los xilanos suelen estar formados por una cadena principal de residuos de xilosa unidos por enlaces β-(1→4) y pueden dividirse en homoxilanos y heteroxilanos. Los homoxilanos tienen una cadena principal de residuos de D-xilopiranosa unidos por enlaces glucosídicos β(1→4). Los homoxilanos tienen principalmente funciones estructurales. Los heteroxilanos, como los glucuronoxilanos, los glucuronoarabinoxilanos y los heteroxilanos complejos, tienen una cadena principal de D-xilopiranosa y ramificaciones cortas de carbohidratos. Por ejemplo, el glucuronoxilano tiene una sustitución con residuos de glucuronosilo y 4-O-metil glucuronosilo unidos por enlaces α-(1→2). Los arabinoxilanos y los glucuronoarabinoxilanos contienen residuos de arabinosa unidos a la cadena principal [6]
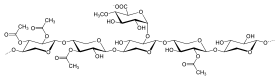
La hemicelulosa de tipo manano se puede clasificar en dos tipos según la diferencia entre sus cadenas principales: galactomananos y glucomananos. Los galactomananos tienen solo residuos de D-manopiranosa unidos por enlaces β-(1→4) en cadenas lineales. Los glucomananos constan de residuos de D-manopiranosa unidos por enlaces β-(1→4) y residuos de D-glucopiranosa unidos por enlaces β-(1→4) en las cadenas principales. En cuanto a las cadenas laterales, los residuos de D-galactopiranosa tienden a estar unidos por enlaces 6 a ambos tipos como cadenas laterales individuales con cantidades variables. [1]
La conformación de las cadenas de glucanos de enlace mixto contiene generalmente bloques de β-(1→4) D-glucopiranosa separados por una única β-(1→3) D-glucopiranosa. La población de β-(1→4) y β-(1→3) es de alrededor del 70% y 30% respectivamente. Estos glucanos consisten principalmente en segmentos de celotrioxilo (C 18 H 32 O 16 ) y celotraosilo (C 24 H 42 O 21 ) en orden aleatorio. Hay algunos estudios que muestran la relación molar de celotrioxilo/celotraosilo para la avena (2,1-2,4), la cebada (2,8-3,3) y el trigo (4,2-4,5). [1] [5]

Los xiloglucanos tienen una estructura similar a la celulosa con residuos de α-D-xilopiranosa en la posición 6. Para describir mejor las diferentes cadenas laterales, se utiliza una notación de código de una sola letra para cada tipo de cadena lateral. G: residuo de Glc no ramificado; X: α-d-Xyl-(1→6)-Glc. L: β-Gal, S: α-l-Araf, F: α-l-Fuc. Estas son las cadenas laterales más comunes. [5]
Los dos tipos más comunes de xiloglucanos en las paredes celulares de las plantas se identifican como XXXG y XXGG. [1]
Las hemicelulosas se sintetizan a partir de nucleótidos de azúcar en el aparato de Golgi de la célula . [8] Dos modelos explican su síntesis: 1) un "modelo de 2 componentes" donde la modificación ocurre en dos proteínas transmembrana, y 2) un "modelo de 1 componente" donde la modificación ocurre solo en una proteína transmembrana. Después de la síntesis, las hemicelulosas son transportadas a la membrana plasmática a través de vesículas de Golgi.
Cada tipo de hemicelulosa es biosintetizada por enzimas especializadas. [8] [9]
Las cadenas principales de mananos son sintetizadas por la familia de proteínas similares a la celulosa sintasa A (CSLA) y posiblemente por enzimas de la familia de proteínas similares a la celulosa sintasa D (CSLD). [8] [9] La manano sintasa, una enzima particular de la CSLA, es responsable de la adición de unidades de manosa a la cadena principal. [8] [9] Las cadenas laterales de galactosa de algunos mananos son añadidas por la galactomanano galactosiltransferasa. [8] [9] La acetilación de mananos está mediada por una manano O-acetiltransferasa, sin embargo, esta enzima no ha sido identificada definitivamente. [9]
La síntesis de la cadena principal del xiloglucano está mediada por la familia de proteínas similares a la celulosa sintasa C (CSLC), particularmente la glucano sintasa , que agrega unidades de glucosa a la cadena. [8] [9] La síntesis de la cadena principal del xiloglucano también está mediada de alguna manera por la xilosiltransferasa , pero este mecanismo es independiente de su función de transferasa y sigue sin estar claro. [9] Sin embargo, la xilosiltransferasa en su función de transferasa se utiliza para la adición de xilosa a la cadena lateral. [8] [9] Otras enzimas utilizadas para la síntesis de la cadena lateral del xiloglucano incluyen la galactosiltransferasa (que es responsable de la adición de [galactosa y de la cual se utilizan dos formas diferentes), la fucosiltransferasa (que es responsable de la adición de fucosa) y la acetiltransferasa (que es responsable de la acetilación). [8] [9]
La síntesis de la cadena principal de xilano, a diferencia de la de otras hemicelulosas, no está mediada por ninguna proteína similar a la celulosa sintasa. [9] En cambio, la xilano sintasa es responsable de la síntesis de la cadena principal, facilitando la adición de xilosa. [9] Se han identificado varios genes para las xilano sintasas. [9] Se utilizan varias otras enzimas para la adición y modificación de las unidades de cadena lateral de xilano, incluyendo la glucuronosiltransferasa (que agrega [unidades de ácido glucurónico), la xilosiltransferasa (que agrega unidades de xilosa adicionales), la arabinosiltransferasa (que agrega arabinosa), la metiltransferasa (responsable de la metilación ) y la acetiltransferasa (responsable de la acetilación). [9] Dado que el glucano de enlace mixto es un homopolímero no ramificado de glucosa, no hay síntesis de cadena lateral, solo la adición de glucosa a la cadena principal en dos enlaces, β1-3 y β1-4. [9] La síntesis de la cadena principal está mediada por enzimas en las familias de proteínas similares a la celulosa sintasa F y H (CSLF y CSLH), específicamente la glucano sintasa. [8] [9] Se han identificado varias formas de glucano sintasa de CSLF y CSLH. [8] [9] Todas ellas son responsables de la adición de glucosa a la cadena principal y todas son capaces de producir enlaces β1-3 y β1-4, sin embargo, se desconoce cuánto contribuye cada enzima específica a la distribución de los enlaces β1-3 y β1-4. [8] [9]
En el proceso de pulpa al sulfito, la hemicelulosa se hidroliza en gran medida por el licor ácido de pulpa y termina en el licor marrón, donde los azúcares hexosos fermentables (alrededor del 2 %) se pueden utilizar para producir etanol . Este proceso se aplicó principalmente a los licores marrones de sulfito de calcio. [10]
Los arabinogalactanos se pueden utilizar como emulsionantes , estabilizadores y aglutinantes de acuerdo con la Ley Federal de Alimentos, Medicamentos y Cosméticos. Los arabinogalactanos también se pueden utilizar como agente aglutinante en edulcorantes . [11]
Las películas a base de xilano muestran una baja permeabilidad al oxígeno y, por lo tanto, son de interés potencial como embalaje para productos sensibles al oxígeno. [12]
El agar se utiliza para elaborar gelatinas y pudines. También es un medio de crecimiento con otros nutrientes para microorganismos . [13]
El curdlan se puede utilizar como sustituto de grasas para producir alimentos dietéticos que mantengan el sabor y la sensación en boca de los productos que contienen grasas reales. [13]
Los betaglucanos tienen un papel importante en los complementos alimenticios y también son prometedores en cuestiones relacionadas con la salud, especialmente en las reacciones inmunes y el tratamiento del cáncer. [14]
La goma xantana, junto con otros polisacáridos, puede formar geles con una alta viscosidad en solución que se pueden utilizar en la industria petrolera para espesar el lodo de perforación. En la industria alimentaria, la goma xantana se utiliza en productos como aderezos y salsas. [15]
El alginato juega un papel importante en el desarrollo de textiles antimicrobianos debido a sus características de respeto al medio ambiente y su alto nivel de industrialización como biopolímero sostenible . [16]

Como un compuesto polisacárido en las paredes celulares de las plantas similar a la celulosa, la hemicelulosa ayuda a la celulosa en el fortalecimiento de las paredes celulares de las plantas. [6] La hemicelulosa interactúa con la celulosa proporcionando reticulación de las microfibrillas de celulosa : la hemicelulosa buscará huecos en la pared celular durante su formación y proporcionará soporte alrededor de las fibrillas de celulosa para dotar a la pared celular de la máxima resistencia posible que pueda proporcionar. [6] La hemicelulosa domina la lámina media de la célula vegetal, a diferencia de la celulosa que se encuentra principalmente en las capas secundarias. Esto permite que la hemicelulosa proporcione un soporte intermedio para la celulosa en las capas externas de la célula vegetal. En algunas paredes celulares, la hemicelulosa también interactuará con la lignina para proporcionar soporte de tejido estructural de plantas más vasculares. [3] [17]
Existen muchas formas de obtener hemicelulosa; todas ellas se basan en métodos de extracción a partir de árboles de madera dura o blanda molidos en muestras más pequeñas. En las maderas duras, el principal extracto de hemicelulosa es el glucuronoxilano (xilanos acetilados), mientras que el galactoglucomanano se encuentra en las maderas blandas. [18] [19] Antes de la extracción, la madera normalmente debe molerse en virutas de madera de diversos tamaños según el reactor utilizado. A continuación, se utiliza un proceso de extracción con agua caliente, también conocido como autohidrólisis o tratamiento hidrotérmico, con la adición de ácidos y bases para cambiar el tamaño y las propiedades del producto. [18] [19] La principal ventaja de la extracción con agua caliente es que ofrece un método en el que el único producto químico que se necesita es agua, lo que lo hace ecológico y económico. [20]
El objetivo del tratamiento con agua caliente es eliminar la mayor cantidad posible de hemicelulosa de la madera. Esto se hace a través de la hidrólisis de la hemicelulosa para lograr oligómeros más pequeños y xilosa. La xilosa, cuando se deshidrata, se convierte en furfural. [21] Cuando el objetivo es la xilosa y el furfural [ verificar ortografía ] , se agregan catalizadores ácidos, como el ácido fórmico, para aumentar la transición de polisacárido a monosacáridos. También se ha demostrado que este catalizador también utiliza un efecto disolvente para ayudar a la reacción. [21]
Un método de pretratamiento consiste en remojar la madera con ácidos diluidos (con concentraciones de alrededor del 4%). Esto convierte la hemicelulosa en monosacáridos. Cuando el pretratamiento se realiza con bases (por ejemplo, hidróxido de sodio o potasio), se destruye la estructura de la lignina. [19] Esto cambia la estructura de cristalina a amorfa. El pretratamiento hidrotérmico es otro método. [ Se necesita más explicación ] Este ofrece ventajas como que no se necesitan disolventes tóxicos o corrosivos, ni tampoco reactores especiales, y no hay costos adicionales para desechar productos químicos peligrosos. [18]
El proceso de extracción con agua caliente se realiza en reactores discontinuos, reactores semicontinuos o reactores continuos de pulpa. En los reactores discontinuos y semicontinuos, las muestras de madera se pueden utilizar en condiciones tales como astillas o pellets, mientras que un reactor de pulpa debe tener partículas tan pequeñas como 200 a 300 micrómetros. [19] Mientras que el tamaño de partícula disminuye, el rendimiento de producción también disminuye. [22] Esto se debe al aumento de celulosa. [ cita requerida ]
El proceso de agua caliente se realiza a una temperatura de entre 160 y 240 grados Celsius para mantener la fase líquida. Esto se hace por encima del punto de ebullición normal del agua para aumentar la solubilización de la hemicelulosa y la despolimerización de los polisacáridos. [21] Este proceso puede tardar varios minutos o varias horas dependiendo de la temperatura y el pH del sistema. [19] Las temperaturas más altas combinadas con tiempos de extracción más altos conducen a rendimientos más altos. Se obtiene un rendimiento máximo a un pH de 3,5. [18] Si es inferior, el rendimiento de la extracción disminuye exponencialmente. Para controlar el pH, generalmente se añade bicarbonato de sodio. [18] El bicarbonato de sodio inhibe la autólisis de los grupos acetilo, así como los enlaces de glicosilo. Dependiendo de la temperatura y el tiempo, la hemicelulosa se puede convertir aún más en oligómeros, monómeros y lignina. [18]
{{cite web}}: CS1 maint: varios nombres: lista de autores ( enlace ){{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )