La fotofarmacología es un campo multidisciplinario emergente que combina fotoquímica y farmacología . [1] Basado en la capacidad de la luz para cambiar la farmacocinética y la farmacodinamia de las moléculas bioactivas, su objetivo es regular la actividad de los fármacos in vivo mediante el uso de luz. [2] La modulación basada en la luz se logra incorporando fotointerruptores moleculares como azobenceno y diariletenos o fotojaulas como compuestos de o-nitrobencilo, cumarina y BODIPY en el farmacóforo. [3] Esta activación selectiva de las biomoléculas ayuda a prevenir o minimizar la actividad fuera del objetivo y los efectos secundarios sistémicos. Además, el hecho de que la luz sea el elemento regulador ofrece ventajas adicionales, como la capacidad de administrarse con una alta precisión espaciotemporal, una toxicidad baja o insignificante y la capacidad de controlarse tanto cualitativa como cuantitativamente ajustando su longitud de onda e intensidad. [4]
Aunque la fotofarmacología es un campo relativamente nuevo, el concepto de utilizar la luz en aplicaciones terapéuticas entró en práctica hace unas décadas. La terapia fotodinámica (PTD) es un protocolo bien establecido y practicado clínicamente en el que se utilizan fotosensibilizadores para producir oxígeno singlete para destruir células o tejidos enfermos o dañados. [2] La optogenética es otro método que se basa en la luz para controlar dinámicamente funciones biológicas, especialmente cerebrales y neuronales. [4] Aunque este enfoque ha demostrado ser útil como herramienta de investigación, su implementación clínica está limitada por el requisito de manipulación genética. Principalmente, estas dos técnicas sentaron las bases de la fotofarmacología. Hoy en día, es un campo en rápida evolución con diversas aplicaciones tanto en investigación básica como en medicina clínica que tiene el potencial de superar algunos de los desafíos que limitan la gama de aplicaciones de otras terapias guiadas por luz.
Figura 1. Representación esquemática del mecanismo de (a) fotofarmacología (b) terapia fotodinámica y (c) optogenética
El descubrimiento de fotorreceptores naturales como las rodopsinas en el ojo inspiró a la comunidad de investigación biomédica y farmacológica a diseñar proteínas sensibles a la luz para aplicaciones terapéuticas. [2] El desarrollo de moléculas sintéticas fotoconmutables es el hito más importante en la historia de los sistemas de suministro de luz. Los científicos continúan con sus esfuerzos para explorar nuevos fotointerruptores y estrategias de administración con un rendimiento mejorado para apuntar a diferentes moléculas biológicas, como canales iónicos, ácidos nucleicos y receptores enzimáticos. La investigación en fotofarmacología avanzó desde estudios in vitro a estudios in vivo en un período de tiempo significativamente corto, arrojando resultados prometedores en ambas formas. Se están realizando ensayos clínicos para evaluar más a fondo la seguridad y eficacia de estas terapias fotofarmacológicas y validar su potencial como enfoque innovador de administración de fármacos.
Los fotointerruptores moleculares se utilizan en el campo de la fotofarmacología, donde la energía de una molécula se puede controlar de forma reversible con luz para lograr una resolución espacial y temporal de un efecto particular. Los fotointerruptores pueden funcionar mediante fotoisomerización a través de la cual se usa luz para adaptar conformacionalmente una molécula a un sitio biológico, o mediante un efecto ambiental donde un factor externo, como un efecto solvente o un enlace de hidrógeno, puede permitir o apagar selectivamente un estado emisivo dentro de una molécula. Para visualizar procesos fotofísicos, una representación útil es el diagrama de Jablonski . Este es un diagrama que representa los niveles de energía electrónica y vibratoria dentro de una molécula como niveles verticales y muestra las posibles vías de relajación de los estados excitados. Normalmente, el estado fundamental se denomina S 0 y se dibuja en la parte inferior de la figura con excitaciones vibratorias cercanas justo encima. Una absorción promoverá un electrón al estado S 1 en cualquier nivel de energía vibratoria, o a un estado excitado de orden superior si la energía absorbida tiene suficiente magnitud. El estado excitado puede entonces sufrir una conversión interna, que es la relajación electrónica a un estado inferior con la misma energía vibratoria o relajación vibratoria dentro de un estado. Esto puede ir seguido de un cruce entre sistemas en el que el electrón sufre un cambio de espín o una desintegración radiativa o no radiativa de regreso al estado fundamental. [5]

Un ejemplo de un compuesto orgánico que sufre fotoisomerización es el azobenceno . La estructura son dos anillos de fenilo unidos con un doble enlace N = N y es el compuesto aril azo más simple. El azobenceno y sus derivados tienen dos bandas de absorbancia accesibles: el estado S 1 de una transición n-π* que puede excitarse usando luz azul, y el estado S 2 de una transición π-π* que puede excitarse usando luz ultravioleta. . [6] El azobenceno y sus derivados tienen dos isómeros, trans y cis. El isómero trans, que tiene los anillos de fenilo en lados opuestos del doble enlace azo, es el isómero térmicamente preferido ya que hay menos distorsión estereoelectrónica y más deslocalización presente. Sin embargo, la excitación del isómero trans al estado S 2 facilita un cambio al isómero cis. La absorción de S 1 está asociada con una conversión de nuevo al isómero trans. De esta manera, el azobenceno y sus derivados pueden actuar como reservas reversibles de energía manteniendo una configuración tensa en el isómero cis. Las modificaciones de los sustituyentes del azobenceno permiten ajustar la energía de estas absorciones y, si están diseñadas de manera que las dos bandas de absorción se superpongan, se puede utilizar una sola longitud de onda de luz para alternar entre ellas. Hay varios fotointerruptores similares que se isomerizan entre las configuraciones E y Z a través de un grupo azo (por ejemplo, azobenceno y azopirazol) o un puente de etileno (por ejemplo, estilbeno y hemitioíndigo). [7]
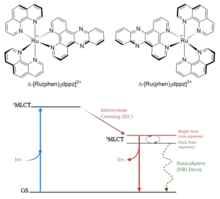
Alternativamente, los fotointerruptores pueden ser ellos mismos emisores y exhibir control ambiental sobre sus propiedades. Un ejemplo de ello es una clase de complejos de coordinación de rutenio y polipiridilo. Normalmente contienen dos ligandos bidentados de bipiridina o fenantrolina y un ligando bidentado extendido de fenantrolina-fenazina como la dipirido[3,2-a:2,3-c]fenazina (dppz). [8] Estos complejos tienen un estado excitado de transferencia de carga de metal a ligando ( 1 MLCT) que sufre un rápido cruce entre sistemas a un estado 3 MLCT debido al fuerte acoplamiento espín-órbita del centro de rutenio. Estos estados excitados se localizan en los nitrógenos de fenazina del ligando extendido y la emisión se produce desde el estado 3 MLCT. Las interacciones de los enlaces de hidrógeno, como la presencia de agua alrededor de estos átomos de nitrógeno, estabilizan el estado 3 MLCT, apagando el proceso de emisión. Por lo tanto, al controlar si está presente un disolvente polar acuoso o prótico, los comportamientos emisivo pueden "activarse/desactivarse" y se facilita la alternancia entre "estados brillantes" y "estados oscuros". Este comportamiento del interruptor de luz hace que estos y complejos similares sean de interés reciente en aplicaciones fotofarmacológicas como la terapia fotodinámica.
Como se mencionó anteriormente, la fotofarmacología se basa en el uso de fotointerruptores moleculares que se incorporan a la estructura de moléculas biológicamente activas, lo que permite controlar ópticamente su potencia. [7] Se introducen en la estructura de compuestos bioactivos mediante inserción, extensión o reemplazo bioisostérico. [7] Estas incorporaciones pueden estar respaldadas por consideraciones estructurales de la molécula o análisis SAR (relación estructura-actividad) para determinar la posición óptima. [7] Algunos ejemplos de moléculas fotoconmutables comúnmente utilizadas en fotofarmacología son los azobencenos, los diariletenos y las fotojaulas. [9]
Los azobencenos son una clase de moléculas fotoconmutables y se utilizan en aplicaciones fotofarmacológicas para su fotoisomerización reversible, como se describe en la sección anterior. Un ejemplo de una molécula fotoconmutable que utiliza azobenceno es el fototrexato. El fototrexato es un inhibidor de la dihidrofolato reductasa humana y es un análogo del metotrexato , un agente de quimioterapia. [10] Cuando está en su forma cis fotoactiva, se ha demostrado que el fototrexato es un potente antifolato y es relativamente inactivo cuando está en su forma trans. [10] La azologización, o incorporación de azobenceno, del metotrexato permite el control de la actividad citotóxica y se considera un paso adelante en el desarrollo de fármacos anticancerígenos dirigidos con eficacia localizada. [10]
Los fotointerruptores de diariletileno tienen reacciones de ciclación y cicloreversión reversibles que son fotoinducidas. [11] Son una clase de compuestos que tienen grupos funcionales aromáticos unidos a cada extremo de un doble enlace carbono-carbono. Un ejemplo de esta clase de molécula que se utiliza en fotofarmacología es el estilbeno . Bajo la influencia de la luz, el estilbeno cambia entre sus dos isómeros (E y Z).
Figura 4. Figura que muestra isomerizaciones de estilbeno bajo luz de E a Z
Se ha demostrado que los diariletenos tienen algunas ventajas sobre los interruptores de azobencenos más investigados, como la irreversibilidad térmica, la alta eficiencia de la fotoconmutación, la estabilidad celular favorable y la baja toxicidad. [11] Se ha demostrado que los diariletenos también son prometedores en otros campos además de la fotofarmacología. Estos campos incluyen el almacenamiento óptico de datos, los dispositivos optoelectrónicos, el autoensamblaje supramolecular y la lucha contra la falsificación. [11]
Una clase de sustancias conocidas como fotojaulas contienen “grupos fotosensibles, también conocidos como 'grupos protectores fotorremovibles', de los cuales se liberan sustancias objetivo al exponerlas a longitudes de onda de luz específicas”. [12] Los grupos fotosensibles protegen física y químicamente al objetivo para que no se libere hasta que la molécula experimente una fotorreacción. [12] Debido a estas interacciones con la luz, son moléculas comúnmente utilizadas en fotofarmacología. Más recientemente, han desempeñado un papel importante en la quimioterapia fotoactivada (PACT). En PACT, las fotojaulas utilizan un grupo protector fotoremovible que protege los fármacos citotóxicos hasta que el enlace se escinde mediante interacción luminosa y se libera el fármaco citotóxico. [13] Algunas jaulas fotográficas bien conocidas incluyen “derivados de o-nitrobencilo, derivados de cumarina, BODIPY, derivados de xanteno, derivados de quinona y diarilenos”. [12] Sin embargo, existen limitaciones en el uso de fotojaulas en aplicaciones clínicas, ya que no hay muchos PPG que puedan usarse in vivo. Esto se debe a que los conjugados PPG-carga útil deben tener una solubilidad e inercia biológica aceptables para la biocompatibilidad y la necesidad de un desenjaulamiento eficiente por encima de 600 nm. [13]
Figura 5. Ejemplo de un sistema de liberación de fotojaula activado por NIR [14]
La fotofarmacología, el uso de la luz para controlar la actividad de los fármacos, ha surgido como un enfoque prometedor para la administración y la terapia de fármacos. Aprovechando el poder de la luz, los investigadores pueden lograr un control preciso sobre la liberación y activación de fármacos, ofreciendo nuevas posibilidades para tratamientos específicos y personalizados. En esta subsección, exploramos la aplicación de la fotofarmacología en la administración de fármacos, centrándonos en los avances recientes y las posibles aplicaciones clínicas. En este estudio [15] los investigadores diseñaron inhibidores de HDAC que pueden activarse o desactivarse con luz, proporcionando un control terapéutico preciso. Este enfoque podría reducir los efectos secundarios de la quimioterapia tradicional al dirigir los inhibidores a áreas específicas del cuerpo, lo que podría conducir a tratamientos contra el cáncer más efectivos y personalizados.

En este estudio, [16] los investigadores desarrollaron una estrategia para conectar un grupo fotoconmutable a un antibiótico común; ciprofloxacina. Al conectar el grupo fotoconmutable, los investigadores pueden controlar la actividad de la ciprofloxacina con luz. Este enfoque podría conducir potencialmente a nuevas formas de tratar infecciones bacterianas, con la capacidad de activar y desactivar la actividad del antibiótico según sea necesario. En este artículo [17] se desarrolla un protocolo in vitro para probar diferentes longitudes de onda de luz en líneas celulares de cáncer humano y se descubre que la luz azul inhibe con mayor eficacia el crecimiento celular. Esto sugiere que la fotofarmacología podría ofrecer nuevas opciones de tratamiento del cáncer al apuntar a longitudes de onda de luz específicas para modular la actividad del fármaco en las células tumorales. Otra aplicación de la fotofarmacología [18] es el desarrollo de un fotoCORM luminiscente injertado en carboximetilquitosano que, cuando se expone a la luz, libera monóxido de carbono (CO) para inducir la muerte apoptótica en células de cáncer colorrectal, lo que demuestra un control preciso sobre la liberación de CO para la terapia dirigida contra el cáncer. Los investigadores desarrollaron una caja de herramientas de antagonistas fotoconmutables que pueden interactuar con los GPCR, una clase de proteínas implicadas en diversos procesos celulares. [19] Al utilizar la luz para cambiar la actividad de estos antagonistas, los investigadores pueden controlar la interacción entre los antagonistas y los GPCR en tiempo real. Este enfoque permite una modulación precisa de la actividad de GPCR, lo que podría conducir a nuevos conocimientos sobre las vías de señalización celular y posibles aplicaciones terapéuticas. En otra aplicación [20], al utilizar luz para controlar el ensamblaje de nanoporos, los investigadores pueden potencialmente regular el flujo de iones o moléculas a través de estos nanoporos. Este enfoque podría tener aplicaciones en diversos campos, incluida la detección, la administración de fármacos y la nanotecnología. En este artículo [21] han utilizado la fotofarmacología para controlar la actividad de los fármacos; Las fibras multifuncionales en el estudio entregan luz y medicamentos a áreas específicas del cuerpo. Las fibras implantadas activan los fármacos que responden a la luz, alterando su estructura y ofreciendo una administración precisa del fármaco en condiciones que requieren una dosis o un momento exacto. En otro estudio, [22] se diseñaron ligandos para cambiar su modo de unión al ADN cuádruplex G tras la exposición a la luz visible. Este método podría modular potencialmente la actividad del ADN G-quadruplex, crucial en la expresión genética y el mantenimiento de los telómeros, ofreciendo nuevas vías terapéuticas, particularmente en el tratamiento del cáncer. El estudio subraya la promesa de la fotofarmacología a la hora de apuntar a estructuras de ADN específicas, lo que sugiere que el ADN cuádruplex G es un objetivo viable para futuras intervenciones fotofarmacológicas. Este estudio [23]desarrollaron conjugados fotoactivables de anticuerpo-fotoCORM dirigidos a células de cáncer de ovario humano, liberando CO tras la exposición a la luz para disminuir la viabilidad celular. Este enfoque ofrece una orientación precisa a las células cancerosas y al mismo tiempo minimiza el daño al tejido sano, lo que muestra el potencial de la fotofarmacología en la terapia contra el cáncer. En este artículo, se ha desarrollado [24] un compuesto fotoactivable que se une y modula la actividad de la proteína CRY1, regulando el reloj circadiano de los mamíferos. Al utilizar la luz para controlar la actividad del compuesto, los investigadores pueden tratar potencialmente los trastornos del ritmo circadiano y las afecciones de salud relacionadas modulando la función de CRY1. La fotofarmacología implica el uso de la luz para controlar la actividad de los fármacos. En otra aplicación [25], los investigadores utilizan la fotofarmacología para controlar la liberación de fármacos y se centran en un fármaco que interactúa con la tubulina, visualizando su liberación en tiempo real con cristalografía en serie con resolución temporal. Esta técnica ofrece información sobre las interacciones entre fármacos y tubulina y demuestra el potencial para diseñar fármacos con acciones precisas.
El futuro de la fotofarmacología es inmensamente prometedor. Tiene el potencial de revolucionar la terapia farmacológica convencional ofreciendo nuevas vías para la medicina de precisión, el tratamiento de trastornos neurológicos y en el campo de la oncología y la oftalmología . [1] Además, es prometedor para el campo de la medicina regenerativa , donde se pueden utilizar fotointerruptores para modular la actividad de las vías de señalización para la reparación y regeneración de tejidos específicos. [3]
La fotofarmacología seguirá creciendo y expandiéndose con los nuevos descubrimientos y avances que se produzcan en otros campos relacionados como la química sintética, la biología, la nanotecnología, la farmacología y la bioingeniería. Si bien el potencial de la fotofarmacología es enorme, existen algunos desafíos que deben abordarse para convertirla en una realidad clínica. Uno de esos desafíos es el desarrollo de fotointerruptores estables y biocompatibles que sean selectivos para sus receptores objetivo sin actividad cruzada. [2] Es particularmente importante que estas fotoconmutables tengan sus bandas de absorbancia dentro del rango de longitud de onda de 650 nm a 900 nm. [2] Por lo tanto, se requiere un diseño molecular óptimo de los fotointerruptores para lograr las características mencionadas anteriormente y el nivel de rendimiento deseado. En la actualidad, la fotofarmacología utiliza un enfoque de diseño racional de fármacos basado en el estudio de la relación estructura-actividad; sin embargo, una detección fenotípica de fármacos fotoconmutables también podría ser beneficiosa.
Para lograr un buen control espacio-temporal sobre la actividad del fármaco, debería haber una diferencia significativa entre la actividad de los isómeros. Sin embargo, la comprensión de los cambios estructurales durante los efectos biológicos inducidos por la fotoconmutación es limitada. Esta escasez de conocimiento también es un desafío para el crecimiento de este campo, ya que dificulta la optimización de la actividad y potencia de los isómeros para obtener los resultados esperados durante las aplicaciones. [3]
Otro obstáculo, el mayor desafío en fotofarmacología, es encontrar formas apropiadas y efectivas de llevar luz a los tejidos profundos del cuerpo y evitar problemas como la dispersión y la absorción. Se han intentado varias estrategias a este respecto, una de las cuales es el desarrollo de ligandos fotoconmutables que responden a longitudes de onda que penetran en los tejidos profundos, como la luz roja o infrarroja. Además, algunos estudios preclínicos recientes han estimulado el desarrollo de dispositivos inalámbricos, compactos o inyectables y controlables de forma remota capaces de suministrar luz a los tejidos neurales con un daño mínimo. [26] Existen nuevos sistemas optofluídicos que pueden regular simultáneamente tanto la administración de fármacos como la actividad de la luz en sitios específicos. Aunque la entrega externa de luz es el método más preferido, el uso de fuentes de luz exógenas internas, como compuestos luminiscentes, donde la luz se entregaría directamente en el sitio de acción. Esto podría evitar los problemas relacionados con la penetración de la luz y también mejorar el grado de selectividad. Además, esto crea la oportunidad de utilizar la fotofarmacología como un enfoque teranóstico que combina la administración dirigida de fármacos y la obtención de imágenes moleculares. [2]