

La extracción de cobre se refiere a los métodos utilizados para obtener cobre de sus minerales . La conversión de minerales de cobre consiste en una serie de procesos físicos, químicos y electroquímicos. Los métodos han evolucionado y varían según el país en función de la fuente del mineral, las regulaciones ambientales locales y otros factores. [1]

El Complejo del Cobre Antiguo de América del Norte ha sido datado radiométricamente en 9500 a. C., es decir, alrededor de 7480 a. C., lo que lo convierte en uno de los ejemplos más antiguos conocidos de extracción de cobre en el mundo. [2] La evidencia más temprana del martillado en frío del cobre nativo proviene de la excavación en Çayönü Tepesi en el este de Anatolia , que data entre 7200 y 6600 a. C. [3] Entre los diversos elementos considerados votivos o amuletos, había uno que parecía un anzuelo y otro como un punzón. Otro hallazgo, en la cueva de Shanidar en Mergasur, Irak, contenía cuentas de cobre y se remonta a 8700 a. C. [4]
Una de las minas de cobre más antiguas del mundo conocidas, a diferencia del uso de depósitos superficiales, se encuentra en el valle de Timna , Israel, y se ha utilizado desde el cuarto milenio antes de Cristo, con un uso de depósitos superficiales que se produjo en el quinto y sexto milenio. [5] [6]
El yacimiento arqueológico de Pločnik , en el sureste de Europa ( Serbia ), contiene la evidencia más antigua datada con seguridad de la fabricación de cobre a alta temperatura, del 5000 a. C. [7] El hallazgo de junio de 2010 se extiende por otros 500 años, datado en el quinto milenio a. C., lo que representa el registro más temprano de fundición de cobre de Rudna Glava ( Serbia ). [8]
La tecnología de fundición del cobre dio origen a la Edad del Cobre , también conocida como Edad Calcolítica, y luego a la Edad del Bronce . La Edad del Bronce no habría sido posible sin el desarrollo de la tecnología de fundición.

Hasta la segunda mitad del siglo XX, la fundición de minerales de sulfuro era casi el único medio para producir cobre metálico a partir de minerales extraídos ( producción primaria de cobre). En 2002, el 80% de la producción primaria mundial de cobre provenía de minerales de cobre, hierro y azufre, y la gran mayoría de estos se procesaban mediante fundición. [9]
En un principio, el cobre se recuperaba de los minerales de sulfuro fundiéndolos directamente en un horno. [10] Las fundiciones se ubicaban inicialmente cerca de las minas para minimizar el costo del transporte. Esto evitaba los costos prohibitivos de transportar los minerales de desecho y el azufre y el hierro presentes en los minerales que contenían cobre. Sin embargo, a medida que disminuía la concentración de cobre en los yacimientos de mineral, los costos energéticos de fundir todo el mineral también se volvieron prohibitivos y se hizo necesario concentrar primero los minerales.
Las técnicas de concentración iniciales incluían la clasificación manual [11] y la concentración por gravedad. Estas dieron como resultado grandes pérdidas de cobre. En consecuencia, el desarrollo del proceso de flotación por espuma fue un gran paso adelante en el procesamiento de minerales. [12] El proceso moderno de flotación por espuma fue inventado independientemente a principios del siglo XX en Australia por CV Potter y aproximadamente al mismo tiempo por GD Delprat . [13] Hizo posible el desarrollo de la mina gigante Bingham Canyon en Utah. [14]
En el siglo XX, la mayoría de los minerales se concentraban antes de fundirlos. La fundición se realizaba inicialmente utilizando plantas de sinterización y altos hornos , [15] o con tostadores y hornos de reverbero . [16] La fundición en hornos de reverbero y tostadores dominaron la producción primaria de cobre hasta la década de 1960. [9]
En los años 1960 y 1970, las grandes operaciones mineras de cobre de empresas estadounidenses fueron nacionalizadas en muchos de los principales países productores de cobre. [17] Así, en los años 1980, las empresas estatales superaron el papel dominante que habían tenido hasta entonces empresas estadounidenses como Anaconda Copper y Kennecott . [17] A fines de los años 1970 y principios de los años 1980, varias compañías petroleras como ARCO , Exxon (Exxon Minerals) y Standard Oil Company se expandieron a la minería de cobre durante algunos años antes de vender sus activos de cobre. [17] Según se informa, las ganancias no fueron tan altas como se esperaba. [17] Las inversiones en la minería de cobre se concentraron en Chile en los años 1980 y 1990, dado que la minería de cobre en otros países enfrentaba problemas como inestabilidad política ( Perú ), mayores requisitos ambientales (países desarrollados) o desinterés general en la inversión extranjera en una industria minera nacionalizada ( Zaire , Zambia ). [17]

El grado promedio de los minerales de cobre en el siglo XXI es inferior al 0,6% de cobre, con una proporción de minerales de mena económicos que es inferior al 2% del volumen total de la roca de mena. Por lo tanto, en todas las operaciones mineras, el mineral generalmente debe ser beneficiado (concentrado). El concentrado se vende típicamente a fundiciones distantes , aunque algunas minas grandes tienen fundiciones ubicadas cerca. Esta coubicación de minas y fundiciones era más típica en los siglos XIX y principios del XX, cuando las fundiciones más pequeñas podían ser económicas. Las técnicas de procesamiento posteriores dependen de la naturaleza del mineral.
En el caso habitual, cuando se trata principalmente de minerales de cobre sulfurados (como calcopirita , FeCuS 2 ), el mineral se trata mediante conminución , donde la roca se tritura para producir partículas pequeñas (<100 μm) que consisten en fases minerales individuales. Estas partículas están listas para ser separadas para eliminar la ganga (residuos de rocas de silicato) mediante flotación por espuma. [1]


En la flotación por espuma, el mineral triturado se humedece, se suspende en una suspensión y se mezcla con reactivos que vuelven hidrófobas las partículas de sulfuro . Los reactivos típicos ("colectores") incluyen etilxantato de potasio y etilxantato de sodio , pero también se utilizan ditiofosfatos y ditiocarbamatos. La suspensión se introduce en un tanque de aireación lleno de agua que contiene un surfactante como metilisobutilcarbinol (MIBC). El aire se fuerza constantemente a través de la suspensión. Las burbujas de aire se adhieren a las partículas hidrófobas de sulfuro de cobre, que se transportan a la superficie donde se retira la espuma. Estos desnatados generalmente se someten a una celda limpiadora-depuradora para eliminar el exceso de silicatos y otros minerales de sulfuro que pueden afectar negativamente la calidad del concentrado (normalmente, galena ), y el concentrado final se envía a fundición. La roca que no ha flotado en la celda de flotación se descarta como relave o se procesa más para extraer otros metales como plomo (de galena) y zinc (de esfalrita ), si existen. Se toman diversas medidas para mejorar la eficiencia de la flotación por espuma. Se utiliza cal para elevar el pH del baño de agua, lo que hace que el colector se adhiera de manera más eficiente a los sulfuros de cobre. El proceso puede producir concentrados con un contenido de cobre de 27-29% y 37-40% a partir de calcopirita y calcocita , respectivamente.

Los minerales de cobre oxidados incluyen carbonatos como la azurita y la malaquita , el silicato crisocola y sulfatos como la atacamita . En algunos casos, se permite que los minerales de sulfuro se degraden a óxidos. Dichos minerales son susceptibles de hidrometalurgia. Específicamente, dichos minerales de óxido generalmente se extraen en ácido sulfúrico acuoso , generalmente en una lixiviación en pilas o en vertederos . La solución de lixiviación preñada resultante se purifica mediante extracción con solvente (SX). Se trata con un solvente orgánico y un quelante orgánico. Los quelantes se unen a los iones de cobre (y ningún otro ion, idealmente), los complejos resultantes se disuelven en la fase orgánica. Este solvente orgánico se evapora, dejando un residuo de los complejos de cobre. Los iones de cobre se liberan del residuo con ácido sulfúrico. El ácido sulfúrico barrado (desnudo) se recicla nuevamente en los montones. Los ligandos orgánicos también se recuperan y reciclan. Otra posibilidad es que el cobre se precipite de la solución rica poniéndolo en contacto con chatarra de hierro, un proceso denominado cementación . El cobre cementado normalmente es menos puro que el cobre obtenido mediante extracción por electroforesis en polvo. [18]

Los sulfuros secundarios, aquellos formados por enriquecimiento secundario supérgeno , son resistentes ( refractarios ) a la lixiviación sulfúrica. [19] Los sulfuros secundarios de cobre están dominados por el mineral calcocita; un mineral formado a partir de sulfuros primarios, como la calcopirita , que experimentan procesos químicos como oxidación o reducción. [20] Normalmente, los minerales de sulfuro secundarios se concentran mediante flotación por espuma. [21] Otros procesos de extracción como la lixiviación se utilizan eficazmente para la extracción de sulfuros de cobre secundarios, pero a medida que aumenta la demanda de cobre, se requieren procesos de extracción adaptados a minerales de baja calidad, debido al agotamiento de los recursos de cobre. [22] Los procesos que incluyen in situ, en vertedero y en pilas son métodos rentables que son adecuados para extraer cobre de minerales de baja calidad. [23]
Los procesos de extracción de sulfuros secundarios de cobre y minerales de baja calidad incluyen el proceso de biolixiviación en pilas. La biolixiviación en pilas presenta un método de extracción rentable que requiere un consumo de energía menos intensivo, lo que genera mayores ganancias. [24] Este proceso de extracción se puede aplicar a grandes cantidades de minerales de baja calidad, con un menor costo de capital y un impacto ambiental mínimo. [24] [25]
Generalmente, la flotación directa con espuma no se utiliza para concentrar minerales de óxido de cobre, como resultado de la estructura en gran parte iónica e hidrófila de la superficie del mineral de óxido de cobre. [26] Los minerales de óxido de cobre se tratan típicamente mediante flotación con reactivos quelantes y flotación con ácidos grasos, que utilizan reactivos orgánicos para asegurar la adsorción en la superficie del mineral a través de la formación de compuestos hidrófobos en la superficie del mineral. [26] [27]
Algunos depósitos de sulfuro supergénico se pueden lixiviar utilizando un proceso de lixiviación en pilas de oxidación bacteriana para oxidar los sulfuros a ácido sulfúrico, lo que también permite la lixiviación simultánea con ácido sulfúrico para producir una solución de sulfato de cobre . [28] [29] Para los minerales de óxido, se utilizan tecnologías de extracción por solventes y electroobtención para recuperar el cobre de la solución de lixiviación preñada . [30] Para asegurar la mejor recuperación de cobre, es importante reconocer el efecto que la disolución del cobre, el consumo de ácido y la composición mineral de ganga tienen sobre la eficacia de la extracción. [30]
Los minerales de sulfuro supergénicos ricos en cobre nativo son refractarios al tratamiento con lixiviación con ácido sulfúrico en todas las escalas de tiempo practicables, y las partículas metálicas densas no reaccionan con los medios de flotación de espuma. Por lo general, si el cobre nativo es una parte menor de un perfil supergénico, no se recuperará y se reportará a los relaves . Cuando son lo suficientemente ricos, los cuerpos de mineral de cobre nativo pueden tratarse para recuperar el cobre contenido mediante separación por gravedad . A menudo, la naturaleza de la ganga es importante, ya que los minerales de cobre nativo ricos en arcilla resultan difíciles de liberar. Esto se debe a que los minerales de arcilla interactúan con los reactivos de flotación utilizados en los procesos de extracción, que luego se consumen, lo que da como resultado una recuperación mínima de un concentrado de cobre de alta calidad. [31]
El proceso de calcinación se realiza generalmente en combinación con hornos de reverbero . En el calcinador, el concentrado de cobre se oxida parcialmente para producir " calcinación ". Se libera dióxido de azufre . La estequiometría de la reacción es:
La tostación generalmente deja más azufre en el producto calcinado (15% en el caso del tostador de Mount Isa Mines [32] ) que el que deja una planta de sinterización en el producto sinterizado (alrededor del 7% en el caso de la fundición de refinación y fundición electrolítica [33] ).
A partir de 2005, la tostación ya no es común en el tratamiento de concentrados de cobre porque su combinación con hornos de reverbero no es eficiente energéticamente y la concentración de SO2 en los gases de escape del tostador es demasiado diluida para una captura rentable. Ahora se favorece la fundición directa y se utilizan las siguientes tecnologías de fundición: fundición flash , hornos Isasmelt , Noranda, Mitsubishi o El Teniente. [9]


La fusión inicial del material a fundir se denomina habitualmente etapa de fundición o de fundición de mata . Puede llevarse a cabo en una variedad de hornos, incluidos los en gran medida obsoletos altos hornos y hornos de reverbero , así como hornos flash , hornos Isasmelt , etc. El producto de esta etapa de fundición es una mezcla de cobre, hierro y azufre que se enriquece en cobre, que se denomina mata o mata de cobre . [9] El término grado de mata se utiliza normalmente para referirse al contenido de cobre de la mata. [34]
El propósito de la etapa de fundición de mata es eliminar la mayor cantidad posible de minerales no deseados de hierro, azufre y ganga (como sílice, magnesia, alúmina y piedra caliza), mientras se minimiza la pérdida de cobre. [9] Esto se logra haciendo reaccionar sulfuros de hierro con oxígeno (en aire o aire enriquecido con oxígeno) para producir óxidos de hierro (principalmente como FeO , pero con algo de magnetita (Fe 3 O 4 )) y dióxido de azufre . [34]
El sulfuro de cobre y el óxido de hierro se pueden mezclar, pero cuando se añade suficiente sílice, se forma una capa de escoria separada. [35] La adición de sílice también reduce el punto de fusión (o, más apropiadamente, la temperatura de liquidus ) de la escoria, lo que significa que el proceso de fundición se puede operar a una temperatura más baja. [35]
La reacción de formación de escoria es:
La escoria es menos densa que la mata, por lo que forma una capa que flota sobre la mata. [36]
El cobre se puede perder de la mata de tres maneras: como óxido cuproso (Cu 2 O) disuelto en la escoria, [37] como sulfuro de cobre disuelto en la escoria [38] o como pequeñas gotas (o gránulos ) de mata suspendidas en la escoria. [39] [40]
La cantidad de cobre perdido como óxido de cobre aumenta a medida que aumenta el potencial de oxígeno de la escoria. [40] El potencial de oxígeno generalmente aumenta a medida que aumenta el contenido de cobre de la mata. [41] Por lo tanto, la pérdida de cobre como óxido aumenta a medida que aumenta el contenido de cobre de la mata. [42]
Por otra parte, la solubilidad del cobre sulfídico en la escoria disminuye a medida que el contenido de cobre de la mata aumenta más allá de aproximadamente el 40%. [38] Nagamori calculó que más de la mitad del cobre disuelto en escorias de matas que contienen menos del 50% de cobre es cobre sulfídico. Por encima de esta cifra, el cobre oxídico comienza a dominar. [38]
La pérdida de cobre en forma de gránulos suspendidos en la escoria depende del tamaño de los gránulos, la viscosidad de la escoria y el tiempo de sedimentación disponible. [43] Rosenqvist sugirió que aproximadamente la mitad de las pérdidas de cobre en la escoria se debían a los gránulos suspendidos. [43]
La masa de escoria generada en la etapa de fundición depende del contenido de hierro del material que se alimenta al horno de fundición y del grado de mata deseado. Cuanto mayor sea el contenido de hierro de la alimentación, más hierro será necesario rechazar en la escoria para obtener un grado de mata determinado. De manera similar, aumentar el grado de mata deseado requiere rechazar más hierro y aumentar el volumen de escoria.
Así, los dos factores que más inciden en la pérdida de cobre por escoria en la etapa de fundición son:
Esto significa que existe un límite práctico en cuanto al grado de mata que se puede obtener si se desea minimizar la pérdida de cobre en la escoria. Por lo tanto, se requieren etapas posteriores de procesamiento (conversión y refinación a fuego).
Las siguientes subsecciones describen brevemente algunos de los procesos utilizados en la fundición de mata.
Los hornos de reverbero son hornos largos que pueden tratar concentrado húmedo, seco o tostado. La mayoría de los hornos de reverbero utilizados en los últimos años trataban concentrado tostado porque introducir materiales de alimentación secos en el horno de reverbero es más eficiente energéticamente y porque la eliminación de parte del azufre en el tostador da como resultado calidades de mata más altas. [9]
La carga del horno de reverbero se añade al horno a través de orificios de alimentación a lo largo de los lados del horno, y la carga sólida se funde. [9] Normalmente se añade sílice adicional para ayudar a formar la escoria. El horno se enciende con quemadores que utilizan carbón pulverizado, fueloil o gas natural. [44]
Los hornos de reverbero también pueden alimentarse con escoria fundida de la etapa de conversión posterior para recuperar el cobre contenido y otros materiales con un alto contenido de cobre. [44]
Debido a que el baño del horno de reverbero está en reposo, se produce muy poca oxidación de la carga (y, por lo tanto, se elimina muy poco azufre del concentrado). Es esencialmente un proceso de fusión. [43] En consecuencia, los hornos de reverbero cargados en húmedo tienen menos cobre en su producto de mata que los hornos cargados con calcinación, y también tienen menores pérdidas de cobre en la escoria. [44] Gill cita un valor de cobre en la escoria de 0,23 % para un horno de reverbero cargado en húmedo frente a 0,37 % para un horno cargado con calcinación. [44]
En el caso de hornos cargados con calcinación, una parte significativa del azufre se ha eliminado durante la etapa de calcinación, y la calcinación consiste en una mezcla de óxidos y sulfuros de cobre y hierro. El horno de reverbero actúa para permitir que estas especies se acerquen al equilibrio químico a la temperatura de operación del horno (aproximadamente 1600 °C en el extremo del quemador del horno y alrededor de 1200 °C en el extremo de la chimenea; [45] la mata está a aproximadamente 1100 °C y la escoria a aproximadamente 1195 °C [44] ). En este proceso de equilibrio, el oxígeno asociado con los compuestos de cobre se intercambia con el azufre asociado con los compuestos de hierro, lo que aumenta el contenido de óxido de hierro del horno, y los óxidos de hierro interactúan con sílice y otros materiales de óxido para formar la escoria. [44]
La principal reacción de equilibrio es:
La escoria y la mata forman capas distintas que pueden ser retiradas del horno como corrientes separadas. La capa de escoria se deja fluir periódicamente a través de un agujero en la pared del horno por encima de la altura de la capa de mata. La mata se retira drenándola a través de un agujero en cucharas para que sea transportada por grúa a los convertidores. [44] Este proceso de drenaje se conoce como sangría del horno. [44] El orificio de sangría de la mata es normalmente un agujero a través de un bloque de cobre enfriado por agua que evita la erosión de los ladrillos refractarios que recubren el horno. Cuando se completa la eliminación de la mata o la escoria, el orificio normalmente se tapa con arcilla, que se retira cuando el horno está listo para ser sangrado nuevamente.
Los hornos de reverbero se utilizaban a menudo para tratar la escoria fundida del convertidor para recuperar el cobre contenido. [44] Este se vertía en los hornos desde cucharas transportadas por grúas. Sin embargo, la escoria del convertidor tiene un alto contenido de magnetita [46] y parte de esta magnetita se precipitaría de la escoria del convertidor (debido a su punto de fusión más alto), formando una acreción en el hogar del horno de reverbero y haciendo necesario apagar el horno para eliminar la acreción. [46] Esta formación de acreción limita la cantidad de escoria del convertidor que se puede tratar en un horno de reverbero. [46]
Aunque los hornos de reverbero tienen muy pocas pérdidas de cobre por escoria, no son muy eficientes energéticamente y las bajas concentraciones de dióxido de azufre en sus gases de escape hacen que su captura sea poco económica. En consecuencia, los operadores de fundiciones dedicaron mucho dinero en los años 1970 y 1980 al desarrollo de nuevos procesos de fundición de cobre más eficientes. [47] Además, en años anteriores se habían desarrollado tecnologías de fundición instantánea que comenzaron a reemplazar a los hornos de reverbero. En 2002, 20 de los 30 hornos de reverbero que todavía funcionaban en 1994 habían sido cerrados. [9]
En la fundición instantánea , el concentrado se dispersa en una corriente de aire u oxígeno y las reacciones de fundición se completan en gran medida mientras las partículas minerales todavía están en vuelo. [47] Las partículas reaccionadas luego se depositan en un baño en el fondo del horno, donde se comportan como calcinación en un horno de reverbero. [48] Se forma una capa de escoria sobre la capa de mata, y se pueden extraer por separado del horno. [48]

El proceso ISASMELT es un proceso de fundición energéticamente eficiente que fue desarrollado conjuntamente entre los años 1970 y 1990 por Mount Isa Mines (una subsidiaria de MIM Holdings y ahora parte de Glencore ) y la CSIRO del Gobierno de Australia . Tiene costos operativos y de capital relativamente bajos para un proceso de fundición.
La tecnología ISASMELT se ha aplicado a la fundición de plomo, cobre y níquel. En 2021, había 22 plantas en funcionamiento en once países, junto con tres plantas de demostración ubicadas en Mt Isa. La capacidad instalada de las plantas operativas de cobre/níquel en 2020 fue de 9,76 millones de toneladas por año de materias primas y 750 mil toneladas por año en las plantas operativas de plomo. [49]
Las fundiciones basadas en el proceso ISASMELT de cobre se encuentran entre las fundiciones de cobre de menor costo del mundo. [50]
La mata que se produce en la fundición contiene entre un 30 y un 70 % de cobre (según el proceso utilizado y la filosofía de funcionamiento de la fundición), principalmente en forma de sulfuro de cobre y sulfuro de hierro. El azufre se elimina a alta temperatura en forma de dióxido de azufre mediante la inyección de aire a través de la mata fundida:
En una reacción paralela el sulfuro de hierro se convierte en escoria:
La pureza de este producto es del 98%, se le conoce como blíster debido a la superficie rota que se crea por el escape de gas de dióxido de azufre cuando se enfrían los lingotes o los cerdos de cobre blíster . Los subproductos generados en el proceso son dióxido de azufre y escoria . El dióxido de azufre se captura y se convierte en ácido sulfúrico y se vende en el mercado abierto o se utiliza en procesos de lixiviación de cobre.

El cobre blíster se coloca en un horno de ánodo, un horno que refina el cobre blíster hasta convertirlo en cobre de grado anódico en dos etapas, eliminando la mayor parte del azufre y el hierro restantes y luego eliminando el oxígeno introducido durante la primera etapa. Esta segunda etapa, a menudo denominada como poling , se realiza soplando gas natural , o algún otro agente reductor, a través del óxido de cobre fundido. Cuando esta llama arde de color verde, lo que indica el espectro de oxidación del cobre, el oxígeno se ha quemado en su mayor parte. Esto crea cobre con una pureza de aproximadamente el 99%.

La etapa final en la producción de cobre es el refinado. El refinado se logra mediante electrólisis , que aprovecha la conversión fácil (de bajo potencial) y selectiva de soluciones de cobre (II) en el metal. Los ánodos fundidos a partir de cobre blíster procesado se colocan en una solución acuosa de 3-4% de sulfato de cobre y 10-16% de ácido sulfúrico . Los cátodos son láminas delgadas laminadas de cobre altamente puro o, más comúnmente en estos días, láminas iniciales de acero inoxidable reutilizables (como en el proceso IsaKidd ). [51] Se requiere un potencial de solo 0,2-0,4 voltios para que comience el proceso. En las plantas industriales son posibles densidades de corriente de hasta 420 A/m 2 . [52]
En el ánodo ( reacción de oxidación ), el cobre y los metales menos nobles se disuelven . Los metales más nobles y los elementos menos solubles , como la plata , el oro , el selenio y el telurio , se depositan en el fondo de la celda como limo del ánodo , que forma un subproducto vendible. Los iones de cobre (II) migran a través del electrolito hasta el cátodo. En el cátodo ( reacción de reducción ), los iones Cu 2+ se reducen en el metal de cobre y el Cu (s) se deposita, pero los componentes menos nobles, como el arsénico y el zinc, permanecen en solución a menos que se use un voltaje más alto. [53]
Las reacciones que involucran cobre metálico y iones Cu 2+ en los electrodos son las siguientes:
Los concentrados de cobre producidos por las minas se venden a fundiciones y refinerías que tratan el mineral y refinan el cobre y cobran por este servicio a través de cargos por tratamiento (TC) y cargos por refinación (RC). Los TC se cobran en dólares estadounidenses por tonelada de concentrado tratado y los RC se cobran en centavos por libra tratada, denominados en dólares estadounidenses, con precios de referencia establecidos anualmente por las principales fundiciones japonesas. El cliente en este caso puede ser una fundición, que revende lingotes de cobre blíster a una refinería, o una fundición-refinación que está integrada verticalmente.
Una forma predominante de concentrado de cobre contiene oro y plata, como el producido por Bougainville Copper Limited en la mina Panguna desde principios de la década de 1970 hasta fines de la década de 1980. [54]
El contrato típico para una minera está denominado contra el precio de la Bolsa de Metales de Londres, menos los TC-RC y cualquier penalidad o crédito aplicable. Se pueden aplicar penalidades a los concentrados de cobre según el nivel de elementos nocivos como arsénico , bismuto , plomo o tungsteno . Debido a que una gran parte de los yacimientos de mineral de sulfuro de cobre contienen plata u oro en cantidades apreciables, se puede pagar un crédito a la minera por estos metales si su concentración dentro del concentrado es superior a una cierta cantidad. Por lo general, el refinador o la fundición cobran a la minera una tarifa basada en la concentración; un contrato típico especificará que se debe un crédito por cada onza del metal en el concentrado por encima de cierta concentración; por debajo de eso, si se recupera, la fundición conservará el metal y lo venderá para sufragar los costos.
El concentrado de cobre se comercializa a través de contratos al contado o de contratos a largo plazo como un producto intermedio por derecho propio. A menudo, la fundición vende el metal de cobre en nombre de la minera. La minera recibe el precio en el momento en que la fundición-refinadora realiza la venta, no al precio vigente en la fecha de entrega del concentrado. En un sistema de precios cotizados, el precio se acuerda en una fecha fija en el futuro, normalmente 90 días después de la entrega a la fundición.
El cátodo de cobre de grado A está compuesto en un 99,99 % por láminas de 1 cm de espesor y aproximadamente 1 metro cuadrado que pesan aproximadamente 200 libras. Es un verdadero producto básico , que se puede entregar y comercializar en las bolsas de metales de la ciudad de Nueva York (COMEX), Londres (London Metals Exchange) y Shanghái (Shanghai Futures Exchange). A menudo, el cátodo de cobre se comercializa en las bolsas de manera indirecta a través de warrants, opciones o contratos de swap, de modo que la mayor parte del cobre se comercializa en la LME/COMEX/SFE, pero la entrega se realiza directamente, moviendo logísticamente el cobre físico y transfiriendo la lámina de cobre desde los propios almacenes físicos.
La especificación química para el cobre de grado electrolítico es ASTM B 115-00 (una norma que especifica la pureza y la resistividad eléctrica máxima del producto).

El pico de cobre es el momento en el que se alcanza la tasa máxima de producción mundial de cobre . Dado que el cobre es un recurso finito, en algún momento futuro la nueva producción minera disminuirá y en algún momento anterior la producción alcanzará un máximo. Cuándo ocurrirá esto es un tema de disputa. A diferencia de los combustibles fósiles , el cobre se desecha y se reutiliza, y se ha estimado que al menos el 80% de todo el cobre extraído alguna vez todavía está disponible (habiéndose reciclado repetidamente). [55]
El cobre es uno de los metales industriales más importantes, ocupando el tercer lugar después del hierro y el aluminio en términos de cantidad utilizada. [56] Es valorado por su conductividad térmica y eléctrica, ductilidad, maleabilidad y resistencia a la corrosión. Los usos eléctricos representan alrededor de las tres cuartas partes del consumo total de cobre, incluidos cables de alimentación, cables de datos y equipos eléctricos. También se utiliza en tuberías de refrigeración y enfriamiento, intercambiadores de calor , tuberías de agua y productos de consumo. [56]
El cobre ha sido utilizado por los seres humanos durante al menos 10.000 años. Más del 97% de todo el cobre extraído y fundido en la historia se ha extraído desde 1900. [ cita requerida ] La mayor demanda de cobre debido al crecimiento de las economías india y china desde 2006 ha provocado un aumento de los precios y un aumento del robo de cobre . [ 57 ]
La preocupación por el suministro de cobre no es nueva. En 1924, el geólogo y experto en minería de cobre Ira Joralemon advirtió: [58]
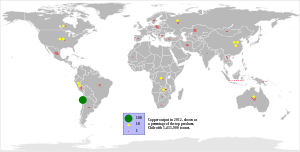
A nivel mundial, los recursos económicos de cobre se están agotando y cada año se consume una producción equivalente a la de tres minas de cobre de clase mundial. [57] El analista ambiental Lester Brown sugirió en 2008 que el cobre podría agotarse en 25 años basándose en lo que él consideraba una extrapolación razonable de un crecimiento del 2% anual. [59]
Se han hecho cincuenta y seis nuevos descubrimientos de cobre durante las tres décadas de 1975 a 2005. [57] Se dice que los descubrimientos mundiales de nuevos depósitos de cobre alcanzaron su punto máximo en 1996. [60] Sin embargo, según el Servicio Geológico de Estados Unidos (USGS), las reservas mundiales de cobre restantes se han más que duplicado desde entonces, de 310 millones de toneladas métricas en 1996 [61] a 890 millones de toneladas métricas en 2022. [62]

Como se muestra en el cuadro siguiente, los tres principales productores nacionales de cobre, respectivamente, en 2002, fueron Chile, Indonesia y los Estados Unidos . En 2013, fueron Chile, China y Perú. Veintiuna de las 28 minas de cobre más grandes del mundo (en 2006) no son susceptibles de expansión. [57]
El cobre es un elemento bastante común , con una concentración estimada de 50 a 70 ppm (0,005 a 0,007 por ciento) en la corteza terrestre (1 kg de cobre por cada 15 a 20 toneladas de roca de la corteza). [75] Una concentración de 60 ppm se multiplicaría hasta 1,66 cuatrillones de toneladas en el2,77 × 10 22 kg de masa de la corteza [76] , o más de 90 millones de años al ritmo de producción de 2013 de 18,3 MT por año. Sin embargo, no todo puede extraerse de manera rentable con el nivel actual de tecnología y el valor de mercado actual.
El Servicio Geológico de los Estados Unidos (USGS) informó que en 2005 la base actual de reservas totales de cobre en minerales potencialmente recuperables era de 1.600 millones de toneladas, de las cuales 950 millones de toneladas se consideraban económicamente recuperables. [77] Una evaluación global de 2013 identificó "455 depósitos conocidos (con recursos identificados bien definidos) que contienen alrededor de 1.800 millones de toneladas métricas de cobre", y predijo "una media de 812 depósitos no descubiertos dentro del kilómetro superior de la superficie de la Tierra" que contienen otros 3.100 millones de toneladas métricas de cobre "lo que representa alrededor de 180 veces la producción mundial de cobre de 2012 de todos los tipos de depósitos de cobre". [78]
En Estados Unidos, se recupera y se vuelve a poner en servicio más cobre a partir de material reciclado que el que se obtiene a partir de mineral recién extraído. El valor de reciclaje del cobre es tan grande que la chatarra de primera calidad normalmente tiene al menos el 95% del valor del metal primario del mineral recién extraído. [80] En Europa, aproximadamente el 50% de la demanda de cobre proviene del reciclaje (en 2016). [81]
En 2011 [actualizar], el cobre reciclado aportaba el 35% del consumo mundial total de cobre. [82] [ necesita actualización ]
En 2006, basándose en las tasas de descubrimiento y en los estudios geológicos existentes, los investigadores calcularon que podrían utilizarse 1.600 millones de toneladas métricas de cobre. Esta cifra se basó en la definición más amplia posible de cobre disponible, así como en la ausencia de limitaciones energéticas y preocupaciones ambientales. [77]
El Servicio Geológico de Estados Unidos estimó que, en 2013, quedaban 3.500 millones de toneladas métricas de recursos de cobre sin descubrir en todo el mundo en depósitos de tipo pórfido y alojados en sedimentos, dos tipos que actualmente proporcionan el 80% de la producción de cobre extraído. Esto se sumaba a los 2.100 millones de toneladas métricas de recursos identificados. Los recursos de cobre no descubiertos identificados y estimados combinados ascendían a 5.600 millones de toneladas métricas, [83] 306 veces la producción mundial de cobre recién extraído de 2013, de 18,3 millones de toneladas métricas.
Se estima que los nódulos de aguas profundas contienen 700 millones de toneladas de cobre. [65]
Julian Simon fue miembro senior del Cato Institute y profesor de economía y negocios. En su libro The Ultimate Resource 2 (publicado por primera vez en 1981 y reimpreso en 1998), critica extensamente la noción de “recursos máximos” y utiliza el cobre como ejemplo. Sostiene que, si bien el “pico de cobre” ha sido un temor persistente desde principios del siglo XX, las “reservas conocidas” crecieron a un ritmo que superó la demanda, y el precio del cobre no estaba aumentando sino cayendo a largo plazo. Por ejemplo, si bien la producción mundial de cobre en 1950 era solo una octava parte de lo que era a principios de la década de 2000, las reservas conocidas también eran mucho menores en ese momento –alrededor de 100 millones de toneladas métricas–, lo que hacía parecer que el mundo se quedaría sin cobre en 40 a 50 años como máximo.
La propia explicación de Simon para este desarrollo es que la noción misma de reservas conocidas es profundamente errónea, [84] ya que no tiene en cuenta los cambios en la rentabilidad minera. A medida que se agotan las minas más ricas, los desarrolladores dirigen su atención a fuentes más pobres del elemento y eventualmente desarrollan métodos baratos de extracción, aumentando las reservas conocidas. Así, por ejemplo, el cobre era tan abundante hace 5000 años, apareciendo en forma pura así como en minerales de cobre altamente concentrados, que los pueblos prehistóricos podían recolectarlo y procesarlo con tecnología muy básica. A principios del siglo XXI, el cobre se extrae comúnmente de minerales que contienen entre 0,3 y 0,6% de cobre en peso. Sin embargo, a pesar de que el material está mucho menos extendido, el costo de, por ejemplo, una olla de cobre era mucho menor a fines del siglo XX que hace 5000 años. [85] [ cita completa requerida ]
timna milenio.
{{citation}}: CS1 maint: bot: estado de URL original desconocido ( enlace )