
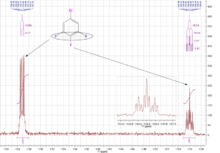
La espectroscopia de resonancia magnética nuclear de flúor-19 ( RMN de flúor o RMN de 19 F ) es una técnica analítica utilizada para detectar e identificar compuestos que contienen flúor. El 19 F es un núcleo importante para la espectroscopia de RMN debido a su receptividad y su gran dispersión de desplazamiento químico , que es mayor que la de la espectroscopia de resonancia magnética nuclear de protones . [1] [2] [3]
19 F tiene un espín nuclear (I) de 1 ⁄ 2 y una relación giromagnética alta . En consecuencia, este isótopo responde muy bien a las mediciones de RMN. Además, el 19 F comprende el 100 % de flúor natural. El único otro giro altamente sensible1/2Los núcleos activos en RMN que son monoisotópicos (o casi) son 1 H y 31 P. [4] [a] De hecho, el núcleo de 19 F es el tercer núcleo más receptivo de RMN, después del núcleo de 3 H y el núcleo de 1 H.
Los cambios químicos de 19 F NMR abarcan un rango de ca. 800 ppm. Para compuestos organoflúor el rango es más estrecho, siendo ca. -50 a -70 ppm (para grupos CF 3 ) a -200 a -220 ppm (para grupos CH 2 F). El rango espectral muy amplio puede causar problemas en el registro de espectros, como una mala resolución de los datos y una integración inexacta.
También es posible registrar espectros de 19 F{ 1 H} y 1 H{ 19 F} desacoplados y correlaciones de enlaces múltiples 19 F- 13 C HMBC y espectros HOESY a través del espacio.
Los cambios químicos de 19 F NMR en la literatura varían fuertemente, comúnmente en más de 1 ppm, incluso dentro del mismo solvente. [5] Aunque el compuesto de referencia para la espectroscopía de RMN 19 F, CFCl 3 puro (0 ppm), [6] se ha utilizado desde la década de 1950, [7] no estuvieron presentes instrucciones claras sobre cómo medirlo e implementarlo en mediciones de rutina hasta recientemente. [5] Una investigación de los factores que influyen en el cambio químico en la espectroscopia de RMN de flúor reveló que el disolvente tiene el mayor efecto (Δδ = ±2 ppm o más). [5] Se ha preparado una tabla de referencia específica de disolvente con 5 compuestos de referencia interna ( CFCl 3 , C 6 H 5 F , PhCF 3 , C 6 F 6 y CF 3 CO 2 H ) para permitir una referencia reproducible con una precisión de Δδ = ±30 ppb. [5] Como el desplazamiento químico del CFCl 3 también se ve afectado por el disolvente, se debe tener cuidado al utilizar CFCl 3 disuelto como compuesto de referencia con respecto al desplazamiento químico del CFCl 3 puro (0 ppm). [5] Ejemplo de desplazamientos químicos determinados frente a CFCl 3 puro : [5]
Para obtener una lista completa de los cambios químicos de los compuestos de referencia en 11 disolventes deuterados, se remite al lector a la literatura citada. [5]
También se ha proporcionado recientemente una lista concisa de cambios químicos debidamente referenciados de más de 240 sustancias químicas fluoradas. [5]
Los cambios químicos de 19 F NMR son más difíciles de predecir que los cambios de 1 H NMR. Específicamente, los cambios de 19 F NMR se ven fuertemente afectados por las contribuciones de los estados excitados electrónicos, mientras que los cambios de 1 H NMR están dominados por las contribuciones diamagnéticas. [8]
Para sustituyentes de flúor vinílico, la siguiente fórmula permite estimar los cambios químicos de 19 F:
Al determinar los desplazamientos químicos del 19 F de los átomos de flúor aromáticos, específicamente los fluoruros de fenilo, existe otra ecuación que permite una aproximación. Adoptada de "Determinación de la estructura de compuestos orgánicos", [10] esta ecuación es:
Los datos mostrados arriba son solo representativos de algunas tendencias y moléculas. Se pueden consultar otras fuentes y tablas de datos para obtener una lista más completa de tendencias en los cambios químicos del 19 F. Algo a tener en cuenta es que, históricamente, la mayoría de las fuentes literarias cambiaron la convención de utilizar negativos. Por lo tanto, tenga cuidado con el signo de los valores informados en otras fuentes. [8]
Las constantes de acoplamiento 19 F- 19 F son generalmente mayores que las constantes de acoplamiento 1 H- 1 H. Comúnmente se observan acoplamientos de largo alcance 19 F- 19 F ( 2 J, 3 J, 4 J o incluso 5 J). Generalmente, cuanto mayor sea el alcance del acoplamiento, menor será el valor. [11] El hidrógeno se acopla con el flúor, lo cual es muy típico de ver en el espectro de 19 F. Con un hidrógeno geminal, las constantes de acoplamiento pueden ser tan grandes como 50 Hz. Otros núcleos pueden acoplarse con flúor; sin embargo, esto se puede evitar realizando experimentos desacoplados. Es común realizar RMN de flúor con carbono y protones desacoplados. Los átomos de flúor también pueden acoplarse entre sí. Entre los átomos de flúor, las constantes de acoplamiento homonucleares son mucho mayores que entre los átomos de hidrógeno. Los flúor gemales suelen tener un valor J de 250-300 Hz. [11] Hay muchas buenas referencias para acoplar valores constantes. [11] Las citas se incluyen a continuación.
La resonancia magnética (MRI) de 19 F es una alternativa viable a la MRI de 1 H. Los problemas de sensibilidad se pueden superar mediante el uso de nanopartículas blandas . Las aplicaciones incluyen agentes de contraste sensibles al pH, temperatura, enzimas, iones metálicos y redox . También se pueden utilizar para el etiquetado celular a largo plazo. [12]
{{cite book}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace )