
Una enamina es un compuesto insaturado derivado de la condensación de un aldehído o cetona con una amina secundaria . [1] [2] Las enaminas son intermediarios versátiles. [3] [4]
La palabra "enamina" se deriva del afijo en -, utilizado como sufijo de alqueno , y la raíz amina . Esto se puede comparar con el enol , que es un grupo funcional que contiene tanto alqueno ( en- ) como alcohol (-ol ) . Las enaminas se consideran análogos nitrogenados de los enoles. [6]
Si uno o ambos sustituyentes de nitrógeno es un átomo de hidrógeno, se trata de la forma tautomérica de una imina . Esto generalmente se reorganizará en imina; sin embargo existen varias excepciones (como la anilina ). La tautomería enamina-imina puede considerarse análoga a la tautomería ceto-enol . En ambos casos, un átomo de hidrógeno cambia su ubicación entre el heteroátomo (oxígeno o nitrógeno) y el segundo átomo de carbono.
Las enaminas son buenos nucleófilos y buenas bases. Su comportamiento como nucleófilos basados en carbono se explica con referencia a las siguientes estructuras de resonancia.
Las enaminas son restos lábiles y, por tanto, químicamente útiles que pueden producirse fácilmente a partir de reactivos de partida disponibles comercialmente. Una ruta común para la producción de enaminas es a través de una reacción nucleofílica catalizada por ácido de especies cetonas [7] o aldehídos [8] que contienen un α-hidrógeno con aminas secundarias. La catálisis ácida no siempre es necesaria si el pK aH de la amina que reacciona es suficientemente alto (por ejemplo, pirrolidina , que tiene un pK aH de 11,26). Sin embargo, si el pK aH de la amina que reacciona es bajo, entonces se requiere catálisis ácida a través de los pasos de adición y deshidratación [9] ( los agentes deshidratantes comunes incluyen MgSO 4 y Na 2 SO 4 ). [10] Las aminas primarias generalmente no se utilizan para la síntesis de enaminas debido a la formación preferencial de especies de iminas termodinámicamente más estables. [11] La autocondensación de metilcetona es una reacción secundaria que se puede evitar mediante la adición de TiCl 4 [12] a la mezcla de reacción (para que actúe como eliminador de agua ). [13] [14] A continuación se muestra un ejemplo de un aldehído que reacciona con una amina secundaria para formar una enamina a través de un intermedio de carbinolamina :
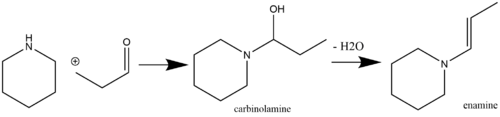
Aunque las enaminas son más nucleofílicas que sus homólogos enólicos, aún pueden reaccionar selectivamente, lo que las hace útiles para reacciones de alquilación. El nucleófilo de enamina puede atacar los haloalcanos para formar el intermedio de sal de iminio alquilado que luego se hidroliza para regenerar una cetona (un material de partida en la síntesis de enaminas). Esta reacción fue iniciada por Gilbert Stork , y a veces se hace referencia a ella con el nombre de su inventor (la alquilación de enamina de Stork ). De manera análoga, esta reacción se puede utilizar como un medio eficaz de acilación . En esta reacción se pueden utilizar una variedad de agentes alquilantes y acilantes, incluidos haluros alílicos y bencílicos. [15]

En una reacción muy similar a la alquilación de enaminas, las enaminas se pueden acilar para formar un producto dicarbonilo final . El material de partida de enamina sufre una adición nucleofílica a haluros de acilo formando el intermedio de sal de iminio que puede hidrolizarse en presencia de ácido. [dieciséis]

Se pueden usar bases fuertes como LiNR 2 para desprotonar iminas y formar metaloenaminas. Las metaloenaminas pueden resultar útiles sintéticamente debido a su nucleofilicidad (son más nucleófilas que los enolatos). Por lo tanto, son más capaces de reaccionar con electrófilos más débiles (por ejemplo, pueden usarse para abrir epóxidos . [17] ) Lo más destacado es que estas reacciones han permitido alquilaciones asimétricas de cetonas mediante la transformación en metaloenaminas intermedias quirales. [18]
Los compuestos de β-haloamonio se pueden sintetizar mediante la reacción de halogenación de enaminas con haluros en un disolvente de éter dietílico . La hidrólisis dará como resultado la formación de α-halocetonas. [19] Se ha demostrado que la cloración, la bromación e incluso la yodación son posibles. La reacción general se muestra a continuación:
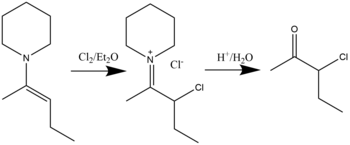
Las enaminas se pueden acoplar de manera cruzada con enol silanos mediante el tratamiento con nitrato de amonio cérico . Estas reacciones fueron informadas por el grupo Narasaka en 1975, proporcionando una ruta hacia enaminas estables, así como un caso de una 1,4-dicetona (derivada de un reactivo de amina morfolina ). [20] Posteriormente, estos resultados fueron explotados por el grupo MacMillan con el desarrollo de un organocatalizador que utilizaba los sustratos de Narasaka para producir 1,4 dicarbonilos enantioselectivamente, con buenos rendimientos. [21] La dimerización oxidativa de aldehídos en presencia de aminas se produce mediante la formación de una enamina seguida de una formación final de pirrol . [22] Este método para la síntesis simétrica de pirrol fue desarrollado en 2010 por el grupo Jia, como una nueva vía valiosa para la síntesis de productos naturales que contienen pirrol. [23]
La química de las enaminas se ha implementado con el fin de producir una versión enantioselectiva de un solo recipiente de la anulación de Robinson . La anulación de Robinson, publicada por Robert Robinson en 1935, es una reacción catalizada por bases que combina una cetona y una metil vinil cetona (comúnmente abreviada como MVK) para formar un sistema de anillos fusionados con ciclohexenona . Esta reacción puede ser catalizada por prolina para proceder a través de intermedios de enamina quirales que permiten una buena estereoselectividad. [24] Esto es importante, especialmente en el campo de la síntesis de productos naturales, por ejemplo, para la síntesis de la cetona de Wieland-Miescher , un componente vital para moléculas biológicamente activas más complejas. [25] [26]
Las enaminas actúan como nucleófilos que requieren menos activación ácido/base para su reactividad que sus homólogos enolatos. También se ha demostrado que ofrecen una mayor selectividad con menos reacciones secundarias. Existe un gradiente de reactividad entre los diferentes tipos de enaminas, y las cetonaenaminas ofrecen una mayor reactividad que sus homólogos aldehídos. [27] Las cetonaenaminas cíclicas siguen una tendencia de reactividad en la que el anillo de cinco miembros es el más reactivo debido a su conformación máximamente plana en el nitrógeno, siguiendo la tendencia 5>8>6>7 (el anillo de siete miembros es el menos reactivo). Esta tendencia se ha atribuido a la cantidad de carácter p en el orbital del par solitario del nitrógeno: el carácter p más alto corresponde a una mayor nucleofilicidad porque el orbital p permitiría la donación al orbital π del alqueno. De manera análoga, si el N par solitario participa en interacciones estereoelectrónicas en el resto amina, el par solitario saldrá del plano (se piramidalizará ) y comprometerá la donación en el enlace π CC adyacente. [28] [29]

Hay muchas formas de modular la reactividad de las enaminas además de alterar la estérica/electrónica en el centro de nitrógeno, incluido el cambio de temperatura, disolvente, cantidades de otros reactivos y tipo de electrófilo. El ajuste de estos parámetros permite la formación preferencial de enaminas E/Z y también afecta la formación de la enamina más/menos sustituida a partir del material de partida cetona. [30]
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ); Volúmenes recopilados , vol. 5, pág. 1014.