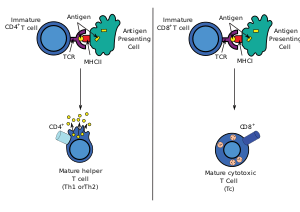
Una célula T citotóxica (también conocida como TC , linfocito T citotóxico , CTL , célula T asesina , célula T citolítica , célula T CD8 + o célula T asesina ) es un linfocito T (un tipo de glóbulo blanco ) que mata células cancerosas , células infectadas por patógenos intracelulares (como virus o bacterias) o células dañadas de otras maneras. [1]
La mayoría de las células T citotóxicas expresan receptores de células T (TCR) que pueden reconocer un antígeno específico . Un antígeno es una molécula capaz de estimular una respuesta inmunitaria y a menudo es producido por células cancerosas , virus, bacterias o señales intracelulares. Los antígenos dentro de una célula se unen a moléculas MHC de clase I y son llevados a la superficie de la célula por la molécula MHC de clase I, donde pueden ser reconocidos por la célula T. Si el TCR es específico para ese antígeno, se une al complejo de la molécula MHC de clase I y el antígeno, y la célula T destruye la célula.
Para que el TCR se una a la molécula MHC de clase I, el primero debe estar acompañado de una glicoproteína llamada CD8 , que se une a la porción constante de la molécula MHC de clase I. Por lo tanto, estas células T se denominan células T CD8 + .
La afinidad entre el CD8 y la molécula MHC mantiene a la célula T y a la célula diana estrechamente unidas durante la activación específica del antígeno. Las células T CD8 + se reconocen como células T una vez que se activan y generalmente se las clasifica como células que tienen una función citotóxica predefinida dentro del sistema inmunológico. Sin embargo, las células T CD8 + también tienen la capacidad de producir algunas citocinas , como el TNF-α y el IFN-γ , con efectos antitumorales y antimicrobianos.

El sistema inmunológico debe reconocer millones de antígenos potenciales. Hay menos de 30.000 genes en el cuerpo humano, por lo que es imposible tener un gen para cada antígeno. En lugar de eso, el ADN de millones de glóbulos blancos en la médula ósea se mezcla para crear células con receptores únicos, cada uno de los cuales puede unirse a un antígeno diferente. Algunos receptores se unen a los tejidos del propio cuerpo humano, por lo que para evitar que el cuerpo se ataque a sí mismo, esos glóbulos blancos autorreactivos se destruyen durante el desarrollo posterior en el timo , en el que el yodo es necesario para su desarrollo y actividad. [2]
Los TCR tienen dos partes, generalmente una cadena alfa y una beta. (Algunos TCR tienen una cadena gamma y una delta. Son inherentes a actuar contra el estrés y forman parte de la barrera epitelial [3] ). Las células madre hematopoyéticas en la médula ósea migran al timo , donde experimentan una recombinación V(D)J de su ADN TCR de cadena beta para formar una forma de desarrollo de la proteína TCR, conocida como pre-TCR. Si esa reorganización es exitosa, las células luego reorganizan su ADN TCR de cadena alfa para crear un complejo TCR alfa-beta funcional. Este producto de reordenamiento genético altamente variable en los genes TCR ayuda a crear millones de células T diferentes con diferentes TCR, lo que ayuda al sistema inmunológico del cuerpo a responder a prácticamente cualquier proteína de un invasor. La gran mayoría de las células T expresan TCR alfa-beta (células T αβ), pero algunas células T en tejidos epiteliales (como el intestino) expresan TCR gamma-delta ( células T gamma delta ), que reconocen antígenos no proteicos. Estas últimas se caracterizan por su capacidad para reconocer antígenos que no se presentan. Además, pueden reconocer proteínas de choque tóxico microbiano y proteínas de estrés de células propias. [4] Las células T γδ poseen una amplia plasticidad funcional tras reconocer células infectadas o transformadas, ya que son capaces de producir citocinas (IFN-γ, TNF-α, IL-17) y quimiocinas (IP-10, linfotactina), desencadenar la citólisis de células diana (perforinas, granzimas...), e interactuar con otras células, como células epiteliales, monocitos, células dendríticas, neutrófilos y células B. En algunas infecciones, como el citomegalovirus humano , hay una expansión clonal de células T γδ periféricas que tienen TCR específicos, lo que indica la naturaleza adaptativa de la respuesta inmune mediada por estas células. [5]
Las células T con TCR funcionalmente estables expresan tanto los correceptores CD4 como CD8 y, por lo tanto, se las denomina células T "doble positivas" (DP) (CD4 + CD8 + ). Las células T doblemente positivas están expuestas a una amplia variedad de autoantígenos en el timo y se someten a dos criterios de selección:
Sólo aquellas células T que se unen débilmente a los complejos de antígeno propio del MHC son seleccionadas positivamente. Las células que sobreviven a la selección positiva y negativa se diferencian en células T monopositivas (CD4 + o CD8 + ), dependiendo de si su TCR reconoce un antígeno presentado por el MHC de clase I (CD8) o un antígeno presentado por el MHC de clase II (CD4). Son las células T CD8 + las que madurarán y se convertirán en células T citotóxicas después de su activación con un antígeno restringido de clase I.
Las células T pasan por diferentes estadios, dependiendo del número de veces que han estado en contacto con el antígeno. En primer lugar, los linfocitos T naïve son aquellas células que aún no han encontrado un antígeno en el timo. A continuación, los linfocitos T se convierten en células T de memoria. Este tipo de células T son aquellas que han estado en contacto con el antígeno al menos una vez pero han vuelto posteriormente a un estado quiescente o inactivo, listas para responder de nuevo al antígeno contra el que fueron estimuladas. Finalmente, cuando se desencadena la respuesta inmune específica, estas células T naïve y de memoria se activan, dando lugar a las células T efectoras que tienen la capacidad de matar patógenos o células tumorales. [6] [7]
El umbral de activación de estas células es muy alto y el proceso puede ocurrir por dos vías: independiente del timo (por las células APC infectadas ) o dependiente del timo (por las células T CD4+ ). En la vía independiente del timo, debido a que la CPA está infectada, está altamente activada y expresa una gran cantidad de correceptores para la coactivación. Si las CPA no están infectadas, las células CD4 deben participar: ya sea para activar la CPA por coestimulación (más común) o para activar directamente la célula Tc mediante la secreción de IL-2 .
Si se produce la activación, el linfocito polariza sus gránulos hacia el lugar de la sinapsis y los libera, produciendo un “golpe letal”. En este punto, se separa de la célula diana y puede pasar a otra, y a otra más. La célula diana muere en unas 6 horas, normalmente por apoptosis. [8]
El MHC de clase I se expresa en todas las células huésped , excepto en las no nucleadas , como los eritrocitos . Cuando estas células se infectan con un patógeno intracelular , degradan proteínas extrañas mediante el procesamiento de antígenos . Esto da como resultado fragmentos de péptidos, algunos de los cuales son presentados por el MHC de clase I al receptor de antígeno de células T (TCR) en las células T CD8 + .
La activación de las células T citotóxicas depende de varias interacciones simultáneas entre las moléculas expresadas en la superficie de la célula T y las moléculas en la superficie de la célula presentadora de antígeno (CPA). Por ejemplo, considere el modelo de dos señales para la activación de las células T.
Una simple activación de células T CD8 + vírgenes requiere la interacción con células presentadoras de antígenos profesionales, principalmente con células dendríticas maduras . Para generar células T de memoria duraderas y permitir la estimulación repetitiva de células T citotóxicas, las células dendríticas tienen que interactuar tanto con células T auxiliares CD4 + activadas como con células T CD8 + . [9] [7] Durante este proceso, las células T auxiliares CD4 + "autorizan" a las células dendríticas para que den una señal activadora potente a las células T CD8 + vírgenes . [10] Esta autorización de las células presentadoras de antígenos por parte de las células T auxiliares CD4 + se produce mediante la señalización entre CD154/CD40L en la célula auxiliar T y el receptor CD40 en la célula presentadora de antígeno durante la formación de la sinapsis inmunológica. [11]
Si bien en la mayoría de los casos la activación depende del reconocimiento del antígeno por parte del TCR, se han descrito vías alternativas para la activación. Por ejemplo, se ha demostrado que las células T citotóxicas se activan cuando son atacadas por otras células T CD8, lo que lleva a la tolerización de estas últimas. [12]
Una vez activada, la célula T C experimenta una expansión clonal con la ayuda de la citocina interleucina 2 (IL-2), que es un factor de crecimiento y diferenciación de las células T. Esto aumenta el número de células específicas para el antígeno diana que luego pueden viajar por todo el cuerpo en busca de células somáticas positivas al antígeno .
Cuando se exponen a células somáticas infectadas/disfuncionales, las células T C liberan las citotoxinas perforina , granzimas y granulisina . A través de la acción de la perforina, las granzimas ingresan al citoplasma de la célula diana y su función de serina proteasa desencadena la cascada de caspasas , que es una serie de cisteína proteasas que finalmente conducen a la apoptosis (muerte celular programada). Esto se llama un "golpe letal" y permite observar una muerte en forma de onda de las células diana. [13] Debido al alto orden de lípidos y la fosfatidilserina cargada negativamente presente en su membrana plasmática, las células T C son resistentes a los efectos de sus citotoxinas perforina y granzima. [14]
Una segunda forma de inducir la apoptosis es a través de la interacción de la superficie celular entre el linfocitos T y la célula infectada. Cuando se activa un linfocitos T , comienza a expresar el ligando de la proteína de superficie FAS (FasL)(Apo1L)(CD95L), que puede unirse a las moléculas Fas (Apo1)(CD95) expresadas en la célula diana. Sin embargo, se cree que esta interacción Fas-ligando Fas es más importante para la eliminación de linfocitos T no deseados durante su desarrollo o para la actividad lítica de ciertas células TH que para la actividad citolítica de las células linfocitos T efectoras . La interacción de Fas con FasL permite el reclutamiento del complejo de señalización inducido por muerte (DISC). [15] El dominio de muerte asociado a Fas (FADD) se transloca con el DISC, lo que permite el reclutamiento de las procaspasas 8 y 10. [15] Estas caspasas luego activan las caspasas efectoras 3, 6 y 7, lo que lleva a la escisión de los sustratos de muerte como lamina A , lamina B1, lamina B2, PARP ( poli ADP ribosa polimerasa ) y DNA-PKcs (proteína quinasa activada por ADN). El resultado final es la apoptosis de la célula que expresó Fas. Las células T CD8 también pueden mostrar muerte celular inducida por activación o AICD, que está mediada por el complejo receptor CD3. Recientemente, se ha demostrado que una proteína TLT-1 liberada por plaquetas induce muerte celular similar a AICD en células T CD8 [16]
Se sugiere que el factor de transcripción Eomesodermina desempeña un papel clave en la función de las células T CD8 + , actuando como un gen regulador en la respuesta inmune adaptativa. [17] Los estudios que investigaron el efecto de la pérdida de función de Eomesodermina encontraron que una disminución en la expresión de este factor de transcripción resultó en una cantidad reducida de perforina producida por las células T CD8 + . [17]
A diferencia de los anticuerpos , que son eficaces contra infecciones virales y bacterianas , las células T citotóxicas son principalmente eficaces contra los virus. [18]
Durante la infección por el virus de la hepatitis B (VHB), las células T citotóxicas matan a las células infectadas y producen citocinas antivirales capaces de purgar el VHB de los hepatocitos viables. También desempeñan un papel patogénico importante, contribuyendo a casi la totalidad de la lesión hepática asociada con la infección por VHB. [19] Se ha demostrado que las plaquetas facilitan la acumulación de células T citotóxicas específicas del virus en el hígado infectado. [20] En algunos estudios con ratones, la inyección con células T CD8 + CXCR5 + mostró una disminución significativa de HBsAg . Además, un aumento de los niveles de CXCL13 facilitó el reclutamiento de células T CD8+ CXCR5+ intrahepáticas y, estos tipos de células produjeron altos niveles de interferón (IFN)-γ específico del VHB e IL-21 , que pueden ayudar a mejorar el control de la infección crónica por VHB. [21]
Las células T citotóxicas se han implicado en la progresión de la artritis . La principal implicación de la artritis reumatoide es su afectación articular. La membrana sinovial se caracteriza por hiperplasia , aumento de la vascularidad e infiltración de células inflamatorias; principalmente linfocitos T CD4+, que son los principales organizadores de las respuestas inmunitarias mediadas por células. En diferentes estudios, la artritis reumatoide está fuertemente vinculada a los antígenos del complejo mayor de histocompatibilidad (MHC) de clase II. Las únicas células del cuerpo que expresan antígenos MHC de clase II son las células presentadoras de antígenos constitutivas . Esto sugiere fuertemente que la artritis reumatoide es causada por antígenos artritogénicos no identificados. El antígeno podría ser cualquier antígeno exógeno, como proteínas virales, o una proteína endógena. [22] Recientemente, se han identificado varios posibles antígenos endógenos, por ejemplo, la glucoproteína 39 del cartílago humano, la proteína de unión a la cadena pesada y la proteína citrulinada. Los linfocitos T CD4+ activados estimulan a los monocitos, macrófagos y fibroblastos sinoviales para que elaboren las citocinas interleucina-1 , interleucina-6 y factor de necrosis tumoral alfa (TNFa), y para que secreten metaloproteinasas. Las tres primeras son clave para impulsar la inflamación en la artritis reumatoide. Estos linfocitos activados también estimulan a las células B para que produzcan inmunoglobulinas, incluido el factor reumatoide. [23] Su papel patogénico es desconocido, pero puede deberse a la activación del complemento a través de la formación de complejos inmunes. Además, varios estudios en animales sugieren que las células T citotóxicas pueden tener un efecto predominantemente proinflamatorio en la enfermedad. También se ha estudiado que la producción de citocinas por las células CD8+ puede acelerar el progreso de la enfermedad artrítica. [24]
Se ha descubierto que las células T CD8 + desempeñan un papel en la infección por VIH . Con el tiempo, el VIH ha desarrollado muchas estrategias para evadir el sistema inmunitario de la célula huésped. Por ejemplo, el VIH ha adoptado tasas de mutación muy altas para permitirles escapar del reconocimiento por parte de las células T CD8 + . [25] También son capaces de regular a la baja la expresión de las proteínas de superficie MHC de clase I de las células que infectan, con el fin de evadir aún más la destrucción por parte de las células T CD8 + . [25] Si las células T CD8 + no pueden encontrar, reconocer y unirse a las células infectadas, el virus no será destruido y seguirá creciendo.
Además, las células T CD8 + pueden estar implicadas en la diabetes tipo 1. [26] Estudios en un modelo de ratón diabético mostraron que las células CD4+ son responsables de la infiltración masiva de leucocitos mononucleares en los islotes pancreáticos . Sin embargo, se ha demostrado que las células CD8+ desempeñan un papel efector, responsable de la destrucción final de las células beta de los islotes. Sin embargo, en estudios con ratones NOD que portaban una mutación nula en el locus de beta-2 microglobulina (B2M) y, por lo tanto, carecían de moléculas de clase I del complejo mayor de histocompatibilidad y células T CD8+, se encontró que no desarrollaron diabetes. [27]
Las células T CD8 + pueden ser necesarias para resolver la neuropatía periférica inducida por quimioterapia (CIPN). [28] [29] Los ratones sin células T CD8 + muestran CIPN prolongada en comparación con los ratones normales y la inyección de células T CD8 + educadas resuelve o previene la CIPN.
Los linfocitos T citotóxicos se han implicado en el desarrollo de varias enfermedades y trastornos, por ejemplo en el rechazo de trasplantes (los linfocitos T citotóxicos atacan al nuevo órgano después de detectarlo como extraño, debido a la variación de HLA entre donante y receptor); [30] en la producción excesiva de citocinas en la infección grave por SARS-CoV-2 (debido a una respuesta linfocítica exagerada, se generan una gran cantidad de citocinas proinflamatorias , dañando al sujeto); [31] [32] enfermedades inflamatorias y degenerativas del sistema nervioso central, como la esclerosis múltiple (las células T se sensibilizan a ciertas proteínas, como la mielina , atacando a las células sanas y reclutando más células inmunes, agravando la enfermedad). [33]
Las células T colaboradoras/CD4+ •expresan glicoproteínas CD4 en su superficie celular, que se activan en presencia de antígenos peptídicos en la superficie de los patógenos invasores; •responden inmediatamente para proteger el sistema inmunológico; •secretan diferentes proteínas citoquinas según la respuesta inmune.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )