El dodecilsulfato de sodio ( SDS ) o laurilsulfato de sodio ( SLS ) , a veces escrito laurilsulfato de sodio , es un compuesto orgánico de fórmula CH3 (CH2 ) 11OSO3Na y estructura H3C− ( CH2 ) 11 − O− . S(=O) 2 −O − Na + . Es un tensioactivo aniónico utilizado en muchos productos de limpieza e higiene. Este compuesto es la sal sódica del organosulfato de 12 carbonos . Su cola de hidrocarburo combinada con un " grupo de cabeza " polar le da al compuesto propiedades anfifílicas que lo hacen útil como detergente . El SDS también forma parte de mezclas producidas a partir de aceites económicos de coco y palma . El SDS es un componente común de muchos productos de limpieza doméstica, higiene personal y cosméticos, farmacéuticos y alimenticios, así como de formulaciones de productos y limpieza industriales y comerciales. [2]

La concentración micelar crítica (CMC) en agua a 25 °C es 8,2 mM, [1] y el número de agregación a esta concentración generalmente se considera aproximadamente 62. [3] La fracción de ionización micelar (α) es de aproximadamente 0,3 (o 30%). [4]
El SDS se utiliza principalmente en detergentes para ropa con muchas aplicaciones de limpieza. [5] Es un tensioactivo de gran eficacia y se utiliza en cualquier tarea que requiera la eliminación de manchas y residuos aceitosos. Por ejemplo, se encuentra en concentraciones más altas en productos industriales, incluidos desengrasantes de motores, limpiadores de pisos y limpiadores exteriores de automóviles. [ cita necesaria ]
Es un componente de jabones de manos, pastas de dientes, champús, cremas de afeitar y formulaciones de baños de burbujas , por su capacidad para crear espuma, por sus propiedades tensioactivas y en parte por su efecto espesante. [6]
El dodecilsulfato de sodio, que aparece como sinónimo de laurilsulfato de sodio (SLS), se considera un ingrediente generalmente reconocido como seguro (GRAS) para uso alimentario según la USFDA (21 CFR 172.822). [7] Se utiliza como agente emulsionante y ayuda para batir. [8] Como emulsionante en o con claras de huevo, el Código de Regulaciones Federales de los Estados Unidos exige que no supere las 1.000 partes por millón (0,1%) en sólidos de clara de huevo o las 125 partes por millón (0,0125%) en huevos congelados o líquidos. claras y como batidor para la preparación de malvaviscos no debe exceder el 0,5% del peso de gelatina. [9] Se informa que el SLS disminuye temporalmente la percepción de dulzura. [10]
El SDS se utiliza en procedimientos de limpieza [11] y se utiliza comúnmente como componente para lisar células durante la extracción de ARN o ADN , y para desnaturalizar proteínas en preparación para la electroforesis en la técnica SDS-PAGE . [12]
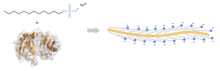
En el caso de SDS-PAGE, el compuesto actúa rompiendo los enlaces no covalentes de las proteínas y desnaturalizándolas, es decir, provocando que las moléculas de proteínas pierdan sus conformaciones y formas nativas. Al unirse a las proteínas en una proporción de una molécula de SDS por cada 2 residuos de aminoácidos, el detergente cargado negativamente proporciona a todas las proteínas una carga negativa neta similar y, por lo tanto, una relación carga-masa similar. [13] De esta manera, la diferencia en la movilidad de las cadenas polipeptídicas en el gel se puede atribuir únicamente a su longitud en contraposición a su carga y forma nativas. [13] [14] Esta separación basada en el tamaño de la cadena polipeptídica simplifica el análisis de las moléculas de proteínas. [15]
El lauril sulfato de sodio es ampliamente utilizado en el campo farmacéutico como solubilizante y emulsionante iónico adecuado para aplicaciones en dispersiones líquidas, soluciones, emulsiones y microemulsiones, tabletas, espumas y semisólidos como cremas, lociones y geles. [16] Además, SLS ayuda a la humectabilidad de las tabletas, así como a la lubricación durante la fabricación. Las marcas comerciales de SLS de calidad farmacéutica incluyen Kolliphor SLS y Kolliphor SLS Fine. [17]
SLS se utiliza en una técnica mejorada para preparar tejidos cerebrales para su estudio mediante microscopía óptica. La técnica, que ha sido bautizada como CLARITY, fue obra de Karl Deisseroth y sus compañeros de trabajo en la Universidad de Stanford , e implica la infusión del órgano con una solución de acrilamida para unir las macromoléculas del órgano ( proteínas , ácidos nucleicos , etc.), seguido mediante polimerización térmica para formar un "cerebro-hidrogel" (una malla intercalada por todo el tejido para fijar las macromoléculas y otras estructuras en el espacio), y luego mediante la eliminación de lípidos utilizando SDS para eliminar la dispersión de la luz con una pérdida mínima de proteínas, haciendo que el tejido sea cuasi- transparente. [18] [19]
Junto con el dodecilbencenosulfonato de sodio y Triton X-100 , las soluciones acuosas de SDS son populares para dispersar o suspender nanotubos, como los nanotubos de carbono . [20]
El SLS se ha propuesto como un microbicida tópico potencialmente eficaz, para uso intravaginal, para inhibir y posiblemente prevenir la infección por varios virus con y sin envoltura, como los virus del herpes simple , el VIH y el virus del bosque de Semliki . [21] [22]
Se ha demostrado que las membranas líquidas formadas a partir de SDS en agua funcionan como separadores de partículas inusuales. [23] El dispositivo actúa como un filtro inverso, permitiendo el paso de partículas grandes mientras captura partículas más pequeñas.
El SDS se sintetiza tratando alcohol laurílico con trióxido de azufre , óleum o ácido clorosulfúrico para producir lauril sulfato de hidrógeno. [24] El alcohol laurílico se puede utilizar en forma pura o como mezclas de alcoholes grasos. Cuando se producen a partir de estas fuentes, los productos "SDS" son una mezcla de varios alquilsulfatos de sodio , siendo el SDS el componente principal. [25] Por ejemplo, el SDS es un componente, junto con otros anfífilos de longitud de cadena , cuando se produce a partir de aceite de coco, y se conoce como cocosulfato de sodio (SCS). [26] El SDS está disponible comercialmente en polvo, gránulos y otras formas (cada una de las cuales difiere en sus velocidades de disolución), así como en soluciones acuosas de diferentes concentraciones. [ cita necesaria ]
Según algunos estudios [ se necesita aclaración ] , el SDS no es cancerígeno en bajas concentraciones . [27] [28] Como todos los detergentes , el lauril sulfato de sodio elimina la grasa de la piel y puede causar irritación de la piel y los ojos. [ cita necesaria ] Se ha demostrado que irrita la piel del rostro, con exposición prolongada y constante (más de una hora) en adultos jóvenes. [29] El SDS puede empeorar los problemas de la piel en personas con hipersensibilidad cutánea crónica , y algunas personas se ven afectadas más que otras. [30] [31] [32]
El SDS es un ingrediente común en las pastas dentales debido a su bajo costo, [33] su falta de impacto en el sabor, [33] y su acción deseable como agente espumante. [33]
El SDS puede reducir la cantidad de mal aliento , que causa compuestos volátiles de azufre (VSC, por sus siglas en inglés) en la boca. [34] Una serie de pequeños estudios cruzados (25 a 34 pacientes) han respaldado la eficacia del SLS en la reducción de las VSC y su impacto positivo relacionado sobre el mal aliento, aunque en general se ha observado que estos estudios reflejan desafíos técnicos en el control. de las variables del diseño del estudio. [34]
Fuentes primarias del grupo de Irma Rantanen de la Universidad de Turku , Finlandia, afirman que las pastas que contienen SLS causan más sequedad de boca ( xerostomía ) que la alternativa propuesta. Sin embargo, una revisión Cochrane de 2011 de estos estudios, y del área más general, concluye que "no hay evidencia sólida... de que alguna terapia tópica sea efectiva para aliviar el síntoma de sequedad de boca". [35]
Se ha planteado una preocupación de seguridad sobre la base de varios estudios sobre el efecto de la pasta de dientes SDS en las úlceras aftosas (más específicamente, úlceras bucales o "aftas"), comúnmente conocidas como aftas o llagas blancas. [33] Según el NHS, el SLS es motivo de preocupación para las úlceras bucales. [36] [37] Como señala Lippert en 2013, "muy pocas... pastas dentales comercializadas contienen un tensioactivo distinto del SLS [SDS]", y los principales fabricantes continúan formulando sus productos con SDS. [33]
Obtener información de alta resolución de un sistema complejo, manteniendo al mismo tiempo la perspectiva global necesaria para comprender el funcionamiento del sistema, representa un desafío clave en biología.
Aquí abordamos este desafío con un método (denominado CLARIDAD) para la transformación de tejido intacto en una forma nanoporosa hibridada con hidrogel (entrecruzada a una red tridimensional de polímeros hidrófilos) que está completamente ensamblada pero es ópticamente transparente y permeable a las macromoléculas.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) Mantenimiento de CS1: varios nombres: lista de autores ( enlace )[ página necesaria ][Citando:] Carcinogénesis.
Un estudio oral crónico de un año de duración con beagles demostró que el laurilsulfato de sodio en concentraciones de hasta el 2% en la dieta no era tumorigénico ni cancerígeno.
[pag.
157] / Resumen… En estudios de mutagénesis, las ratas alimentadas con 1,13% y 0,56% de lauril sulfato de sodio en la dieta durante 90 días no produjeron más aberraciones cromosómicas ni efectos clastogénicos que una dieta de control.
[pag.
175].
/ Conclusión.
El lauril sulfato de sodio y el lauril sulfato de amonio parecen ser seguros en formulaciones diseñadas para un uso breve y discontinuo seguido de un enjuague minucioso de la superficie de la piel.
En productos destinados a un contacto prolongado con la piel, las concentraciones no deben exceder el 1%.
[pag.
176.].
[Cita:] El lauril sulfato de sodio y el lauril sulfato de amonio parecen ser seguros en formulaciones diseñadas para un uso breve y discontinuo seguido de un enjuague minucioso de la superficie de la piel.
En productos destinados a un contacto prolongado con la piel, las concentraciones no deben exceder el 1%... Nuevos estudios confirmaron las propiedades irritantes de estos ingredientes y reforzaron el límite de concentración del 1% o usos sin aclarado establecido por el Panel [anterior].
[pag.
89] / Los estudios disponibles que buscaron carcinogénesis no lograron encontrar evidencia de que el lauril sulfato de amonio sea [sic.] cancerígeno.
Ninguno de los datos disponibles sugirió que el SLS o el lauril sulfato de amonio pudieran ser cancerígenos.
A pesar de que en Internet se afirma lo contrario, la carcinogenicidad de estos ingredientes es sólo un rumor.
[páginas.
89 y siguientes]
{{cite journal}}: Mantenimiento CS1: varios nombres: lista de autores ( enlace ).[Resumen de citas:] No hay pruebas sólidas de esta revisión de que algún tratamiento tópico sea eficaz para aliviar el síntoma de sequedad bucal.Véase Rantanen, et al. (2003) J. Contemp. Mella. Practica. 4 (2): 11–23, [1], y Rantanen, et al. (2003) sueco. Mella. J. 27 (1): 31–34, [2], al que se hace referencia allí.
No utilice pasta de dientes que contenga lauril sulfato de sodio.