
Un gas respirable es una mezcla de elementos y compuestos químicos gaseosos utilizados para la respiración . El aire es el gas respirable más común y el único natural, pero también se utilizan otras mezclas de gases u oxígeno puro en equipos de respiración y hábitats cerrados. El oxígeno es el componente esencial de cualquier gas respirable. Los gases respirables para uso hiperbárico se han desarrollado para mejorar el rendimiento del aire ordinario al reducir el riesgo de enfermedad por descompresión , reducir la duración de la descompresión , reducir la narcosis por nitrógeno o permitir un buceo profundo más seguro .
Un gas respirable es una mezcla de elementos y compuestos químicos gaseosos utilizados para la respiración . El aire es el gas respirable más común y el único natural. Otras mezclas de gases, u oxígeno puro , también se utilizan en equipos de respiración y hábitats cerrados como equipos de buceo , equipos de buceo de superficie , cámaras de recompresión , montañismo a gran altitud , aviones de alto vuelo , submarinos , trajes espaciales , naves espaciales , vida médica. equipos de soporte y primeros auxilios , y máquinas de anestesia . [1] [2] [3]
El oxígeno es el componente esencial de cualquier gas respirable, a una presión parcial de entre aproximadamente 0,16 y 1,60 bar a la presión ambiente , ocasionalmente más baja para el montañismo a gran altura , o más alta para el tratamiento con oxígeno hiperbárico . El oxígeno suele ser el único componente metabólicamente activo , a menos que el gas sea una mezcla anestésica. Parte del oxígeno del gas respirable se consume en los procesos metabólicos y los componentes inertes no cambian y sirven principalmente para diluir el oxígeno a una concentración adecuada, por lo que también se conocen como gases diluyentes.
Por lo tanto, la mayoría de los gases respirables son una mezcla de oxígeno y uno o más gases metabólicamente inertes . [1] [3] Los gases respiratorios para uso hiperbárico se han desarrollado para mejorar el rendimiento del aire ordinario al reducir el riesgo de enfermedad por descompresión , reducir la duración de la descompresión , reducir la narcosis por nitrógeno o permitir un buceo profundo más seguro . [1] [3] Las técnicas utilizadas para llenar cilindros de buceo con gases distintos del aire se denominan mezcla de gases . [4] [5]
Los gases respirables para uso a presiones ambientales por debajo de la presión atmosférica normal suelen ser oxígeno puro o aire enriquecido con oxígeno para proporcionar suficiente oxígeno para mantener la vida y la conciencia, o para permitir niveles de esfuerzo más altos que los que serían posibles usando aire. Es común proporcionar oxígeno adicional como un gas puro agregado al aire respirable al inhalarlo o mediante un sistema de soporte vital.

Un gas respirable seguro para uso hiperbárico tiene cuatro características esenciales:
Se utilizan estos gases respirables comunes para buceo:
El aire respirable es aire atmosférico con un estándar de pureza adecuado para la respiración humana en la aplicación especificada. Para uso hiperbárico, la presión parcial de los contaminantes aumenta en proporción a la presión absoluta, y debe limitarse a una composición segura para la profundidad o rango de presión en el que se va a utilizar.
Los gases respirables para el buceo se clasifican por fracción de oxígeno. Los límites establecidos por las autoridades pueden diferir ligeramente, ya que los efectos varían gradualmente con la concentración y entre las personas, y no son predecibles con precisión. [ cita necesaria ]
Los gases respirables para el buceo se mezclan a partir de una pequeña cantidad de gases componentes que proporcionan a la mezcla características especiales que no están disponibles en el aire atmosférico.
El oxígeno (O 2 ) debe estar presente en cada gas respirable. [1] [2] [3] Esto se debe a que es esencial para el proceso metabólico del cuerpo humano , que sustenta la vida. El cuerpo humano no puede almacenar oxígeno para su uso posterior como lo hace con los alimentos. Si el cuerpo se ve privado de oxígeno durante más de unos minutos, se produce la pérdida del conocimiento y la muerte. Los tejidos y órganos del cuerpo (en particular, el corazón y el cerebro) resultan dañados si se les priva de oxígeno durante más de cuatro minutos.
Llenar una botella de buceo con oxígeno puro cuesta aproximadamente cinco veces más que llenarla con aire comprimido. Como el oxígeno favorece la combustión y provoca oxidación en los cilindros de buceo , se debe manipular con precaución al mezclar gases . [4] [5]
Históricamente, el oxígeno se ha obtenido mediante destilación fraccionada de aire líquido , pero cada vez más se obtiene mediante tecnologías no criogénicas, como las tecnologías de adsorción por cambio de presión (PSA) y de adsorción por cambio de vacío (VSA). [20]
La fracción del componente de oxígeno de una mezcla de gases respirables a veces se utiliza al nombrar la mezcla:
La fracción de oxígeno determina la mayor profundidad a la que se puede utilizar la mezcla de forma segura para evitar la toxicidad del oxígeno . Esta profundidad se denomina profundidad operativa máxima . [1] [3] [7] [10]
La concentración de oxígeno en una mezcla de gases depende de la fracción y la presión de la mezcla. Se expresa por la presión parcial de oxígeno (P O 2 ). [1] [3] [7] [10]
La presión parcial de cualquier gas componente en una mezcla se calcula como:
Para el componente de oxígeno,
dónde:
La presión parcial mínima segura de oxígeno en un gas respirable suele ser de 16 kPa (0,16 bar). Por debajo de esta presión parcial, el buzo puede correr riesgo de pérdida del conocimiento y muerte debido a hipoxia , dependiendo de factores que incluyen la fisiología individual y el nivel de esfuerzo. Cuando se respira una mezcla hipóxica en aguas poco profundas, es posible que no tenga una P O 2 lo suficientemente alta como para mantener consciente al buceador. Por esta razón, los "gases de viaje" normóxicos o hiperóxicos se utilizan a profundidades medias entre las fases de "fondo" y "descompresión" de la inmersión.
La P O 2 máxima segura en un gas respirable depende del tiempo de exposición, el nivel de ejercicio y la seguridad del equipo respiratorio que se utiliza. Normalmente está entre 100 kPa (1 bar) y 160 kPa (1,6 bar); para inmersiones de menos de tres horas se considera comúnmente que es 140 kPa (1,4 bar), aunque se sabe que la Marina de los EE. UU. autoriza inmersiones con una P O 2 de hasta 180 kPa (1,8 bar). [1] [2] [3] [7] [10] En caso de P O 2 elevado o exposiciones más prolongadas, el buceador corre el riesgo de sufrir toxicidad por oxígeno, lo que puede provocar una convulsión . [1] [2] Cada gas respirable tiene una profundidad operativa máxima que está determinada por su contenido de oxígeno. [1] [2] [3] [7] [10] Para la recompresión terapéutica y la oxigenoterapia hiperbárica se utilizan habitualmente presiones parciales de 2,8 bar en la cámara, pero no hay riesgo de ahogamiento si el ocupante pierde el conocimiento. [2] Para períodos más largos, como en el buceo de saturación , se pueden tolerar 0,4 bar durante varias semanas.
Los analizadores de oxígeno se utilizan para medir la presión parcial de oxígeno en la mezcla de gases. [4]
Divox es oxígeno de grado respirable etiquetado para uso en buceo. En los Países Bajos , el oxígeno puro para respirar se considera medicinal, a diferencia del oxígeno industrial, como el que se utiliza en la soldadura , y sólo está disponible bajo prescripción médica . La industria del buceo registró Divox como marca comercial de oxígeno respirable para eludir las estrictas normas relativas al oxígeno medicinal, facilitando así a los buceadores (recreativos) obtener oxígeno para mezclar su gas respirable. En la mayoría de los países, no existe diferencia en la pureza del oxígeno médico y el oxígeno industrial, ya que se producen exactamente con los mismos métodos y fabricantes, pero se etiquetan y llenan de manera diferente. La principal diferencia entre ellos es que el rastro de registro es mucho más extenso para el oxígeno medicinal, para identificar más fácilmente el rastro exacto de fabricación de un "lote" de oxígeno, en caso de que se descubran problemas con su pureza. El oxígeno de grado aeronáutico es similar al oxígeno médico, pero puede tener un menor contenido de humedad. [4]
Para diluir el gas se utilizan gases que no tienen función metabólica en el gas respirable y, por tanto, se clasifican como gases diluyentes. Algunos de ellos tienen un efecto narcótico reversible a presión parcial elevada, por lo que deben limitarse para evitar efectos narcóticos excesivos a la presión máxima a la que se pretende respirar. Los gases diluyentes también afectan la densidad de la mezcla de gases y, por tanto, el trabajo respiratorio .
El nitrógeno (N 2 ) es un gas diatómico y el componente principal del aire , el gas respirable más barato y más común utilizado para el buceo. Provoca narcosis por nitrógeno en el buceador, por lo que su uso se limita a inmersiones a poca profundidad. El nitrógeno puede causar enfermedad por descompresión . [1] [2] [3] [21]
La profundidad de aire equivalente se utiliza para estimar los requisitos de descompresión de una mezcla de nitrox (oxígeno/nitrógeno). Se utiliza una profundidad narcótica equivalente para estimar la potencia narcótica de trimix (mezcla de oxígeno/helio/nitrógeno). Muchos buceadores consideran que el nivel de narcosis causado por una inmersión de 30 m (100 pies), mientras respiran aire, es un máximo confortable. [1] [2] [3] [22] [23]
El nitrógeno en una mezcla de gases casi siempre se obtiene agregando aire a la mezcla.

El helio (He) es un gas inerte que es menos narcótico que el nitrógeno a presión equivalente (de hecho, no hay ninguna evidencia de narcosis por helio) y tiene una densidad mucho menor, por lo que es más adecuado para inmersiones más profundas que nitrógeno. [1] [3] El helio es igualmente capaz de causar enfermedad por descompresión . A altas presiones, el helio también causa el síndrome nervioso de alta presión , que es un síndrome de irritación del sistema nervioso central que en cierto modo es opuesto a la narcosis. [1] [2] [3] [24]
Los rellenos con mezcla de helio son considerablemente más caros que los rellenos con aire debido al costo del helio y al costo de mezclar y comprimir la mezcla. [ cita necesaria ]
El helio no es adecuado para inflar trajes secos debido a sus malas propiedades de aislamiento térmico : en comparación con el aire, que se considera un aislante razonable, el helio tiene una conductividad térmica seis veces mayor. [25] El bajo peso molecular del helio (PM monoatómico = 4, en comparación con el nitrógeno diatómico PM = 28) aumenta el timbre de la voz de quien respira, lo que puede impedir la comunicación. [1] [3] [26] Esto se debe a que la velocidad del sonido es más rápida en un gas de menor peso molecular, lo que aumenta la frecuencia de resonancia de las cuerdas vocales. [1] [26] El helio se escapa de válvulas dañadas o defectuosas más fácilmente que otros gases porque los átomos de helio son más pequeños, lo que les permite pasar a través de espacios más pequeños en los sellos .
El helio se encuentra en cantidades importantes únicamente en el gas natural , del que se extrae a bajas temperaturas mediante destilación fraccionada.
El neón (Ne) es un gas inerte que a veces se utiliza en el buceo comercial profundo , pero es muy caro. [1] [3] [11] [17] Al igual que el helio, es menos narcótico que el nitrógeno, pero a diferencia del helio, no distorsiona la voz del buceador. Comparado con el helio, el neón tiene propiedades de aislamiento térmico superiores. [27]
El hidrógeno (H 2 ) se ha utilizado en mezclas de gases para buceo profundo, pero es muy explosivo cuando se mezcla con más de un 4 a 5 % de oxígeno (como el oxígeno que se encuentra en el gas respirable). [1] [3] [11] [14] Esto limita el uso de hidrógeno en inmersiones profundas e impone protocolos complicados para garantizar que el exceso de oxígeno se elimine del equipo de respiración antes de que comience a respirar hidrógeno. Al igual que el helio, eleva el timbre de la voz del buceador. La mezcla de hidrógeno y oxígeno, cuando se utiliza como gas de buceo, a veces se denomina Hydrox . Las mezclas que contienen hidrógeno y helio como diluyentes se denominan Hydreliox.
Muchos gases no son adecuados para su uso en gases respirables de buceo. [5] [28] Aquí hay una lista incompleta de gases comúnmente presentes en un ambiente de buceo:
El argón (Ar) es un gas inerte que es más narcótico que el nitrógeno, por lo que generalmente no es adecuado como gas respirable para buceo. [29] Argox se utiliza para la investigación de la descompresión. [1] [3] [30] [31] A veces lo utilizan buzos cuyo principal gas respirable es a base de helio para inflar trajes secos , debido a las buenas propiedades de aislamiento térmico del argón. El argón es más caro que el aire o el oxígeno, pero considerablemente menos que el helio. El argón es un componente del aire natural y constituye el 0,934% en volumen de la atmósfera terrestre. [32]
El dióxido de carbono (CO 2 ) es producido por el metabolismo del cuerpo humano y puede provocar intoxicación por dióxido de carbono . [28] [33] [34] Cuando el gas respirable se recicla en un rebreather o en un sistema de soporte vital , los depuradores eliminan el dióxido de carbono antes de reutilizar el gas.
El monóxido de carbono (CO) es un gas altamente tóxico que compite con el dioxígeno por unirse a la hemoglobina, evitando así que la sangre transporte oxígeno (ver intoxicación por monóxido de carbono ). Generalmente se produce por una combustión incompleta . [1] [2] [5] [28] Cuatro fuentes comunes son:
Generalmente se evita el monóxido de carbono en la medida de lo posible colocando la entrada de aire en aire no contaminado, filtrando las partículas del aire de entrada, utilizando un diseño de compresor adecuado y lubricantes apropiados, y asegurando que las temperaturas de funcionamiento no sean excesivas. Cuando el riesgo residual es excesivo, se puede utilizar un catalizador de hopcalita en el filtro de alta presión para convertir el monóxido de carbono en dióxido de carbono, que es mucho menos tóxico.
Los hidrocarburos (C x H y ) están presentes en los lubricantes y combustibles para compresores . Pueden ingresar a los cilindros de buceo como resultado de contaminación, fugas, [ se necesita aclaración ] o debido a una combustión incompleta cerca de la entrada de aire. [2] [4] [5] [28] [35]
El proceso de comprimir gas en un cilindro de buceo elimina la humedad del gas. [5] [28] Esto es bueno para prevenir la corrosión en el cilindro, pero significa que el buzo inhala gas muy seco. El gas seco extrae la humedad de los pulmones del buzo mientras está bajo el agua, lo que contribuye a la deshidratación , que también se cree que es un factor de riesgo predisponente a la enfermedad por descompresión . También es incómodo, provoca sequedad de boca y garganta y provoca sed en el buceador. Este problema se reduce en los rebreathers porque la reacción de cal sodada , que elimina el dióxido de carbono, también devuelve humedad al gas respirable, [9] y la humedad relativa y la temperatura del gas exhalado son relativamente altas y hay un efecto acumulativo debido a la reinhalación. . [37] En climas cálidos, el buceo en circuito abierto puede acelerar el agotamiento por calor debido a la deshidratación. Otra preocupación con respecto al contenido de humedad es la tendencia de la humedad a condensarse a medida que el gas se descomprime mientras pasa por el regulador; esto sumado a la reducción extrema de temperatura, también debido a la descompresión, puede hacer que la humedad se solidifique en forma de hielo. Esta formación de hielo en un regulador puede provocar que las piezas móviles se atasquen y que el regulador falle o fluya libremente. Esta es una de las razones por las que los reguladores de buceo generalmente se construyen con latón y cromados (para protección). El latón, con sus buenas propiedades de conducción térmica, conduce rápidamente el calor del agua circundante al aire frío recién descomprimido, lo que ayuda a evitar la formación de hielo.

Las mezclas de gases generalmente deben analizarse durante el proceso o después de la mezcla para control de calidad. Esto es particularmente importante para mezclas de gases respirables donde los errores pueden afectar la salud y la seguridad del usuario final. Es difícil detectar la mayoría de los gases que probablemente estén presentes en las botellas de buceo porque son incoloros, inodoros e insípidos. Existen sensores electrónicos para algunos gases, como analizadores de oxígeno , analizadores de helio , detectores de monóxido de carbono y detectores de dióxido de carbono . [2] [4] [5] Los analizadores de oxígeno se encuentran comúnmente bajo el agua en rebreathers . [9] Los analizadores de oxígeno y helio se utilizan a menudo en la superficie durante la mezcla de gases para determinar el porcentaje de oxígeno o helio en una mezcla de gases respirables. [4] Los métodos químicos y de otro tipo de detección de gases no se utilizan con frecuencia en el buceo recreativo, pero se utilizan para pruebas periódicas de calidad del aire respirable comprimido de los compresores de aire de buceo. [4]
Las normas para la calidad del gas respirable son publicadas por organizaciones nacionales e internacionales y pueden hacerse cumplir en términos de legislación. En el Reino Unido, el Ejecutivo de Salud y Seguridad indica que los requisitos para los gases respirables de los buceadores se basan en la norma BS EN 12021:2014. Las especificaciones se enumeran para aire compatible con oxígeno, mezclas de nitrox producidas agregando oxígeno, eliminando nitrógeno o mezclando nitrógeno y oxígeno, mezclas de helio y oxígeno (heliox), mezclas de helio, nitrógeno y oxígeno (trimix) y oxígeno puro, para tanto en circuito abierto como en sistemas de recuperación, y para suministro de alta y baja presión (suministro por encima y por debajo de 40 bar). [38]
El contenido de oxígeno es variable dependiendo de la profundidad de operación, pero la tolerancia depende del rango de fracción de gas, siendo ±0,25% para una fracción de oxígeno inferior al 10% en volumen, ±0,5% para una fracción entre 10% y 20%, y ±1 % para una fracción superior al 20%. [38]
El contenido de agua está limitado por los riesgos de formación de hielo en las válvulas de control y la corrosión de las superficies de contención (una mayor humedad no es un problema fisiológico) y generalmente es un factor del punto de rocío . [38]
Otros contaminantes específicos son el dióxido de carbono, el monóxido de carbono, el petróleo y los hidrocarburos volátiles, que están limitados por sus efectos tóxicos. Otros posibles contaminantes deben analizarse basándose en la evaluación de riesgos, y la frecuencia requerida de pruebas para detectar contaminantes también se basa en la evaluación de riesgos. [38]
En Australia, la calidad del aire respirable está especificada en la norma australiana 2299.1, Sección 3.13 Calidad del gas respirable. [39]


La mezcla de gases (o mezcla de gases) de gases respirables para buceo es el llenado de cilindros de gas con gases respirables distintos del aire .
Llenar botellas con una mezcla de gases presenta peligros tanto para el llenador como para el buceador. Durante el llenado existe riesgo de incendio debido al uso de oxígeno y riesgo de explosión debido al uso de gases a alta presión. La composición de la mezcla debe ser segura para la profundidad y duración de la inmersión planificada. Si la concentración de oxígeno es demasiado pobre el buzo puede perder el conocimiento debido a la hipoxia y si es demasiado rica el buceador puede desarrollar toxicidad por oxígeno . Se planifica y controla la concentración de gases inertes, como nitrógeno y helio, para evitar la narcosis por nitrógeno y la enfermedad de descompresión.
Los métodos utilizados incluyen el mezclado por lotes mediante presión parcial o por fracción de masa, y procesos de mezclado continuo. Las mezclas completadas se analizan para determinar su composición para la seguridad del usuario. La legislación puede exigir que los mezcladores de gas demuestren su competencia si llenan para otras personas.
La densidad excesiva de un gas respirable puede aumentar el trabajo respiratorio a niveles intolerables y puede provocar retención de dióxido de carbono a densidades más bajas. [6] El helio se utiliza como componente para reducir la densidad y para reducir la narcosis en profundidad. Al igual que la presión parcial, la densidad de una mezcla de gases es proporcional a la fracción volumétrica de los gases que la componen y a la presión absoluta. Las leyes de los gases ideales son suficientemente precisas para gases a presiones respirables.
La densidad de una mezcla de gases a una temperatura y presión determinadas se puede calcular como:
dónde
Dado que la fracción de gas F i (fracción volumétrica) de cada gas se puede expresar como V i / (V 1 + V 2 + ... + V n )
por sustitución,

Los gases respirables para uso a presión ambiental reducida se utilizan en vuelos a gran altitud en aviones sin presión , en vuelos espaciales , particularmente en trajes espaciales , y en montañismo a gran altura . En todos estos casos, la consideración principal es proporcionar una presión parcial de oxígeno adecuada. En algunos casos, al gas respirable se le agrega oxígeno para lograr una concentración suficiente y, en otros casos, el gas respirable puede ser oxígeno puro o casi puro. Se pueden utilizar sistemas de circuito cerrado para conservar el gas respirable, que puede ser limitado: en el caso del montañismo, el usuario debe llevar oxígeno suplementario, y en los vuelos espaciales el coste de poner la masa en órbita es muy alto.
El uso médico de gases respirables distintos del aire incluye oxigenoterapia y aplicaciones de anestesia.

Las personas necesitan oxígeno para el metabolismo celular normal . [41] El aire suele contener un 21% de oxígeno en volumen. [42] Esto normalmente es suficiente, pero en algunas circunstancias el suministro de oxígeno a los tejidos se ve comprometido.
La oxigenoterapia , también conocida como oxígeno suplementario, es el uso de oxígeno como tratamiento médico . [43] Esto puede incluir niveles bajos de oxígeno en la sangre , toxicidad por monóxido de carbono , dolores de cabeza en racimos y para mantener suficiente oxígeno mientras se administran anestésicos inhalados . [44] El oxígeno a largo plazo suele ser útil en personas con niveles crónicamente bajos de oxígeno, como por ejemplo por EPOC grave o fibrosis quística . [45] [43] El oxígeno se puede administrar de varias maneras, incluida una cánula nasal , una mascarilla y dentro de una cámara hiperbárica . [46] [47]
Las altas concentraciones de oxígeno pueden causar toxicidad por oxígeno , como daño pulmonar o insuficiencia respiratoria en personas predispuestas. [44] [42] También puede secar la nariz y aumentar el riesgo de incendios en quienes fuman . El objetivo de saturación de oxígeno recomendado depende de la afección que se esté tratando. En la mayoría de las condiciones se recomienda una saturación del 94-98%, mientras que en aquellos con riesgo de retención de dióxido de carbono se prefieren saturaciones del 88-92%, y en aquellos con toxicidad por monóxido de carbono o paro cardíaco la saturación debe ser lo más alta posible. [43]
El uso de oxígeno en medicina se volvió común alrededor de 1917. [48] [49] Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud . [50] [51] El costo del oxígeno en el hogar es de aproximadamente 150 dólares estadounidenses al mes en Brasil y 400 dólares estadounidenses al mes en los Estados Unidos. [45] El oxígeno doméstico puede ser proporcionado mediante tanques de oxígeno o un concentrador de oxígeno . [43] Se cree que el oxígeno es el tratamiento más común administrado en los hospitales del mundo desarrollado . [52] [43]


El enfoque más común de la anestesia general es mediante el uso de anestésicos generales inhalados. Cada uno tiene su propia potencia que se correlaciona con su solubilidad en aceite. Esta relación existe porque los fármacos se unen directamente a las cavidades de las proteínas del sistema nervioso central, [ se necesita aclaración ] aunque se han descrito varias teorías sobre la acción anestésica general . Se cree que los anestésicos inhalatorios ejercen sus efectos en diferentes partes del sistema nervioso central. Por ejemplo, el efecto inmovilizador de los anestésicos inhalados se debe a un efecto sobre la médula espinal , mientras que la sedación, la hipnosis y la amnesia afectan zonas del cerebro. [53] : 515
Un anestésico inhalatorio es un compuesto químico que posee propiedades anestésicas generales y que puede administrarse por inhalación. Los agentes de importante interés clínico contemporáneo incluyen agentes anestésicos volátiles como isoflurano , sevoflurano y desflurano , y gases anestésicos como óxido nitroso y xenón .
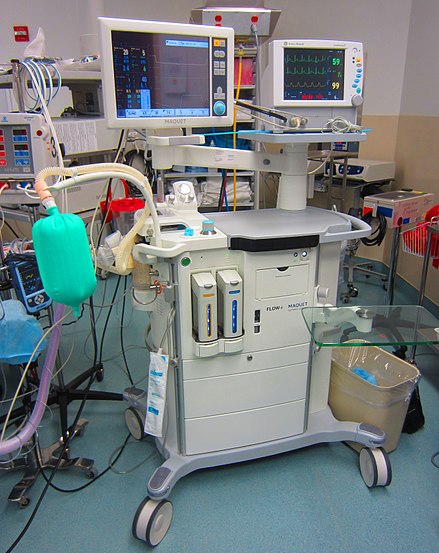
Los gases anestésicos son administrados por anestesiólogos (término que incluye anestesiólogos , enfermeros anestesistas y asistentes de anestesiólogo ) a través de una máscara de anestesia, una vía aérea con máscara laríngea o un tubo traqueal conectado a un vaporizador de anestésico y a un sistema de administración de anestésico . La máquina de anestesia (inglés británico) o máquina de anestesia (inglés estadounidense) o máquina de Boyle se utiliza para apoyar la administración de anestesia . El tipo más común de máquina de anestesia que se utiliza en el mundo desarrollado es la máquina de anestesia de flujo continuo, que está diseñada para proporcionar un suministro preciso y continuo de gases médicos (como oxígeno y óxido nitroso ), mezclados con una concentración precisa de anestésico. vapor (como isoflurano ) y administrarlo al paciente a una presión y un flujo seguros. Las máquinas modernas incorporan un ventilador , una unidad de succión y dispositivos de monitorización del paciente . El gas exhalado pasa a través de un depurador para eliminar el dióxido de carbono y el vapor anestésico y el oxígeno se reponen según sea necesario antes de devolver la mezcla al paciente. [ cita necesaria ]
{{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite book}}: Mantenimiento CS1: URL no apta ( enlace ){{cite book}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite journal}}: Mantenimiento CS1: URL no apta ( enlace ){{cite book}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )