El difosfato de adenosina ( ADP ), también conocido como pirofosfato de adenosina ( APP ), es un compuesto orgánico importante en el metabolismo y es esencial para el flujo de energía en las células vivas . El ADP consta de tres componentes estructurales importantes: una cadena principal de azúcar unida a la adenina y dos grupos fosfato unidos al átomo de carbono 5 de la ribosa . El grupo difosfato del ADP está unido al carbono 5' de la cadena principal de azúcar, mientras que la adenina se une al carbono 1'. [1]
El ADP se puede interconvertir en trifosfato de adenosina (ATP) y monofosfato de adenosina (AMP). El ATP contiene un grupo fosfato más que el ADP. El AMP contiene un grupo fosfato menos. La transferencia de energía utilizada por todos los seres vivos es el resultado de la desfosforilación del ATP por enzimas conocidas como ATPasas . La escisión de un grupo fosfato del ATP da como resultado el acoplamiento de energía a reacciones metabólicas y un subproducto de ADP. [1] El ATP se reforma continuamente a partir de especies de menor energía ADP y AMP. La biosíntesis de ATP se logra a través de procesos como la fosforilación a nivel de sustrato , la fosforilación oxidativa y la fotofosforilación , todos los cuales facilitan la adición de un grupo fosfato al ADP.
El ciclo del ADP proporciona la energía necesaria para realizar el trabajo en un sistema biológico, el proceso termodinámico de transferencia de energía de una fuente a otra. Hay dos tipos de energía: energía potencial y energía cinética . La energía potencial puede considerarse como energía almacenada o energía utilizable que está disponible para realizar el trabajo. La energía cinética es la energía de un objeto como resultado de su movimiento. La importancia del ATP radica en su capacidad de almacenar energía potencial dentro de los enlaces de fosfato. La energía almacenada entre estos enlaces puede luego transferirse para realizar el trabajo. Por ejemplo, la transferencia de energía del ATP a la proteína miosina provoca un cambio conformacional al conectarse a la actina durante la contracción muscular . [1]
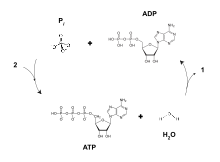
Se necesitan múltiples reacciones entre la miosina y la actina para producir eficazmente una contracción muscular y, por lo tanto, se requiere la disponibilidad de grandes cantidades de ATP para producir cada contracción muscular. Por este motivo, los procesos biológicos han evolucionado para producir formas eficientes de reponer la energía potencial del ATP a partir del ADP. [2]
La ruptura de uno de los enlaces de fósforo del ATP genera aproximadamente 30,5 kilojulios por mol de ATP (7,3 kcal ). [3] El ADP se puede convertir, o transformar de nuevo en ATP, mediante el proceso de liberación de la energía química disponible en los alimentos; en los seres humanos, esto se realiza constantemente a través de la respiración aeróbica en las mitocondrias . [2] Las plantas utilizan vías fotosintéticas para convertir y almacenar energía de la luz solar, también la conversión de ADP en ATP. [3] Los animales utilizan la energía liberada en la descomposición de la glucosa y otras moléculas para convertir ADP en ATP, que luego se puede utilizar para impulsar el crecimiento necesario y el mantenimiento celular. [2]
La vía catabólica de diez pasos de la glucólisis es la fase inicial de liberación de energía libre en la descomposición de la glucosa y se puede dividir en dos fases, la fase preparatoria y la fase de recuperación. El ADP y el fosfato son necesarios como precursores para sintetizar ATP en las reacciones de recuperación del ciclo del TCA y el mecanismo de fosforilación oxidativa . [4] Durante la fase de recuperación de la glucólisis, las enzimas fosfoglicerato quinasa y piruvato quinasa facilitan la adición de un grupo fosfato al ADP mediante fosforilación a nivel de sustrato . [5]
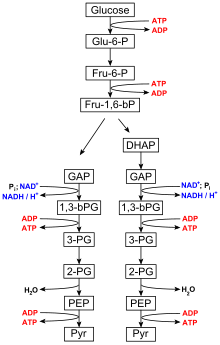
La glucólisis la realizan todos los organismos vivos y consta de 10 pasos. La reacción neta del proceso general de glucólisis es: [6]
Los pasos 1 y 3 requieren el aporte de energía derivada de la hidrólisis de ATP a ADP y Pi ( fosfato inorgánico), mientras que los pasos 7 y 10 requieren el aporte de ADP, cada uno produciendo ATP. [7] Las enzimas necesarias para descomponer la glucosa se encuentran en el citoplasma , el fluido viscoso que llena las células vivas, donde tienen lugar las reacciones glucolíticas. [1]
El ciclo del ácido cítrico , también conocido como ciclo de Krebs o ciclo del ácido tricarboxílico (TCA), es un proceso de 8 pasos que toma el piruvato generado por la glucólisis y genera 4 NADH, FADH2 y GTP, que luego se convierte en ATP. [8] Es solo en el paso 5, donde se genera GTP, por la succinil-CoA sintetasa, y luego se convierte en ATP, que se utiliza ADP (GTP + ADP → GDP + ATP). [9]
La fosforilación oxidativa produce 26 de los 30 equivalentes de ATP generados en la respiración celular al transferir electrones desde NADH o FADH2 a O 2 a través de transportadores de electrones. [10] La energía liberada cuando los electrones pasan desde NADH o FADH2 de mayor energía a O 2 de menor energía es necesaria para fosforilar ADP y generar nuevamente ATP. [11] Es este acoplamiento de energía y fosforilación de ADP a ATP lo que le da a la cadena de transporte de electrones el nombre de fosforilación oxidativa. [1]
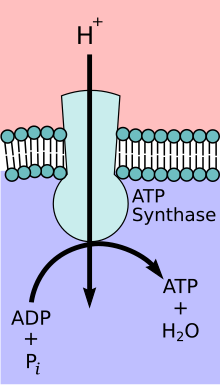
Durante las fases iniciales de la glucólisis y el ciclo del TCA , los cofactores como el NAD+ donan y aceptan electrones [12] que ayudan a la capacidad de la cadena de transporte de electrones de producir un gradiente de protones a través de la membrana mitocondrial interna. [13] El complejo de la ATP sintasa existe dentro de la membrana mitocondrial (porción F O ) y sobresale hacia la matriz (porción F 1 ). La energía derivada como resultado del gradiente químico se utiliza luego para sintetizar ATP mediante el acoplamiento de la reacción del fosfato inorgánico al ADP en el sitio activo de la enzima ATP sintasa ; la ecuación para esto se puede escribir como ADP + P i → ATP. [ cita requerida ]
En condiciones normales, las plaquetas pequeñas con forma de disco circulan libremente en la sangre y sin interacción entre sí. El ADP se almacena en cuerpos densos dentro de las plaquetas sanguíneas y se libera cuando se activan. El ADP interactúa con una familia de receptores de ADP que se encuentran en las plaquetas (P2Y1, P2Y12 y P2X1), lo que conduce a la activación plaquetaria. [14]
El ADP en la sangre se convierte en adenosina por la acción de las ecto-ADPasas , lo que inhibe la activación adicional de las plaquetas a través de los receptores de adenosina . [ cita requerida ]