El nobelio es un elemento químico sintético ; su símbolo es No y su número atómico es 102. Recibe su nombre en honor a Alfred Nobel , el inventor de la dinamita y benefactor de la ciencia. Es un metal radiactivo , el décimo elemento transuránico , el segundo transfermio, y es el penúltimo miembro de la serie de los actínidos . Como todos los elementos con número atómico superior a 100, el nobelio solo se puede producir en aceleradores de partículas bombardeando elementos más ligeros con partículas cargadas. Se sabe que existen un total de doce isótopos de nobelio ; el más estable es el 259 No con una vida media de 58 minutos, pero el 255 No de vida más corta (vida media de 3,1 minutos) es el más utilizado en química porque se puede producir a mayor escala.
Los experimentos químicos han confirmado que el nobelio se comporta como un homólogo más pesado del iterbio en la tabla periódica. Las propiedades químicas del nobelio no se conocen por completo: en su mayoría solo se conocen en solución acuosa . Antes del descubrimiento del nobelio, se predijo que mostraría un estado de oxidación estable +2 , así como el estado +3 característico de los otros actínidos ; estas predicciones se confirmaron más tarde, ya que el estado +2 es mucho más estable que el estado +3 en solución acuosa y es difícil mantener el nobelio en el estado +3.
En las décadas de 1950 y 1960, muchos laboratorios de Suecia , la Unión Soviética y los Estados Unidos reivindicaron el descubrimiento del nobelio . Aunque los científicos suecos pronto se retractaron de sus afirmaciones, la prioridad del descubrimiento y, por tanto, la denominación del elemento fueron objeto de disputa entre científicos soviéticos y estadounidenses. No fue hasta 1992 cuando la Unión Internacional de Química Pura y Aplicada (IUPAC) atribuyó el descubrimiento al equipo soviético. Aun así, nobelio, la propuesta sueca, se mantuvo como nombre del elemento debido a su uso de larga data en la literatura.

Un núcleo atómico superpesado [b] se crea en una reacción nuclear que combina otros dos núcleos de tamaño desigual [c] en uno; aproximadamente, cuanto más desiguales sean los dos núcleos en términos de masa , mayor será la posibilidad de que los dos reaccionen. [12] El material hecho de los núcleos más pesados se convierte en un objetivo, que luego es bombardeado por el haz de núcleos más ligeros. Dos núcleos solo pueden fusionarse en uno si se aproximan lo suficiente; normalmente, los núcleos (todos cargados positivamente) se repelen entre sí debido a la repulsión electrostática . La interacción fuerte puede superar esta repulsión, pero solo a una distancia muy corta de un núcleo; los núcleos del haz se aceleran así en gran medida para que dicha repulsión sea insignificante en comparación con la velocidad del núcleo del haz. [13] La energía aplicada a los núcleos del haz para acelerarlos puede hacer que alcancen velocidades tan altas como una décima parte de la velocidad de la luz . Sin embargo, si se aplica demasiada energía, el núcleo del haz puede desmoronarse. [13]
El hecho de acercarse lo suficiente no es suficiente para que dos núcleos se fusionen: cuando dos núcleos se aproximan, suelen permanecer juntos durante unos 10 −20 segundos y luego se separan (no necesariamente en la misma composición que antes de la reacción) en lugar de formar un solo núcleo. [13] [14] Esto sucede porque durante el intento de formación de un solo núcleo, la repulsión electrostática desgarra el núcleo que se está formando. [13] Cada par de un objetivo y un haz se caracteriza por su sección transversal : la probabilidad de que se produzca la fusión si dos núcleos se aproximan entre sí expresada en términos del área transversal que la partícula incidente debe golpear para que se produzca la fusión. [d] Esta fusión puede ocurrir como resultado del efecto cuántico en el que los núcleos pueden hacer un túnel a través de la repulsión electrostática. Si los dos núcleos pueden permanecer cerca después de esa fase, las interacciones nucleares múltiples dan como resultado una redistribución de energía y un equilibrio energético. [13]
La fusión resultante es un estado excitado [17] —denominado núcleo compuesto— y por lo tanto es muy inestable. [13] Para alcanzar un estado más estable, la fusión temporal puede fisionarse sin la formación de un núcleo más estable. [18] Alternativamente, el núcleo compuesto puede expulsar algunos neutrones , que se llevarían la energía de excitación; si esta última no es suficiente para una expulsión de neutrones, la fusión produciría un rayo gamma . Esto sucede en unos 10 −16 segundos después de la colisión nuclear inicial y da como resultado la creación de un núcleo más estable. [18] La definición del Grupo de Trabajo Conjunto (JWP) IUPAC/IUPAP establece que un elemento químico solo puede reconocerse como descubierto si un núcleo del mismo no se ha desintegrado en 10 −14 segundos. Este valor se eligió como una estimación de cuánto tiempo tarda un núcleo en adquirir electrones y, por lo tanto, mostrar sus propiedades químicas. [19] [e]
El haz pasa a través del objetivo y llega a la siguiente cámara, el separador; si se produce un nuevo núcleo, se transporta con este haz. [21] En el separador, el núcleo recién producido se separa de otros nucleidos (el del haz original y cualquier otro producto de reacción) [f] y se transfiere a un detector de barrera de superficie , que detiene el núcleo. Se marca la ubicación exacta del próximo impacto en el detector; también se marcan su energía y el tiempo de llegada. [21] La transferencia tarda unos 10 −6 segundos; para ser detectado, el núcleo debe sobrevivir este tiempo. [24] El núcleo se registra nuevamente una vez que se registra su desintegración, y se miden la ubicación, la energía y el tiempo de la desintegración. [21]
La estabilidad de un núcleo la proporciona la interacción fuerte. Sin embargo, su alcance es muy corto; a medida que los núcleos se hacen más grandes, su influencia sobre los nucleones más externos ( protones y neutrones) se debilita. Al mismo tiempo, el núcleo se desgarra por la repulsión electrostática entre protones, y su alcance no está limitado. [25] La energía de enlace total proporcionada por la interacción fuerte aumenta linealmente con el número de nucleones, mientras que la repulsión electrostática aumenta con el cuadrado del número atómico, es decir, este último crece más rápido y se vuelve cada vez más importante para los núcleos pesados y superpesados. [26] [27] Por lo tanto, se predice teóricamente [28] y hasta ahora se ha observado [29] que los núcleos superpesados se desintegran predominantemente a través de modos de desintegración que son causados por dicha repulsión: desintegración alfa y fisión espontánea . [g] Casi todos los emisores alfa tienen más de 210 nucleones, [31] y el nucleido más ligero que experimenta principalmente fisión espontánea tiene 238. [32] En ambos modos de desintegración, los núcleos no pueden desintegrarse mediante barreras de energía correspondientes para cada modo, pero se pueden atravesar mediante un túnel. [26] [27]

Las partículas alfa se producen comúnmente en desintegraciones radiactivas porque la masa de una partícula alfa por nucleón es lo suficientemente pequeña como para dejar algo de energía para que la partícula alfa se use como energía cinética para salir del núcleo. [34] La fisión espontánea es causada por la repulsión electrostática que desgarra el núcleo y produce varios núcleos en diferentes instancias de fisión de núcleos idénticos. [27] A medida que aumenta el número atómico, la fisión espontánea rápidamente se vuelve más importante: las vidas medias parciales de fisión espontánea disminuyen en 23 órdenes de magnitud desde el uranio (elemento 92) hasta el nobelio (elemento 102), [35] y en 30 órdenes de magnitud desde el torio (elemento 90) hasta el fermio (elemento 100). [36] El modelo anterior de gota líquida sugería que la fisión espontánea ocurriría casi instantáneamente debido a la desaparición de la barrera de fisión para núcleos con aproximadamente 280 nucleones. [27] [37] El modelo de capas nucleares posterior sugirió que los núcleos con alrededor de 300 nucleones formarían una isla de estabilidad en la que los núcleos serán más resistentes a la fisión espontánea y sufrirán principalmente desintegración alfa con vidas medias más largas. [27] [37] Descubrimientos posteriores sugirieron que la isla predicha podría estar más lejos de lo que se anticipó originalmente; también mostraron que los núcleos intermedios entre los actínidos de larga vida y la isla predicha se deforman y ganan estabilidad adicional a partir de los efectos de capa. [38] Los experimentos en núcleos superpesados más ligeros, [39] así como aquellos más cercanos a la isla esperada, [35] han demostrado una estabilidad mayor que la anticipada previamente contra la fisión espontánea, lo que muestra la importancia de los efectos de capa en los núcleos. [h]
Las desintegraciones alfa son registradas por las partículas alfa emitidas, y los productos de la desintegración son fáciles de determinar antes de la desintegración real; si tal desintegración o una serie de desintegraciones consecutivas produce un núcleo conocido, el producto original de una reacción puede determinarse fácilmente. [i] (Que todas las desintegraciones dentro de una cadena de desintegración estaban de hecho relacionadas entre sí se establece por la ubicación de estas desintegraciones, que deben estar en el mismo lugar.) [21] El núcleo conocido puede reconocerse por las características específicas de la desintegración que sufre, como la energía de desintegración (o más específicamente, la energía cinética de la partícula emitida). [j] La fisión espontánea, sin embargo, produce varios núcleos como productos, por lo que el nucleido original no puede determinarse a partir de sus hijos. [k]
La información de que disponen los físicos que intentan sintetizar un elemento superpesado es, por tanto, la información recogida en los detectores: posición, energía y tiempo de llegada de una partícula al detector, y los de su desintegración. Los físicos analizan estos datos y tratan de concluir que efectivamente fue causado por un nuevo elemento y no podría haber sido causado por un nucleido diferente del que se afirma. A menudo, los datos proporcionados son insuficientes para concluir que definitivamente se creó un nuevo elemento y no hay otra explicación para los efectos observados; se han cometido errores en la interpretación de los datos. [l]
El descubrimiento del elemento 102 fue un proceso complicado y fue reivindicado por grupos de Suecia , Estados Unidos y la Unión Soviética . El primer informe completo e incontrovertible de su detección recién llegó en 1966 del Instituto Conjunto de Investigación Nuclear de Dubna (entonces en la Unión Soviética). [50]
El primer anuncio del descubrimiento del elemento 102 fue anunciado por físicos del Instituto Nobel en Suecia en 1957. El equipo informó que habían bombardeado un objetivo de curio con iones de carbono-13 durante veinticinco horas en intervalos de media hora. Entre bombardeos, se realizó química de intercambio iónico en el objetivo. Doce de los cincuenta bombardeos contenían muestras que emitían partículas alfa de (8,5 ± 0,1) MeV , que estaban en gotas que eluían antes que el fermio (número atómico Z = 100) y el californio ( Z = 98). La vida media informada fue de 10 minutos y se asignó a 251 102 o 253 102, aunque no se excluyó la posibilidad de que las partículas alfa observadas fueran de un isótopo de mendelevio ( Z = 101) de vida presumiblemente corta creado a partir de la captura de electrones del elemento 102. [50] El equipo propuso el nombre nobelio (No) para el nuevo elemento, [51] [52] que fue inmediatamente aprobado por la IUPAC, [53] una decisión que el grupo de Dubna calificó en 1968 de apresurada. [54]
En 1958, los científicos del Laboratorio Nacional Lawrence Berkeley repitieron el experimento. El equipo de Berkeley, formado por Albert Ghiorso , Glenn T. Seaborg , John R. Walton y Torbjørn Sikkeland , utilizó el nuevo acelerador lineal de iones pesados (HILAC) para bombardear un objetivo de curio (95% 244 Cm y 5% 246 Cm) con iones 13 C y 12 C. No pudieron confirmar la actividad de 8,5 MeV reclamada por los suecos, pero en cambio pudieron detectar desintegraciones de fermio-250, supuestamente la hija de 254 102 (producida a partir del curio-246), que tenía una vida media aparente de ~3 s. Probablemente esta asignación también fue errónea, ya que el trabajo posterior de Dubna de 1963 demostró que la vida media del 254 No es significativamente más larga (alrededor de 50 s). Es más probable que las desintegraciones alfa observadas no provengan del elemento 102, sino más bien del Fm 250m . [50]
En 1959, el equipo sueco intentó explicar la incapacidad del equipo de Berkeley para detectar el elemento 102 en 1958, manteniendo que lo habían descubierto. Sin embargo, trabajos posteriores han demostrado que no existen isótopos de nobelio más ligeros que el 259 No (no se podrían haber producido isótopos más pesados en los experimentos suecos) con una vida media de más de 3 minutos, y que los resultados del equipo sueco probablemente provengan del torio -225, que tiene una vida media de 8 minutos y sufre rápidamente una triple desintegración alfa al polonio -213, que tiene una energía de desintegración de 8,53612 MeV. Esta hipótesis tiene peso por el hecho de que el torio-225 se puede producir fácilmente en la reacción utilizada y no se separaría mediante los métodos químicos utilizados. Trabajos posteriores sobre el nobelio también demostraron que el estado divalente es más estable que el trivalente y, por lo tanto, que las muestras que emitían partículas alfa no podían haber contenido nobelio, ya que el nobelio divalente no se habría eluido con los otros actínidos trivalentes. [50] Por lo tanto, el equipo sueco luego se retractó de su afirmación y asoció la actividad a efectos de fondo. [53]
En 1959, el equipo continuó sus estudios y afirmó que eran capaces de producir un isótopo que se desintegraba predominantemente por emisión de una partícula alfa de 8,3 MeV, con una vida media de 3 s con una rama de fisión espontánea asociada del 30% . La actividad se asignó inicialmente a 254 102 pero luego se cambió a 252 102. Sin embargo, también notaron que no era seguro que se hubiera producido el elemento 102 debido a las difíciles condiciones. [50] El equipo de Berkeley decidió adoptar el nombre propuesto por el equipo sueco, "nobelio", para el elemento. [53]
Mientras tanto, en Dubna, se llevaron a cabo experimentos en 1958 y 1960 con el objetivo de sintetizar también el elemento 102. El primer experimento de 1958 bombardeó plutonio-239 y -241 con iones de oxígeno-16 . Se observaron algunas desintegraciones alfa con energías de poco más de 8,5 MeV, y se asignaron a 251,252,253 102, aunque el equipo escribió que no se podía descartar la formación de isótopos a partir de impurezas de plomo o bismuto (que no producirían nobelio). Si bien los experimentos posteriores de 1958 señalaron que se podían producir nuevos isótopos a partir de impurezas de mercurio , talio , plomo o bismuto, los científicos todavía mantuvieron su conclusión de que el elemento 102 podía producirse a partir de esta reacción, mencionando una vida media de menos de 30 segundos y una energía de desintegración de (8,8 ± 0,5) MeV. Experimentos posteriores de 1960 demostraron que se trataba de efectos de fondo. Experimentos de 1967 también redujeron la energía de desintegración a (8,6 ± 0,4) MeV, pero ambos valores son demasiado altos para poder igualar los del 253 No o el 254 No. [50] El equipo de Dubna declaró más tarde en 1970 y nuevamente en 1987 que estos resultados no eran concluyentes. [50]
En 1961, los científicos de Berkeley afirmaron haber descubierto el elemento 103 en la reacción del californio con iones de boro y carbono. Afirmaron haber producido el isótopo 257 103 y también afirmaron haber sintetizado un isótopo de desintegración alfa del elemento 102 que tenía una vida media de 15 s y una energía de desintegración alfa de 8,2 MeV. Asignaron este valor al 255 102 sin dar ninguna razón para ello. Los valores no concuerdan con los que ahora se conocen para el 255 No, aunque sí concuerdan con los que ahora se conocen para el 257 No, y aunque este isótopo probablemente jugó un papel en este experimento, su descubrimiento no fue concluyente. [50]
En Dubna se continuó trabajando en el elemento 102 y en 1964 se llevaron a cabo allí experimentos para detectar los isótopos derivados de la desintegración alfa del elemento 102, sintetizándolo a partir de la reacción de un blanco de uranio-238 con iones de neón . Los productos se transportaron a lo largo de una lámina de plata y se purificaron químicamente, y se detectaron los isótopos 250 Fm y 252 Fm. El rendimiento de 252 Fm se interpretó como una prueba de que su progenitor 256 102 también se había sintetizado: como se observó que el 252 Fm también podía producirse directamente en esta reacción mediante la emisión simultánea de una partícula alfa con el exceso de neutrones, se tomaron medidas para garantizar que el 252 Fm no pudiera ir directamente a la lámina de plata. La vida media detectada para 256 102 fue de 8 s, que es mucho más alta que el valor más moderno de 1967 de (3,2 ± 0,2) s. [50] Se realizaron más experimentos en 1966 para 254 102, utilizando las reacciones 243 Am ( 15 N ,4n) 254 102 y 238 U( 22 Ne,6n) 254 102, encontrando una vida media de (50 ± 10) s: en ese momento no se entendía la discrepancia entre este valor y el valor anterior de Berkeley, aunque trabajos posteriores demostraron que la formación del isómero 250m Fm era menos probable en los experimentos de Dubna que en los de Berkeley. En retrospectiva, los resultados de Dubna en 254 102 probablemente fueron correctos y ahora pueden considerarse una detección concluyente del elemento 102. [50]
En 1966 se publicó otro experimento muy convincente de Dubna (aunque se presentó en 1965), nuevamente usando las mismas dos reacciones, que concluyó que el 254 102 tenía de hecho una vida media mucho más larga que los 3 segundos que afirmaba Berkeley. [50] Trabajos posteriores en 1967 en Berkeley y 1971 en el Laboratorio Nacional de Oak Ridge confirmaron completamente el descubrimiento del elemento 102 y aclararon observaciones anteriores. [53] En diciembre de 1966, el grupo de Berkeley repitió los experimentos de Dubna y los confirmó completamente, y usó estos datos para finalmente asignar correctamente los isótopos que habían sintetizado previamente pero que aún no podían identificar en ese momento, y así afirmaron haber descubierto el nobelio entre 1958 y 1961. [53]

En 1969, el equipo de Dubna llevó a cabo experimentos químicos con el elemento 102 y concluyó que se comportaba como el homólogo más pesado del iterbio . Los científicos rusos propusieron el nombre joliotio (Jo) para el nuevo elemento en honor a Irène Joliot-Curie , quien había fallecido recientemente, lo que generó una controversia sobre la denominación de elementos que no se resolvería hasta varias décadas después, ya que cada grupo utilizó sus propios nombres propuestos. [53] [55]
En 1992, el grupo de trabajo sobre transfermio de la IUPAC y la IUPAP (TWG) reevaluó las afirmaciones del descubrimiento y concluyó que sólo el trabajo de Dubna de 1966 detectó y asignó correctamente las desintegraciones a los núcleos con número atómico 102 en ese momento. Por lo tanto, el equipo de Dubna es reconocido oficialmente como el descubridor del nobelio, aunque es posible que se detectara en Berkeley en 1959. [50] Esta decisión fue criticada por Berkeley al año siguiente, calificando la reapertura de los casos de los elementos 101 a 103 de "pérdida de tiempo inútil", mientras que Dubna estuvo de acuerdo con la decisión de la IUPAC. [54]
En 1994, como parte de un intento de resolución de la controversia sobre los nombres de los elementos, la IUPAC ratificó los nombres de los elementos 101-109. Para el elemento 102, ratificó el nombre nobelio (No) sobre la base de que se había arraigado en la literatura a lo largo de 30 años y que Alfred Nobel debería ser conmemorado de esta manera. [56] Debido a las protestas por los nombres de 1994, que en su mayoría no respetaban las elecciones de los descubridores, se produjo un período de comentarios y en 1995 la IUPAC nombró al elemento 102 flerovio (Fl) como parte de una nueva propuesta, en honor a Georgy Flyorov o a su homónimo Laboratorio de Reacciones Nucleares Flerov . [57] Esta propuesta tampoco fue aceptada y en 1997 se restableció el nombre nobelio . [56] Hoy en día, el nombre flerovio , con el mismo símbolo, se refiere al elemento 114. [ 58]
En la tabla periódica , el nobelio se encuentra a la derecha del actínido mendelevio , a la izquierda del actínido lawrencio y debajo del lantánido iterbio . El metal nobelio aún no se ha preparado en grandes cantidades y actualmente la preparación en grandes cantidades es imposible. [60] Sin embargo, se han realizado varias predicciones y algunos resultados experimentales preliminares con respecto a sus propiedades. [60]
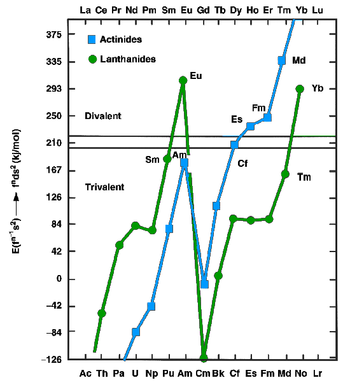
Los lantánidos y actínidos, en estado metálico, pueden existir como metales divalentes (como el europio y el iterbio ) o trivalentes (la mayoría de los demás lantánidos). Los primeros tienen configuraciones f n s 2 , mientras que los segundos tienen configuraciones f n −1 d 1 s 2 . En 1975, Johansson y Rosengren examinaron los valores medidos y predichos para las energías cohesivas ( entalpías de cristalización) de los lantánidos y actínidos metálicos , tanto como metales divalentes como trivalentes. [61] [62] La conclusión fue que la mayor energía de enlace de la configuración [Rn]5f 13 6d 1 7s 2 sobre la configuración [Rn]5f 14 7s 2 para el nobelio no fue suficiente para compensar la energía necesaria para promover un electrón 5f a 6d, como también es cierto para los actínidos muy tardíos: por lo tanto, se esperaba que el einstenio , el fermio , el mendelevio y el nobelio fueran metales divalentes, aunque para el nobelio esta predicción aún no se ha confirmado. [61] El predominio creciente del estado divalente mucho antes de que concluya la serie de actínidos se atribuye a la estabilización relativista de los electrones 5f, que aumenta con el aumento del número atómico: un efecto de esto es que el nobelio es predominantemente divalente en lugar de trivalente, a diferencia de todos los demás lantánidos y actínidos. [63] En 1986, se estimó que el metal nobelio tenía una entalpía de sublimación entre 126 kJ/mol, un valor cercano a los valores del einstenio, fermio y mendelevio y que apoya la teoría de que el nobelio formaría un metal divalente. [60] Al igual que los otros actínidos tardíos divalentes (excepto el lawrencio, una vez más trivalente), el nobelio metálico debería asumir una estructura cristalina cúbica centrada en las caras . [2] El metal nobelio divalente debería tener un radio metálico de alrededor de 197 pm . [60] Se ha predicho que el punto de fusión del nobelio es de 800 °C, el mismo valor que el estimado para el elemento vecino mendelevio. [64] Se predice que su densidad es de alrededor de 9,9 ± 0,4 g/cm 3 . [2]
La química del nobelio no está completamente caracterizada y se conoce solo en solución acuosa, en la que puede adoptar los estados de oxidación +3 o +2 , siendo este último más estable. [51] Se esperaba en gran medida antes del descubrimiento del nobelio que en solución se comportaría como los otros actínidos, siendo predominante el estado trivalente; sin embargo, Seaborg predijo en 1949 que el estado +2 también sería relativamente estable para el nobelio, ya que el ion No 2+ tendría la configuración electrónica del estado fundamental [Rn]5f 14 , incluida la capa 5f 14 llena estable . Pasaron diecinueve años antes de que se confirmara esta predicción. [65]
En 1967, se llevaron a cabo experimentos para comparar el comportamiento químico del nobelio con el del terbio , el californio y el fermio . Los cuatro elementos reaccionaron con cloro y los cloruros resultantes se depositaron a lo largo de un tubo, a lo largo del cual fueron transportados por un gas. Se descubrió que el cloruro de nobelio producido se adsorbía fuertemente en superficies sólidas, lo que demostraba que no era muy volátil , como los cloruros de los otros tres elementos investigados. Sin embargo, se esperaba que tanto el NoCl 2 como el NoCl 3 exhibieran un comportamiento no volátil y, por lo tanto, este experimento no fue concluyente en cuanto a cuál era el estado de oxidación preferido del nobelio. [65] La determinación de la preferencia del nobelio por el estado +2 tuvo que esperar hasta el año siguiente, cuando se llevaron a cabo experimentos de cromatografía de intercambio catiónico y coprecipitación en alrededor de cincuenta mil átomos de 255 No, y se descubrió que se comportaba de manera diferente a los otros actínidos y más como los metales alcalinotérreos divalentes . Esto demostró que en solución acuosa, el nobelio es más estable en el estado divalente cuando no hay oxidantes fuertes. [65] Experimentos posteriores en 1974 mostraron que el nobelio se eluía con los metales alcalinotérreos, entre Ca 2+ y Sr 2+ . [65] El nobelio es el único elemento del bloque f conocido para el cual el estado +2 es el más común y estable en solución acuosa. Esto ocurre debido a la gran brecha de energía entre los orbitales 5f y 6d al final de la serie de los actínidos. [66]
Se espera que la estabilización relativista de la subcapa 7s desestabilice en gran medida el dihidruro de nobelio, NoH 2 , y la estabilización relativista del espinor 7p 1/2 sobre el espinor 6d 3/2 significa que los estados excitados en los átomos de nobelio tienen una contribución de 7s y 7p en lugar de la contribución esperada de 6d. Las largas distancias No–H en la molécula de NoH 2 y la transferencia de carga significativa conducen a una ionicidad extrema con un momento dipolar de 5,94 D para esta molécula. En esta molécula, se espera que el nobelio exhiba un comportamiento similar al del grupo principal , actuando específicamente como un metal alcalinotérreo con su configuración de capa de valencia n s 2 y orbitales 5f similares a los del núcleo. [67]
La capacidad del nobelio para formar complejos con iones de cloruro es muy similar a la del bario , que forma complejos bastante débiles. [65] Su capacidad para formar complejos con citrato , oxalato y acetato en una solución acuosa de nitrato de amonio 0,5 M está entre la del calcio y el estroncio, aunque es algo más cercana a la del estroncio. [65]
En 1967 se estimó que el potencial de reducción estándar del par E °(No 3+ →No 2+ ) estaba entre +1,4 y +1,5 V ; [65] más tarde, en 2009, se descubrió que era de solo alrededor de +0,75 V. [68] El valor positivo muestra que el No 2+ es más estable que el No 3+ y que el No 3+ es un buen agente oxidante. Si bien los valores citados para E °(No 2+ →No 0 ) y E °(No 3+ →No 0 ) varían entre las fuentes, las estimaciones estándar aceptadas son −2,61 y −1,26 V. [65] Se ha predicho que el valor para el par E °(No 4+ →No 3+ ) sería +6,5 V. [65] Se estima que las energías de formación de Gibbs para No 3+ y No 2+ son −342 y −480 kJ/mol , respectivamente. [65]
Un átomo de nobelio tiene 102 electrones. Se espera que estén dispuestos en la configuración [Rn]5f 14 7s 2 ( símbolo del término del estado fundamental 1 S 0 ), aunque la verificación experimental de esta configuración electrónica aún no se había realizado en 2006. Los dieciséis electrones en las subcapas 5f y 7s son electrones de valencia . [60] Al formar compuestos, se pueden perder tres electrones de valencia, dejando atrás un núcleo [Rn]5f 13 : esto se ajusta a la tendencia establecida por los otros actínidos con sus configuraciones electrónicas [Rn]5f n en el estado tripositivo. Sin embargo, es más probable que solo se pierdan dos electrones de valencia, dejando atrás un núcleo [Rn]5f 14 estable con una capa 5f 14 llena. El primer potencial de ionización del nobelio se midió en 1974 y fue de (6,65 ± 0,07) eV como máximo , basándose en la suposición de que los electrones 7s se ionizarían antes que los 5f; [69] este valor aún no se ha refinado más debido a la escasez de nobelio y su alta radiactividad. [70] El radio iónico del hexacoordinado y octacoordinado No 3+ se había estimado preliminarmente en 1978 en alrededor de 90 y 102 pm respectivamente; [65] el radio iónico del No 2+ se ha encontrado experimentalmente en 100 pm con dos cifras significativas . [60] La entalpía de hidratación del No 2+ se ha calculado en 1486 kJ/mol. [65]
Se conocen catorce isótopos de nobelio, con números de masa 248-260 y 262; todos son radiactivos. [6] Además, se conocen isómeros nucleares para números de masa 250, 251, 253 y 254. [71] [72] De estos, el isótopo de vida más larga es 259No con una vida media de 58 minutos, y el isómero de vida más larga es 251mNo con una vida media de 1,7 segundos. [71] [72] Sin embargo, se predice que el isótopo aún no descubierto 261No tiene una vida media aún más larga de 3 horas. [6] Además, el 255No de vida más corta (vida media de 3,1 minutos) se usa con más frecuencia en la experimentación química porque se puede producir en mayores cantidades a partir de la irradiación de californio-249 con iones de carbono-12 . [73] Después del 259 No y el 255 No, los siguientes isótopos de nobelio más estables son el 253 No (vida media de 1,62 minutos), el 254 No (51 segundos ), el 257 No (25 segundos), el 256 No (2,91 segundos) y el 252 No (2,57 segundos). [73] [71] [72] Todos los isótopos de nobelio restantes tienen vidas medias inferiores a un segundo, y el isótopo de nobelio conocido de vida media más corta ( 248 No) tiene una vida media de menos de 2 microsegundos . [6] El isótopo 254 No es especialmente interesante teóricamente ya que está en medio de una serie de núcleos alargados desde 231 Pa hasta 279 Rg , y la formación de sus isómeros nucleares (de los cuales se conocen dos) está controlada por orbitales de protones como 2f 5/2 que vienen justo por encima de la capa esférica de protones; se puede sintetizar en la reacción de 208 Pb con 48 Ca. [74]
Las vidas medias de los isótopos de nobelio aumentan suavemente desde 250 No hasta 253 No. Sin embargo, aparece una caída en 254 No, y más allá de esto, las vidas medias de los isótopos de nobelio pares-pares caen bruscamente a medida que la fisión espontánea se convierte en el modo de desintegración dominante. Por ejemplo, la vida media del 256 No es de casi tres segundos, pero la del 258 No es de solo 1,2 milisegundos. [73] [71] [72] Esto muestra que en el nobelio, la repulsión mutua de protones plantea un límite a la región de núcleos de larga vida en la serie de los actínidos . [75] Los isótopos pares-impares de nobelio en su mayoría continúan teniendo vidas medias más largas a medida que aumentan sus números másicos, con una caída en la tendencia en 257 No. [73] [71] [72]
Los isótopos del nobelio se producen principalmente bombardeando objetivos actínidos ( uranio , plutonio , curio , californio o einstenio ), con la excepción del nobelio-262, que se produce como hijo del lawrencio-262. [73] El isótopo más comúnmente utilizado, 255 No, se puede producir bombardeando curio -248 o californio-249 con carbono-12: el último método es más común. Irradiar un objetivo de 350 μg cm −2 de californio-249 con tres billones (3 × 10 12 ) de iones de carbono-12 de 73 MeV por segundo durante diez minutos puede producir alrededor de 1200 átomos de nobelio-255. [73]
Una vez producido el nobelio-255, se puede separar de forma similar a como se utiliza para purificar el mendelevio, un actínido vecino. El momento de retroceso de los átomos de nobelio-255 producidos se utiliza para alejarlos físicamente del objetivo del que se producen, llevándolos a una fina lámina de metal (normalmente berilio , aluminio , platino u oro ) justo detrás del objetivo en el vacío: esto se combina normalmente atrapando los átomos de nobelio en una atmósfera de gas (con frecuencia helio ) y llevándolos junto con un chorro de gas desde una pequeña abertura en la cámara de reacción. Utilizando un tubo capilar largo e incluyendo aerosoles de cloruro de potasio en el gas helio, los átomos de nobelio pueden transportarse a lo largo de decenas de metros . [76] La fina capa de nobelio recogida en la lámina se puede eliminar entonces con ácido diluido sin disolver completamente la lámina. [76] El nobelio puede entonces aislarse explotando su tendencia a formar el estado divalente, a diferencia de los otros actínidos trivalentes: bajo las condiciones de elución típicamente utilizadas (ácido bis-(2-etilhexil) fosfórico (HDEHP) como fase orgánica estacionaria y ácido clorhídrico 0,05 M como fase acuosa móvil, o utilizando ácido clorhídrico 3 M como eluyente de columnas de resina de intercambio catiónico ), el nobelio pasará a través de la columna y se eluirá mientras que los otros actínidos trivalentes permanecerán en la columna. [76] Sin embargo, si se utiliza una lámina de oro "captora" directa, el proceso se complica por la necesidad de separar el oro utilizando cromatografía de intercambio aniónico antes de aislar el nobelio por elución de columnas de extracción cromatográfica utilizando HDEHP. [76]