
Los dendrímeros son moléculas poliméricas ramificadas y altamente ordenadas . [1] [2] Los términos sinónimos para dendrímero incluyen arboroides y moléculas en cascada . Por lo general, los dendrímeros son simétricos respecto del núcleo y, a menudo, adoptan una morfología tridimensional esférica. La palabra dendrón también se encuentra con frecuencia. Un dendrón generalmente contiene un solo grupo direccionable químicamente llamado punto focal o núcleo. La diferencia entre dendrones y dendrímeros se ilustra en la figura superior, pero los términos generalmente se encuentran indistintamente. [3]
Dendrímero Sustancia compuesta por moléculas de dendrímero idénticas.
Molécula de dendrímero
Molécula constituida por uno o más dendrones que emanan de una única unidad constitucional.
Dendrón
Parte de una molécula con una sola valencia libre, que comprende exclusivamente unidades de repetición constitucionales dendríticas y terminales y en la que cada ruta desde la valencia libre hasta cualquier grupo final comprende el mismo número de unidades de repetición constitucionales. Nota 1: A los efectos de determinar la naturaleza de las unidades de repetición constitucionales, la valencia libre se considera como una conexión a una CRU. Nota 2: Una molécula de dendrímero que comprende un solo dendrón se denomina a veces dendrón, monodendro o dendrón funcionalizado. El uso de los términos "dendrón" o "monodendro" en el sentido de molécula o sustancia no es aceptable. Nota 3: En un dendrón, no hay macrociclos de unidades constitucionales. [4]

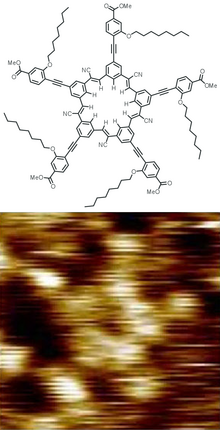
Los primeros dendrímeros fueron fabricados mediante métodos de síntesis divergente por Fritz Vögtle en 1978, [7] RG Denkewalter en Allied Corporation en 1981, [8] [9] Donald Tomalia en Dow Chemical en 1983 [10] y en 1985, [11] [12] y por George R. Newkome en 1985. [13] En 1990, Craig Hawker y Jean Fréchet introdujeron un método sintético convergente . [14] La popularidad de los dendrímeros aumentó considerablemente, lo que dio lugar a más de 5000 artículos científicos y patentes en el año 2005.
Las moléculas dendríticas se caracterizan por su perfección estructural. Los dendrímeros y los dendrones son compuestos monodispersos y, por lo general, muy simétricos y esféricos. El campo de las moléculas dendríticas se puede dividir aproximadamente en especies de bajo peso molecular y especies de alto peso molecular. La primera categoría incluye dendrímeros y dendrones, y la segunda incluye polímeros dendronizados , polímeros hiperramificados y polímeros en cepillo .
Las propiedades de los dendrímeros están dominadas por los grupos funcionales en la superficie molecular , sin embargo, hay ejemplos de dendrímeros con funcionalidad interna. [15] [16] [17] La encapsulación dendrítica de moléculas funcionales permite el aislamiento del sitio activo, una estructura que imita la de los sitios activos en biomateriales. [18] [19] [20] Además, es posible hacer que los dendrímeros sean solubles en agua, a diferencia de la mayoría de los polímeros , funcionalizando su capa externa con especies cargadas u otros grupos hidrófilos . Otras propiedades controlables de los dendrímeros incluyen toxicidad , cristalinidad , formación de tecto-dendrímeros y quiralidad . [3]
Los dendrímeros también se clasifican por generación, que se refiere al número de ciclos de ramificación repetidos que se realizan durante su síntesis. Por ejemplo, si un dendrímero se fabrica mediante síntesis convergente (ver más abajo) y las reacciones de ramificación se realizan en la molécula central tres veces, el dendrímero resultante se considera un dendrímero de tercera generación. Cada generación sucesiva da como resultado un dendrímero con un peso molecular de aproximadamente el doble que el de la generación anterior. Los dendrímeros de generaciones superiores también tienen más grupos funcionales expuestos en la superficie, que luego se pueden usar para personalizar el dendrímero para una aplicación determinada. [21] Los dendrímeros pueden tener un solo grupo funcional en la superficie o pueden modificarse para permitir múltiples grupos funcionales en la superficie. [22]

Uno de los primeros dendrímeros, el dendrímero Newkome, se sintetizó en 1985. Esta macromolécula también se conoce comúnmente con el nombre de arborol. La figura describe el mecanismo de las dos primeras generaciones de arborol a través de una ruta divergente (que se analiza a continuación). La síntesis se inicia mediante la sustitución nucleofílica de 1-bromopentano por trietil sodiometanotricarboxilato en dimetilformamida y benceno . A continuación, los grupos éster se redujeron mediante hidruro de litio y aluminio a un triol en un paso de desprotección . La activación de los extremos de la cadena se logró convirtiendo los grupos alcohol en grupos tosilato con cloruro de tosilo y piridina . A continuación, el grupo tosilo sirvió como grupo saliente en otra reacción con el tricarboxilato, formando la segunda generación. La repetición posterior de los dos pasos conduce a generaciones superiores de arborol. [13]
La poli(amidoamina) , o PAMAM, es quizás el dendrímero más conocido. El núcleo de PAMAM es una diamina (comúnmente etilendiamina ), que se hace reaccionar con acrilato de metilo y luego con otra etilendiamina para formar el PAMAM de generación 0 (G-0). Las reacciones sucesivas crean generaciones superiores, que tienden a tener propiedades diferentes. Las generaciones inferiores pueden considerarse moléculas flexibles sin regiones internas apreciables, mientras que las de tamaño mediano (G-3 o G-4) tienen un espacio interno que está esencialmente separado de la capa externa del dendrímero. Los dendrímeros muy grandes (G-7 y mayores) pueden considerarse más como partículas sólidas con superficies muy densas debido a la estructura de su capa externa. El grupo funcional en la superficie de los dendrímeros PAMAM es ideal para la química de clic , lo que da lugar a muchas aplicaciones potenciales. [23]
Se puede considerar que los dendrímeros tienen tres partes principales: un núcleo, una capa interna y una capa externa. Idealmente, un dendrímero se puede sintetizar para que tenga una funcionalidad diferente en cada una de estas partes para controlar propiedades como la solubilidad, la estabilidad térmica y la unión de compuestos para aplicaciones particulares. Los procesos sintéticos también pueden controlar con precisión el tamaño y el número de ramificaciones en el dendrímero. Hay dos métodos definidos de síntesis de dendrímeros, la síntesis divergente y la síntesis convergente . Sin embargo, debido a que las reacciones reales consisten en muchos pasos necesarios para proteger el sitio activo , es difícil sintetizar dendrímeros utilizando cualquiera de los métodos. Esto hace que los dendrímeros sean difíciles de fabricar y muy caros de comprar. En este momento, solo hay unas pocas empresas que venden dendrímeros; Polymer Factory Sweden AB [24] comercializa dendrímeros bis-MPA biocompatibles y Dendritech [25] es el único productor a escala de kilogramos de dendrímeros PAMAM. NanoSynthons, LLC [26] de Mount Pleasant, Michigan, EE. UU., produce dendrímeros PAMAM y otros dendrímeros patentados.
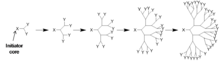
El dendrímero se ensambla a partir de un núcleo multifuncional, que se extiende hacia afuera mediante una serie de reacciones, comúnmente una reacción de Michael . Cada paso de la reacción debe llevarse a cabo hasta su finalización completa para evitar errores en el dendrímero, que pueden causar generaciones finales (algunas ramas son más cortas que otras). Estas impurezas pueden afectar la funcionalidad y la simetría del dendrímero, pero son extremadamente difíciles de purificar porque la diferencia de tamaño relativa entre los dendrímeros perfectos e imperfectos es muy pequeña. [21]
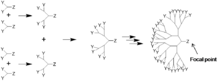
Los dendrímeros se construyen a partir de pequeñas moléculas que terminan en la superficie de la esfera, y las reacciones se desarrollan hacia adentro y finalmente se unen a un núcleo. Este método hace que sea mucho más fácil eliminar impurezas y ramificaciones más cortas en el camino, de modo que el dendrímero final es más monodisperso. Sin embargo, los dendrímeros fabricados de esta manera no son tan grandes como los fabricados con métodos divergentes porque el hacinamiento debido a los efectos estéricos a lo largo del núcleo es limitante. [21]

Los dendrímeros se han preparado mediante química clic , empleando reacciones de Diels-Alder , [28] reacciones de tiol-eno y tiol-ino [29] y reacciones de azida-alquino . [30] [31] [32]
Existen amplios caminos que se pueden abrir explorando esta química en la síntesis de dendrímeros.
Las aplicaciones de los dendrímeros suelen implicar la conjugación de otras especies químicas a la superficie del dendrímero que pueden funcionar como agentes de detección (como una molécula de tinte ), ligandos de afinidad , componentes de orientación, radioligandos , agentes de formación de imágenes o compuestos farmacéuticamente activos . Los dendrímeros tienen un potencial muy fuerte para estas aplicaciones porque su estructura puede dar lugar a sistemas multivalentes . En otras palabras, una molécula de dendrímero tiene cientos de sitios posibles para acoplarse a una especie activa. Los investigadores apuntaron a utilizar los entornos hidrófobos de los medios dendríticos para llevar a cabo reacciones fotoquímicas que generan los productos que se desafían sintéticamente. Se sintetizaron dendrímeros solubles en agua con terminación en ácido carboxílico y fenol para establecer su utilidad en la administración de fármacos, así como para llevar a cabo reacciones químicas en su interior. [33] Esto podría permitir a los investigadores unir tanto moléculas de orientación como moléculas de fármaco al mismo dendrímero, lo que podría reducir los efectos secundarios negativos de los medicamentos en las células sanas. [23]
Los dendrímeros también se pueden utilizar como agentes solubilizantes. Desde su introducción a mediados de la década de 1980, esta nueva clase de arquitectura de dendrímeros ha sido un candidato principal para la química anfitrión-huésped . [34] Los dendrímeros con núcleo hidrófobo y periferia hidrófila han demostrado exhibir un comportamiento similar a las micelas y tienen propiedades de contenedor en solución. [35] El uso de dendrímeros como micelas unimoleculares fue propuesto por Newkome en 1985. [36] Esta analogía destacó la utilidad de los dendrímeros como agentes solubilizantes. [37] La mayoría de los medicamentos disponibles en la industria farmacéutica son de naturaleza hidrófoba y esta propiedad en particular crea importantes problemas de formulación. Este inconveniente de los medicamentos se puede mejorar con el andamiaje dendrimérico, que se puede utilizar para encapsular y solubilizar los medicamentos debido a la capacidad de dichos andamiajes para participar en extensos enlaces de hidrógeno con agua. [38] [39] [40] [41] [42] [43] Los laboratorios de dendrímeros están intentando manipular el rasgo solubilizante del dendrímero, para explorar los dendrímeros para la administración de fármacos [44] [45] y para apuntar a portadores específicos. [46] [47] [48]
Para que los dendrímeros puedan utilizarse en aplicaciones farmacéuticas, deben superar los obstáculos regulatorios necesarios para llegar al mercado. Un andamio de dendrímero diseñado para lograr esto es el dendrímero de polietoxietilglicinamida (PEE-G). [49] [50] Este andamio de dendrímero ha sido diseñado y ha demostrado tener alta pureza por HPLC , estabilidad, solubilidad acuosa y baja toxicidad inherente.

Los métodos para administrar productos naturales inalterados mediante el uso de portadores poliméricos son de amplio interés. Los dendrímeros se han estudiado para la encapsulación de compuestos hidrófobos y para la administración de fármacos contra el cáncer. Las características físicas de los dendrímeros, incluida su monodispersidad, solubilidad en agua, capacidad de encapsulación y gran número de grupos periféricos funcionalizables, hacen que estas macromoléculas sean candidatos apropiados para vehículos de administración de fármacos.
Los dendrímeros son dispositivos de administración de fármacos particularmente versátiles debido a la amplia gama de modificaciones químicas que se pueden realizar para aumentar la idoneidad in vivo y permitir la administración de fármacos dirigida a sitios específicos.
La unión del fármaco al dendrímero se puede lograr mediante (1) una unión covalente o conjugación a la superficie externa del dendrímero formando un profármaco de dendrímero, (2) coordinación iónica a grupos funcionales externos cargados, o (3) encapsulación de tipo micelar de un fármaco a través de un ensamblaje supramolecular dendrímero-fármaco . [51] [52] En el caso de una estructura de profármaco de dendrímero, la unión de un fármaco a un dendrímero puede ser directa o mediada por un enlazador dependiendo de la cinética de liberación deseada. Dicho enlazador puede ser sensible al pH, catalizado por enzimas o un puente disulfuro. La amplia gama de grupos funcionales terminales disponibles para los dendrímeros permite muchos tipos diferentes de químicas de enlazadores, lo que proporciona otro componente ajustable en el sistema. Los parámetros clave a tener en cuenta para la química del enlazador son (1) el mecanismo de liberación al llegar al sitio objetivo, ya sea dentro de la célula o en un determinado sistema orgánico, (2) el espaciamiento entre el fármaco y el dendrímero para evitar que los fármacos lipofílicos se plieguen en el dendrímero, y (3) la degradabilidad del enlazador y las modificaciones de trazas posteriores a la liberación en los fármacos. [53] [54]
El polietilenglicol (PEG) es una modificación común de los dendrímeros para modificar su carga superficial y su tiempo de circulación. La carga superficial puede influir en las interacciones de los dendrímeros con sistemas biológicos, como los dendrímeros modificados con terminales de amina que tienen una propensión a interactuar con las membranas celulares con carga aniónica. Algunos estudios in vivo han demostrado que los dendrímeros policatiónicos son citotóxicos a través de la permeabilización de la membrana, un fenómeno que podría mitigarse parcialmente mediante la adición de tapas de PEGilación en los grupos de amina, lo que da como resultado una menor citotoxicidad y una menor hemólisis de los glóbulos rojos. [55] [56] Además, los estudios han descubierto que la PEGilación de los dendrímeros da como resultado una mayor carga de fármaco, una liberación más lenta del fármaco, tiempos de circulación más prolongados in vivo y una menor toxicidad en comparación con sus homólogos sin modificaciones de PEG. [57] [56]
Se han utilizado numerosas fracciones de orientación para modificar la biodistribución de los dendrímeros y permitir la orientación a órganos específicos. Por ejemplo, los receptores de folato se sobreexpresan en las células tumorales y, por lo tanto, son objetivos prometedores para la administración localizada de fármacos quimioterapéuticos . Se ha demostrado que la conjugación de ácido fólico con dendrímeros PAMAM aumenta la orientación y disminuye la toxicidad fuera del objetivo, al tiempo que mantiene la citotoxicidad en el objetivo de los quimioterapéuticos como el metotrexato , en modelos de cáncer en ratones. [57] [58]
La orientación de los dendrímeros a dianas celulares mediada por anticuerpos también ha demostrado ser prometedora para la administración dirigida de fármacos. Como los receptores del factor de crecimiento epidérmico (EGFR) a menudo se sobreexpresan en tumores cerebrales, los EGFR son un objetivo conveniente para la administración de fármacos en un sitio específico. La administración de boro a células cancerosas es importante para una terapia de captura de neutrones eficaz, un tratamiento del cáncer que requiere una gran concentración de boro en células cancerosas y una baja concentración en células sanas. Un dendrímero borado conjugado con un fármaco de anticuerpo monoclonal que se dirige a los EGFR se utilizó en ratas para administrar con éxito boro a células cancerosas . [59]
La modificación de los dendrímeros de nanopartículas con péptidos también ha tenido éxito en la destrucción dirigida de células de cáncer colorrectal ( HCT-116 ) en un escenario de co-cultivo. Los péptidos de focalización se pueden utilizar para lograr una administración específica del sitio o de la célula, y se ha demostrado que estos péptidos aumentan la especificidad de focalización cuando se combinan con dendrímeros. Específicamente, YIGSR-CMCht/PAMAM cargado con gemcitabina, un tipo único de nanopartícula de dendrímero, induce una mortalidad dirigida en estas células cancerosas. Esto se realiza a través de la interacción selectiva del dendrímero con los receptores de laminina . Los dendrímeros peptídicos pueden emplearse en el futuro para dirigirse con precisión a las células cancerosas y administrar agentes quimioterapéuticos. [60]
El mecanismo de captación celular de los dendrímeros también se puede ajustar mediante modificaciones de orientación química. El dendrímero PAMAM-G4 no modificado es captado en la microglia activada por endocitosis en fase fluida. Por el contrario, la modificación de los dendrímeros PAMAM-G4 hidroxilados con manosa fue capaz de cambiar el mecanismo de internalización a endocitosis mediada por el receptor de manosa (CD206). Además, la modificación de la manosa fue capaz de cambiar la biodistribución en el resto del cuerpo de los conejos. [61]
Los dendrímeros tienen el potencial de cambiar completamente los perfiles farmacocinéticos y farmacodinámicos (PK/PD) de un fármaco. Como portadores, la PK/PD ya no está determinada por el fármaco en sí, sino por la localización del dendrímero, la liberación del fármaco y la excreción del dendrímero. Las propiedades de ADME son muy ajustables variando el tamaño, la estructura y las características de la superficie del dendrímero. Mientras que los dendrímeros G9 se biodistribuyen en gran medida al hígado y al bazo, los dendrímeros G6 tienden a biodistribuirse más ampliamente. A medida que aumenta el peso molecular, el aclaramiento urinario y plasmático disminuyen mientras que la vida media terminal aumenta. [55]
Para aumentar el cumplimiento del paciente con el tratamiento prescrito, la administración oral de medicamentos suele preferirse a otras vías de administración. Sin embargo, la biodisponibilidad oral de muchos medicamentos tiende a ser muy baja. Los dendrímeros se pueden utilizar para aumentar la solubilidad y la estabilidad de los medicamentos administrados por vía oral y aumentar la penetración del medicamento a través de la membrana intestinal. [62] La biodisponibilidad de los dendrímeros PAMAM conjugados con un quimioterapéutico se ha estudiado en ratones; se encontró que alrededor del 9% del dendrímero administrado por vía oral se encontró intacto en la circulación y que se produjo una degradación mínima del dendrímero en el intestino. [63]
La administración intravenosa de dendrímeros parece prometedora como vector genético para administrar genes a varios órganos del cuerpo, e incluso a tumores. Un estudio descubrió que mediante una inyección intravenosa, una combinación de dendrímeros PPI y complejos genéticos dio como resultado la expresión de genes en el hígado, y otro estudio demostró que una inyección similar revirtió el crecimiento de tumores en animales observados. [64] [65]
El principal obstáculo para la administración transdérmica de fármacos es la epidermis. Los fármacos hidrófobos tienen muchas dificultades para penetrar la capa cutánea, ya que se distribuyen en gran medida en los aceites de la piel. Recientemente, se han utilizado dendrímeros PAMAM como vehículos de administración de AINE para aumentar la hidrofilicidad, lo que permite una mayor penetración de los fármacos. [66] Estas modificaciones actúan como potenciadores transdérmicos poliméricos que permiten que los fármacos penetren más fácilmente la barrera cutánea.
Los dendrímeros también pueden actuar como nuevos vehículos oftálmicos para la administración de fármacos, que son diferentes de los polímeros que se utilizan actualmente para este fin. Un estudio de Vanndamme y Bobeck utilizó dendrímeros PAMAM como vehículos de administración oftálmica en conejos para dos fármacos modelo y midió el tiempo de residencia ocular de esta administración, que resultó ser comparable y en algunos casos mayor que el de los polímeros bioadhesivos actuales utilizados en la administración ocular. [67] Este resultado indica que los fármacos administrados fueron más activos y tuvieron una mayor biodisponibilidad cuando se administraron a través de dendrímeros que sus contrapartes de fármaco libre. Además, se han utilizado hidrogeles de ácido hialurónico- dendrímero fotocurables que liberan fármacos como suturas corneales aplicadas directamente al ojo. Estas suturas de hidrogel han demostrado ser eficaces como dispositivo médico en modelos de conejos que superan las suturas tradicionales y minimizan la cicatrización corneal. [68]
La administración de fármacos mediante dendrímeros también ha demostrado ser muy prometedora como posible solución para muchos problemas tradicionalmente difíciles de administración de fármacos. En el caso de la administración de fármacos al cerebro, los dendrímeros pueden aprovechar el efecto EPR y el deterioro de la barrera hematoencefálica (BHE) para cruzar la BHE de manera efectiva in vivo. Por ejemplo, los dendrímeros PAMAM con terminación en hidroxilo poseen una capacidad intrínseca de focalización a los macrófagos inflamados en el cerebro, verificada utilizando dendrímeros de generación neutra marcados con fluorescencia en un modelo de conejo de parálisis cerebral . [69] Esta focalización intrínseca ha permitido la administración de fármacos en una variedad de condiciones, que van desde parálisis cerebral y otros trastornos neuroinflamatorios hasta lesión cerebral traumática y paro circulatorio hipotérmico, en una variedad de modelos animales que van desde ratones y conejos hasta caninos. [70] [71] [72] La captación de dendrímeros en el cerebro se correlaciona con la gravedad de la inflamación y el deterioro de la BHE y se cree que el deterioro de la BHE es el factor impulsor clave que permite la penetración de los dendrímeros. [73] [69] La localización está fuertemente sesgada hacia la microglia activada . La N-acetil cisteína conjugada con dendrímero ha demostrado eficacia in vivo como antiinflamatorio en una dosis más de 1000 veces menor que el fármaco libre, revirtiendo el fenotipo de la parálisis cerebral, el síndrome de Rett , la degeneración macular y otras enfermedades inflamatorias. [69]
Starpharma, una empresa farmacéutica australiana, tiene varios productos que ya han sido aprobados para su uso o que se encuentran en la fase de ensayos clínicos. SPL7013, también conocido como astodrímero sódico, es un polímero hiperramificado utilizado en la línea de productos farmacéuticos VivaGel de Starpharma que actualmente está aprobado para tratar la vaginosis bacteriana y prevenir la propagación del VIH, el VPH y el VHS en Europa, el sudeste asiático, Japón, Canadá y Australia. Debido a la amplia acción antiviral de SPL7013, la empresa lo ha probado recientemente como un posible fármaco para tratar el SARS-CoV-2. La empresa afirma que los estudios in vitro preliminares muestran una alta eficacia en la prevención de la infección por SARS-CoV-2 en las células. [74]
La capacidad de entregar fragmentos de ADN a las partes requeridas de una célula incluye muchos desafíos. La investigación actual se está realizando para encontrar formas de usar dendrímeros para transportar genes a las células sin dañar o desactivar el ADN. Para mantener la actividad del ADN durante la deshidratación, los complejos dendrímero/ADN se encapsularon en un polímero soluble en agua y luego se depositaron sobre o intercalados en películas de polímero funcional con una tasa de degradación rápida para mediar la transfección génica . Con base en este método, se utilizaron complejos dendrímero/ADN PAMAM para encapsular películas de polímero biodegradables funcionales para la entrega de genes mediada por sustrato. La investigación ha demostrado que el polímero funcional de degradación rápida tiene un gran potencial para la transfección localizada. [75] [76] [77]
Los dendrímeros tienen aplicaciones potenciales en sensores . Los sistemas estudiados incluyen sensores de protones o pH que utilizan poli(propilenimina), [78] compuestos de dendrímeros de tetrahexacontaamina de sulfuro de cadmio/polipropilenimina para detectar la extinción de la señal de fluorescencia , [79] y dendrímeros de poli(propilenamina) de primera y segunda generación para la fotodetección de cationes metálicos [80] , entre otros. La investigación en este campo es amplia y continua debido al potencial de detección múltiple y sitios de unión en estructuras dendríticas.
Los dendrímeros también se utilizan en la síntesis de nanopartículas metálicas monodispersas . Los dendrímeros de poli(amidoamida), o PAMAM, se utilizan por sus grupos de amina terciaria en los puntos de ramificación dentro del dendrímero. Los iones metálicos se introducen en una solución acuosa de dendrímero y forman un complejo con el par solitario de electrones presente en las aminas terciarias. Después de la formación de complejos, los iones se reducen a sus estados de valencia cero para formar una nanopartícula que se encapsula dentro del dendrímero. Estas nanopartículas tienen un ancho que varía de 1,5 a 10 nanómetros y se denominan nanopartículas encapsuladas en dendrímero . [81]
Dado el uso generalizado de pesticidas, herbicidas e insecticidas en la agricultura moderna, las empresas también están utilizando dendrímeros para ayudar a mejorar la distribución de agroquímicos a fin de permitir un crecimiento más saludable de las plantas y ayudar a combatir las enfermedades de las plantas. [82]
Los dendrímeros también se están investigando para su uso como sustitutos de la sangre . Su volumen estérico que rodea un centro hemo -mimético retarda significativamente la degradación en comparación con el hemo libre, [83] [84] y previene la citotoxicidad exhibida por el hemo libre. El polímero funcional dendrítico poliamidoamina (PAMAM) se utiliza para preparar la estructura de núcleo-capa, es decir, microcápsulas y se utiliza en la formulación de recubrimientos autorreparadores de origen convencional [85] y renovable. [86]
Recientemente se han implementado diferentes generaciones de dendrímeros de poliamidoamina como contactos selectivos en dispositivos fotovoltaicos. [87]
Los dendrímeros en los sistemas de administración de fármacos son un ejemplo de diversas interacciones entre el huésped y el anfitrión. La interacción entre el huésped y el anfitrión, el dendrímero y el fármaco, respectivamente, puede ser hidrófoba o covalente. La interacción hidrófoba entre el huésped y el anfitrión se considera "encapsulada", mientras que las interacciones covalentes se consideran conjugadas. Se ha demostrado que el uso de dendrímeros en medicina mejora la administración de fármacos al aumentar la solubilidad y la biodisponibilidad del fármaco. En conjunto, los dendrímeros pueden aumentar tanto la captación celular como la capacidad de focalización y reducir la resistencia a los fármacos. [88]
La solubilidad de varios fármacos antiinflamatorios no esteroideos (AINE) aumenta cuando se encapsulan en dendrímeros PAMAM. [89] Este estudio muestra que la mejora de la solubilidad de los AINE se debe a las interacciones electrostáticas entre los grupos de amina de la superficie en PAMAM y los grupos carboxilo que se encuentran en los AINE. Las interacciones hidrofóbicas entre los grupos aromáticos de los fármacos y las cavidades interiores del dendrímero contribuyen al aumento de la solubilidad. [90] Cuando un fármaco se encapsula dentro de un dendrímero, sus propiedades físicas y fisiológicas permanecen inalteradas, incluida la no especificidad y la toxicidad. Sin embargo, cuando el dendrímero y el fármaco están unidos covalentemente, se puede utilizar para la orientación a tejidos específicos y velocidades de liberación controladas. [91] La conjugación covalente de múltiples fármacos en las superficies de los dendrímeros puede plantear un problema de insolubilidad. [91] [92]
Este principio también se está estudiando para su aplicación en el tratamiento del cáncer. Varios grupos han encapsulado medicamentos contra el cáncer como: camptotecina , metotrexato y doxorrubicina . Los resultados de estas investigaciones han demostrado que los dendrímeros han aumentado la solubilidad en agua, han reducido la velocidad de liberación y posiblemente controlan la citotoxicidad de los fármacos. [88] El cisplatino se ha conjugado con dendrímeros PAMAM que dieron como resultado los mismos resultados farmacológicos que se enumeraron anteriormente, pero la conjugación también ayudó a acumular cisplatino en tumores sólidos en administración intravenosa. [93]