

Curare ( / k ʊ ˈ r ɑːr i / o / k j ʊ ˈ r ɑːr i / ; kuu -RAH -ree o kyuu -RAH -ree ) es un nombre común para varios venenos alcaloides para flechas que se originan a partir de extractos de plantas. Utilizado como agente paralizante por los pueblos indígenas de Centro y Sudamérica para la caza y con fines terapéuticos, el curare sólo se activa cuando contamina una herida o se introduce directamente en el torrente sanguíneo; no es activo cuando se ingiere por vía oral. Estos venenos causan debilidad de los músculos esqueléticos y, cuando se administran en dosis suficientes, eventual muerte por asfixia debido a parálisis del diafragma . El curare se prepara hirviendo la corteza de una de las docenas de fuentes vegetales, dejando una pasta oscura y espesa que se puede aplicar a las puntas de flechas o dardos. En medicina, el curare se ha utilizado como tratamiento para el tétanos y la intoxicación por estricnina y como agente paralizante en procedimientos quirúrgicos.
La palabra 'curare' se deriva de wurari , de la lengua caribe de los macusi de Guyana. [1] Tiene su origen en la frase caribeña "mawa cura", que significa la vid Mawa, científicamente conocida como Strychnos toxifera . [ cita necesaria ] Curare también es conocido entre los pueblos indígenas como Ampi, Woorari, Woorara, Woorali, Wourali, Wouralia, Ourare, Ourari, Urare, Urari y Uirary. El sustantivo 'curare' no debe confundirse con el verbo latino 'curare' ('curar, curar, cuidar').
En 1895, el farmacólogo Rudolf Böhm intentó clasificar los distintos venenos alcaloides basándose en los recipientes utilizados para su preparación. Creía que el curare podría clasificarse en tres tipos principales, como se ve a continuación. Por muy útil que pareciera, rápidamente quedó obsoleto. Richard Gill, un recolector de plantas, descubrió que los pueblos indígenas comenzaron a utilizar una variedad de recipientes para sus preparaciones de curare, invalidando en adelante la base de clasificación de Boehm. [2]
Manske también observó en su obra Los alcaloides de 1955 :
Los resultados de los primeros trabajos [anteriores a 1900] fueron muy inexactos debido a la complejidad y variación de la composición de las mezclas de alcaloides involucrados [...] eran alcaloides impuros, no cristalinos [...] Casi todos curare Las preparaciones eran y son mezclas complejas, y muchas de las acciones fisiológicas atribuidas a las primeras preparaciones curarizantes se debían sin duda a impurezas, particularmente a otros alcaloides presentes. Actualmente se considera que las preparaciones de curare son de dos tipos principales, las de Chondrodendron u otros miembros de la familia Menispermaceae y las de Strychnos , un género de la familia Loganiaceae [ahora Strychnaceae]. Algunas preparaciones pueden contener alcaloides de ambos [...] y la mayoría tiene otros ingredientes secundarios. [2]
El curare fue utilizado como veneno paralizante por muchos pueblos indígenas de América del Sur. Como era demasiado caro para usarlo en la guerra, el curare se usaba principalmente para la caza. [3] La presa era disparada con flechas o dardos de cerbatana sumergidos en curare, lo que provocaba asfixia debido a la incapacidad de contraer los músculos respiratorios de la víctima. En particular, el veneno era utilizado por los Kalinago , pueblo indígena de las Antillas Menores en el Caribe , en las puntas de sus flechas. [4] Además, el pueblo Yagua , indígena de Colombia y el noreste de Perú, comúnmente usaba estas toxinas a través de cerbatanas para apuntar a presas a 30 a 40 pasos de distancia. [5]
Debido a su popularidad entre los indígenas como medio para paralizar a las presas, ciertas tribus crearían monopolios a partir de la producción de curare. [3] Así, el curare se convirtió en un símbolo de riqueza entre las poblaciones indígenas.
En 1596, Sir Walter Raleigh mencionó el veneno de las flechas en su libro Descubrimiento del gran, rico y hermoso imperio de Guayana (que se relaciona con sus viajes por Trinidad y Guayana ), aunque el veneno que describió posiblemente no fuera curare. [6] En 1780, el abad Félix Fontana descubrió que actuaba sobre los músculos voluntarios en lugar de sobre los nervios y el corazón. [7] En 1832, Alexander von Humboldt dio el primer relato occidental de cómo los nativos del río Orinoco preparaban la toxina a partir de plantas . [8]

Durante 1811-1812, Sir Benjamin Collins Brody experimentó con el curare ( woorara ). [9] [10] Fue el primero en demostrar que el curare no mata al animal y que la recuperación es completa si la respiración del animal se mantiene artificialmente. En 1825, Charles Waterton describió un experimento clásico en el que mantuvo viva una burra curarizada mediante respiración artificial con un fuelle a través de una traqueotomía . [11] A Waterton también se le atribuye haber traído el curare a Europa. [12] Robert Hermann Schomburgk , que era un botánico de formación, identificó la vid como uno del género Strychnos y le dio el nombre ahora aceptado Strychnos toxifera . [13]
George Harley (1829-1896) demostró en 1850 que el curare ( wourali ) era eficaz para el tratamiento del tétanos y la intoxicación por estricnina . [14] [15] En 1857, Claude Bernard (1813–1878) publicó los resultados de sus experimentos en los que demostró que el mecanismo de acción del curare era el resultado de la interferencia en la conducción de los impulsos nerviosos desde el nervio motor hasta el nervio motor . músculo esquelético , y que esta interferencia se produjo en la unión neuromuscular . [16] [17] Desde 1887, el catálogo de Burroughs Wellcome incluía bajo su marca 'Tabloids', 1 ⁄ 12 tabletas de curare de grano (5,4 mg) (precio: 8 chelines) para usar en la preparación de una solución para inyección hipodérmica. En 1914, Henry Hallett Dale (1875-1968) describió las acciones fisiológicas de la acetilcolina . [18] Después de 25 años, demostró que la acetilcolina es responsable de la transmisión neuromuscular , que puede ser bloqueada por el curare. [19]
_(14784389962).jpg/440px-The_Andes_and_the_Amazon_-bor_across_the_continent_of_South_America_(1876)_(14784389962).jpg)
La toxina más conocida e históricamente más importante (debido a sus aplicaciones médicas) es la d- tubocurarina . Fue aislado de la droga cruda –de una muestra de curare de museo– en 1935 por Harold King de Londres, trabajando en el laboratorio de Sir Henry Dale . King también estableció su estructura química. [20] [21] Pascual Scannone, un anestesiólogo venezolano [22] que se capacitó y especializó en la ciudad de Nueva York, realizó una extensa investigación sobre el curare como posible agente paralizante para los pacientes durante los procedimientos quirúrgicos. En 1942, se convirtió en la primera persona en América Latina en utilizar curare durante un procedimiento médico cuando realizó con éxito una intubación traqueal en un paciente a quien le administró curare para una parálisis muscular en el Hospital El Algodonal de Caracas, Venezuela. [22]
Después de su introducción en 1942, el curare/derivados del curare se convirtieron en un agente paralizante ampliamente utilizado durante procedimientos médicos y quirúrgicos. [ cita necesaria ] En medicina, el curare ha sido reemplazado por varios agentes similares al curare, como el pancuronio , que tienen un perfil farmacodinámico similar, pero menos efectos secundarios.
Los diversos componentes del curare son compuestos orgánicos clasificados como alcaloides de isoquinolina o indol . La tubocurarina es uno de los principales componentes activos del veneno para dardos sudamericano. [23] Como alcaloide, la tubocurarina es un compuesto natural que consta de bases nitrogenadas, aunque la estructura química de los alcaloides es muy variable.

La tubocurarina y la toxiferina C consisten en un sistema cíclico con iones de amonio cuaternario. Por otro lado, si bien la acetilcolina no contiene un sistema cíclico, sí contiene un ion amonio cuaternario. Debido a esta fracción compartida, los alcaloides del curare pueden unirse fácilmente al sitio activo de los receptores de acetilcolina (ACh) en la unión neuromuscular, bloqueando el envío de impulsos nerviosos a los músculos esqueléticos, paralizando efectivamente los músculos del cuerpo.
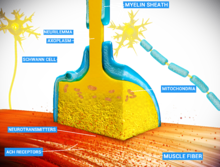
Curare es un ejemplo de un relajante muscular no despolarizante que bloquea el receptor nicotínico de acetilcolina (nAChR) , [24] uno de los dos tipos de receptores de acetilcolina (ACh) , en la unión neuromuscular . La principal toxina del curare, la d-tubocurarina , ocupa la misma posición en el receptor que la ACh con igual o mayor afinidad, y no provoca respuesta, lo que la convierte en un antagonista competitivo . El antídoto para la intoxicación por curare es un inhibidor de la acetilcolinesterasa (AChE) (anticolinesterasa), como la fisostigmina o la neostigmina . Al bloquear la degradación de la ACh, los inhibidores de la AChE aumentan la cantidad de ACh en la unión neuromuscular; la ACh acumulada corregirá el efecto del curare activando a un ritmo mayor los receptores no bloqueados por la toxina.
El tiempo de aparición varía desde un minuto (para la tubocurarina en administración intravenosa , que penetra en una vena más grande), hasta entre 15 y 25 minutos (para la administración intramuscular , donde la sustancia se aplica en el tejido muscular). [24]
Es inofensivo si se toma por vía oral [25] [26] porque los compuestos del curare son demasiado grandes y están muy cargados para pasar a través del revestimiento del tracto digestivo y ser absorbidos en la sangre. Por esta razón, las personas pueden comer presas envenenadas con curare de manera segura y no tiene ningún efecto sobre su sabor. [27]
Intentos aislados de utilizar curare durante la anestesia se remontan a 1912 por parte de Arthur Lawen de Leipzig, [28] pero el curare llegó a la anestesia a través de la psiquiatría ( electroplexia ). En 1939, Abram Elting Bennett lo utilizó para modificar la terapia convulsiva inducida por metrazol . [29] Los relajantes musculares se utilizan en la anestesia moderna por muchas razones, como proporcionar condiciones operativas óptimas y facilitar la intubación de la tráquea. Antes de los relajantes musculares, los anestesiólogos necesitaban utilizar dosis mayores del agente anestésico, como éter , cloroformo o ciclopropano para lograr estos objetivos. Una anestesia tan profunda corría el riesgo de matar a pacientes ancianos o con enfermedades cardíacas.
La fuente del curare en el Amazonas fue investigada por primera vez por Richard Evans Schultes en 1941. Desde la década de 1930, se utilizaba en hospitales como relajante muscular. Descubrió que los diferentes tipos de curare requerían hasta 15 ingredientes y, con el tiempo, ayudó a identificar más de 70 especies que producían la droga.
En la década de 1940, se utilizó en algunas ocasiones durante la cirugía porque se pensaba erróneamente que era un analgésico o anestésico. Los pacientes informaron haber sentido toda la intensidad del dolor, aunque no podían hacer nada al respecto ya que estaban esencialmente paralizados. [30]
El 23 de enero de 1942, Harold Griffith y Enid Johnson administraron una preparación sintética de curare (Intercostrin/Intocostrin) a un paciente sometido a una apendicectomía (para complementar la anestesia convencional). Los derivados del curare más seguros, como el rocuronio y el pancuronio , han reemplazado a la d-tubocurarina para la anestesia durante la cirugía. Cuando se usa con halotano, d-tubocurarina puede causar una caída profunda en la presión arterial en algunos pacientes, ya que ambos medicamentos son bloqueadores de ganglios . [31] Sin embargo, es más seguro usar d-tubocurarina con éter .
En 1954, Beecher y Todd publicaron un artículo que sugería que el uso de relajantes musculares (medicamentos similares al curare) aumentaba casi seis veces la muerte debida a la anestesia. [32] Esto fue refutado en 1956. [33]
Los anestesistas modernos tienen a su disposición una variedad de relajantes musculares para su uso en anestesia. La capacidad de producir relajación muscular independientemente de la sedación ha permitido a los anestesistas ajustar los dos efectos de forma independiente y sobre la marcha para garantizar que sus pacientes estén inconscientes y lo suficientemente relajados como para permitir la cirugía. El uso de bloqueadores neuromusculares conlleva el riesgo de que se produzca conciencia de la anestesia .
Existen decenas de plantas de las que se pueden aislar alcaloides isoquinolina e indol con efectos curarizantes, y que fueron utilizadas por tribus indígenas de Centro y Sudamérica para la producción de venenos para flechas. Entre ellos están:
En la familia Menispermaceae :
Otras familias:
También se han citado como fuentes algunas plantas de la familia Aristolochiaceae .
Los alcaloides con actividad similar al curare están presentes en plantas del género fabáceo Erythrina . [2]
La administración debe ser parenteral , ya que la absorción gastrointestinal es ineficaz. La toxicidad de los alcaloides del curare en humanos no se ha establecido sistemáticamente, pero se considera altamente tóxico y de acción lenta, con una dosis letal más baja reportada de 375 μg/kg (vía de administración desconocida). [35]
Para los animales, la dosis letal media de tubocurarina es: [35]
La muerte se puede prevenir mediante ventilación artificial hasta que el curare disminuya y se recupere la función muscular, en cuyo caso no se producen efectos permanentes del envenenamiento. [2]
En 1807, Alexander von Humboldt proporcionó el primer relato de un testigo ocular sobre la preparación del curare. [3] Se hierve en agua una mezcla de raspados jóvenes de corteza de la planta Strychnos , otras partes limpias de la planta y, ocasionalmente, veneno de serpiente durante dos días. Luego, este líquido se cuela y se evapora para crear una pasta oscura, espesa y viscosa cuya potencia se probará más adelante. [3] Se describió que esta pasta de curare tenía un sabor muy amargo.
En 1938, Richard Gill y su expedición recolectaron muestras de curare procesado y describieron su método de preparación tradicional; una de las especies vegetales utilizadas en aquella época era Chondrodendron tomentosum . [36]
A la preparación se le añaden diversas hierbas irritantes, insectos que pican, gusanos venenosos y diversas partes de anfibios y reptiles. Algunos de ellos aceleran el inicio de la acción o aumentan la toxicidad; otros impiden que la herida cicatrice o que la sangre se coagule.
La intoxicación por curare puede estar indicada por signos típicos de los fármacos bloqueadores neuromusculares, como parálisis que incluye la respiración, pero que no afecta directamente al corazón.
La intoxicación por curare se puede controlar mediante respiración artificial , como la reanimación boca a boca . En un estudio realizado con 29 voluntarios del ejército que estaban paralizados por curare, la respiración artificial logró mantener la saturación de oxígeno siempre por encima del 85%, [37] nivel en el que no hay evidencia de estado alterado de conciencia . [38] Sin embargo, el envenenamiento por curare imita el síndrome de encierro total en el sentido de que hay parálisis de todos los músculos del cuerpo controlados voluntariamente (incluidos los ojos), lo que hace prácticamente imposible que la víctima confirme el conocimiento mientras está paralizada. [39]
La respiración espontánea se reanuda una vez finalizado el tiempo de acción del curare, que generalmente oscila entre 30 minutos [40] y 8 horas, [41] dependiendo de la variante de la toxina y la dosis. El músculo cardíaco no se ve directamente afectado por el curare, pero si han pasado más de cuatro a seis minutos [42] desde el cese respiratorio, el músculo cardíaco puede dejar de funcionar debido a la falta de oxígeno, lo que hace necesaria la reanimación cardiopulmonar, incluidas las compresiones torácicas .
Dado que la tubocurarina y los demás componentes del curare se unen de manera reversible a los receptores de ACh, el tratamiento para la intoxicación por curare implica agregar un inhibidor de la acetilcolinesterasa (AChE), que detendrá la destrucción de la acetilcolina para que pueda competir con el curare. [43] Esto se puede hacer mediante la administración de inhibidores de la acetilcolinesterasa (AChE) como piridostigmina , [44] neostigmina , fisostigmina y edrofonio . La acetilcolinesterasa es una enzima que se utiliza para descomponer el neurotransmisor acetilcolina (ACh) que queda en las sinapsis de las neuronas motoras . Los inhibidores antes mencionados, denominados fármacos "anticurativos", se unen de forma reversible al sitio activo de la enzima, impidiendo su capacidad para unirse a su objetivo original, la ACh. Al bloquear la degradación de la ACh, los inhibidores de la AChE pueden aumentar eficazmente la cantidad de ACh presente en la unión neuromuscular. La ACh acumulada corregirá el efecto del curare activando a un ritmo mayor los receptores no bloqueados por la toxina, restaurando la actividad de las neuronas motoras y el movimiento corporal.