
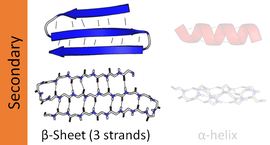

La lámina beta ( lámina β , también lámina β-plegada ) es un motivo común de la estructura secundaria regular de las proteínas . Las láminas beta consisten en cadenas beta ( cadenas β ) conectadas lateralmente por al menos dos o tres enlaces de hidrógeno de la cadena principal , formando una lámina generalmente retorcida y plegada. Una cadena β es un tramo de cadena polipeptídica típicamente de 3 a 10 aminoácidos de longitud con la cadena principal en una conformación extendida . La asociación supramolecular de las láminas β se ha implicado en la formación de las fibrillas y los agregados de proteínas observados en la amiloidosis , la enfermedad de Alzheimer y otras proteinopatías .

La primera estructura de lámina β fue propuesta por William Astbury en la década de 1930. Propuso la idea de la unión de hidrógeno entre los enlaces peptídicos de las hebras β extendidas paralelas o antiparalelas. Sin embargo, Astbury no tenía los datos necesarios sobre la geometría del enlace de los aminoácidos para construir modelos precisos, especialmente porque entonces no sabía que el enlace peptídico era plano. Linus Pauling y Robert Corey propusieron una versión refinada en 1951. Su modelo incorporó la planaridad del enlace peptídico que, según explicaron previamente, resultaba de la tautomerización ceto-enólica .
La mayoría de las cadenas β están dispuestas adyacentes a otras cadenas y forman una extensa red de enlaces de hidrógeno con sus vecinas en la que los grupos N−H en la cadena principal de una cadena establecen enlaces de hidrógeno con los grupos C=O en la cadena principal de las cadenas adyacentes. En la cadena β completamente extendida, las cadenas laterales sucesivas apuntan hacia arriba y hacia abajo en un patrón alterno. Las cadenas β adyacentes en una lámina β están alineadas de modo que sus átomos C α sean adyacentes y sus cadenas laterales apunten en la misma dirección. La apariencia "plisada" de las cadenas β surge de la unión química tetraédrica en el átomo C α ; por ejemplo, si una cadena lateral apunta hacia arriba, entonces los enlaces al C' deben apuntar ligeramente hacia abajo, ya que su ángulo de enlace es de aproximadamente 109,5°. El plisado hace que la distancia entre Cα
yoy Cα
yo + 2es de aproximadamente 6 Å (0,60 nm ), en lugar de los 7,6 Å (0,76 nm) esperados de dos péptidos trans completamente extendidos . La distancia "lateral" entre átomos C α adyacentes en cadenas β unidas por hidrógeno es de aproximadamente 5 Å (0,50 nm).

Sin embargo, las cadenas β rara vez se extienden perfectamente; más bien, presentan una torsión. Los ángulos diedros energéticamente preferidos cerca de ( φ , ψ ) = (–135°, 135°) (en términos generales, la región superior izquierda del diagrama de Ramachandran ) divergen significativamente de la conformación completamente extendida ( φ , ψ ) = (–180°, 180°). [1] La torsión a menudo se asocia con fluctuaciones alternas en los ángulos diedros para evitar que las cadenas β individuales en una lámina más grande se separen. Un buen ejemplo de una horquilla β fuertemente torcida se puede ver en la proteína BPTI .
Las cadenas laterales apuntan hacia afuera desde los pliegues de los pliegues, aproximadamente perpendicularmente al plano de la lámina; los residuos de aminoácidos sucesivos apuntan hacia afuera en caras alternas de la lámina.
Debido a que las cadenas peptídicas tienen una direccionalidad conferida por sus extremos N y C , también se puede decir que las cadenas β son direccionales. Por lo general, se representan en los diagramas de topología de proteínas mediante una flecha que apunta hacia el extremo C. Las cadenas β adyacentes pueden formar enlaces de hidrógeno en disposiciones antiparalelas, paralelas o mixtas.
En una disposición antiparalela, las hebras β sucesivas alternan direcciones de modo que el extremo N de una hebra es adyacente al extremo C de la siguiente. Esta es la disposición que produce la mayor estabilidad entre hebras porque permite que los enlaces de hidrógeno entre hebras entre carbonilos y aminas sean planos, que es su orientación preferida. Los ángulos diedros de la estructura principal del péptido ( φ , ψ ) son de aproximadamente (–140°, 135°) en láminas antiparalelas. En este caso, si dos átomos de Cα
yoy Cαj
son adyacentes en dos cadenas β unidas por enlaces de hidrógeno , luego forman dos enlaces de hidrógeno mutuos en la cadena principal con los grupos peptídicos flanqueantes de cada uno ; esto se conoce como un par cercano de enlaces de hidrógeno.
En una disposición paralela, todos los extremos N de las hebras sucesivas están orientados en la misma dirección; esta orientación puede ser ligeramente menos estable porque introduce no planaridad en el patrón de enlaces de hidrógeno entre hebras. Los ángulos diedros ( φ , ψ ) son de aproximadamente (–120°, 115°) en láminas paralelas. Es raro encontrar menos de cinco hebras paralelas interactuantes en un motivo, lo que sugiere que un número menor de hebras puede ser inestable, sin embargo, también es fundamentalmente más difícil que se formen láminas β paralelas porque las hebras con extremos N y C alineados necesariamente deben estar muy distantes en secuencia [ cita requerida ] . También hay evidencia de que las láminas β paralelas pueden ser más estables ya que las secuencias amiloidogénicas pequeñas parecen agregarse generalmente en fibrillas de láminas β compuestas principalmente de hebras de láminas β paralelas, donde uno esperaría fibrillas antiparalelas si las antiparalelas fueran más estables.
En la estructura de láminas β paralelas, si dos átomos de Cα
yoy Cαj
Si dos cadenas β unidas por puentes de hidrógeno están adyacentes , no forman puentes de hidrógeno entre sí, sino que un residuo forma puentes de hidrógeno con los residuos que flanquean al otro (pero no al revés). Por ejemplo, el residuo i puede formar puentes de hidrógeno con los residuos j − 1 y j + 1; esto se conoce como un par amplio de puentes de hidrógeno. Por el contrario, el residuo j puede formar puentes de hidrógeno con diferentes residuos en conjunto, o con ninguno en absoluto.
La disposición del enlace de hidrógeno en una lámina beta paralela se asemeja a la de un motivo de anillo de amida con 11 átomos.
Por último, una hebra individual puede presentar un patrón de unión mixto, con una hebra paralela en un lado y una hebra antiparalela en el otro. Estas disposiciones son menos comunes de lo que sugeriría una distribución aleatoria de orientaciones, lo que sugiere que este patrón es menos estable que la disposición antiparalela; sin embargo, el análisis bioinformático siempre tiene dificultades para extraer la termodinámica estructural, ya que siempre hay muchas otras características estructurales presentes en las proteínas completas. Además, las proteínas están inherentemente limitadas por la cinética de plegamiento, así como por la termodinámica de plegamiento, por lo que siempre se debe tener cuidado al concluir la estabilidad a partir del análisis bioinformático.
La unión de hidrógeno de las cadenas β no necesita ser perfecta, pero puede presentar disrupciones localizadas conocidas como protuberancias β .
Los enlaces de hidrógeno se encuentran aproximadamente en el plano de la lámina, con los grupos carbonilo del péptido apuntando en direcciones alternas con residuos sucesivos; a modo de comparación, los carbonilos sucesivos apuntan en la misma dirección en la hélice alfa .
Los residuos aromáticos grandes ( tirosina , fenilalanina , triptófano ) y los aminoácidos β-ramificados ( treonina , valina , isoleucina ) se encuentran preferentemente en las cadenas β en el medio de las láminas β. Es probable que se encuentren diferentes tipos de residuos (como prolina ) en las cadenas de los bordes de las láminas β, presumiblemente para evitar la asociación "borde con borde" entre proteínas que podría conducir a la agregación y la formación de amiloide . [2]


Un motivo estructural muy simple que involucra láminas β es la horquilla β , en la que dos cadenas antiparalelas están unidas por un bucle corto de dos a cinco residuos, de los cuales uno es frecuentemente una glicina o una prolina , los cuales pueden asumir las conformaciones de ángulo diedro requeridas para un giro cerrado o un bucle de protuberancia β . Las cadenas individuales también pueden unirse de formas más elaboradas con bucles más largos que pueden contener hélices α .
El motivo de la clave griega consta de cuatro hebras antiparalelas adyacentes y sus bucles de enlace. Consiste en tres hebras antiparalelas conectadas por horquillas, mientras que la cuarta es adyacente a la primera y está unida a la tercera por un bucle más largo. Este tipo de estructura se forma fácilmente durante el proceso de plegamiento de proteínas . [3] [4] Recibió su nombre de un patrón común en las obras de arte ornamental griegas (véase meandro ).
Debido a la quiralidad de sus aminoácidos componentes, todas las cadenas exhiben una torsión hacia la derecha evidente en la mayoría de las estructuras de láminas β de orden superior. En particular, el bucle de enlace entre dos cadenas paralelas casi siempre tiene una quiralidad de cruce hacia la derecha, que se ve fuertemente favorecida por la torsión inherente de la lámina. [5] Este bucle de enlace contiene frecuentemente una región helicoidal, en cuyo caso se denomina motivo β-α-β. Un motivo estrechamente relacionado llamado motivo β-α-β-α forma el componente básico de la estructura terciaria de proteínas más comúnmente observada , el barril TIM .


Una topología proteica supersecundaria simple compuesta por dos o más cadenas β antiparalelas consecutivas unidas entre sí por bucles de horquilla . [7] [8] Este motivo es común en las láminas β y se puede encontrar en varias arquitecturas estructurales, incluidos los barriles β y las hélices β .
La gran mayoría de las regiones de meandro β en las proteínas se encuentran empaquetadas contra otros motivos o secciones de la cadena polipeptídica, formando porciones del núcleo hidrofóbico que canónicamente impulsa la formación de la estructura plegada. [9] Sin embargo, varias excepciones notables incluyen las variantes de la proteína de superficie externa A (OspA) [6] y las proteínas de lámina β de capa única (SLBP) [10] que contienen láminas β de capa única en ausencia de un núcleo hidrofóbico tradicional. Estas proteínas ricas en β presentan láminas β de meandro β de capa única extendidas que se estabilizan principalmente a través de interacciones entre cadenas β e interacciones hidrofóbicas presentes en las regiones de giro que conectan cadenas individuales.
El motivo de bucle psi (bucle Ψ) consta de dos cadenas antiparalelas con una cadena intermedia que está conectada a ambas por enlaces de hidrógeno. [11] Hay cuatro posibles topologías de cadena para bucles Ψ individuales. [12] Este motivo es poco común, ya que el proceso que resulta en su formación parece poco probable que ocurra durante el plegamiento de proteínas. El bucle Ψ se identificó por primera vez en la familia de proteasas aspárticas . [12]
Las láminas β están presentes en los dominios all-β , α+β y α/β , y en muchos péptidos o proteínas pequeñas con una arquitectura general mal definida. [13] [14] Los dominios all-β pueden formar barriles β , sándwiches β , prismas β, hélices β y hélices β .
La topología de una lámina β describe el orden de las hebras β unidas por enlaces de hidrógeno a lo largo de la cadena principal. Por ejemplo, el pliegue de flavodoxina tiene una lámina β paralela de cinco cadenas con topología 21345; por lo tanto, las hebras del borde son la hebra β 2 y la hebra β 5 a lo largo de la cadena principal. Explícitamente, la hebra β 2 está unida por hidrógeno a la hebra β 1, que está unida por hidrógeno a la hebra β 3, que está unida por hidrógeno a la hebra β 4, que está unida por hidrógeno a la hebra β 5, la otra hebra del borde. En el mismo sistema, el motivo de clave griega descrito anteriormente tiene una topología 4123. La estructura secundaria de una lámina β se puede describir de forma aproximada dando el número de hebras, su topología y si sus enlaces de hidrógeno son paralelos o antiparalelos.
Las láminas β pueden ser abiertas , lo que significa que tienen dos hebras de borde (como en el pliegue de flavodoxina o el pliegue de inmunoglobulina ) o pueden ser barriles β cerrados (como el barril TIM ). Los barriles β a menudo se describen por su escalonamiento o cizallamiento . Algunas láminas β abiertas son muy curvadas y se pliegan sobre sí mismas (como en el dominio SH3 ) o forman formas de herradura (como en el inhibidor de ribonucleasa ). Las láminas β abiertas pueden ensamblarse cara a cara (como el dominio de hélice β o el pliegue de inmunoglobulina ) o borde a borde, formando una gran lámina β.
Las estructuras de láminas β plegadas están formadas por cadenas polipeptídicas de hebras β extendidas, con hebras unidas a sus vecinas por enlaces de hidrógeno . Debido a esta conformación de estructura extendida, las láminas β resisten el estiramiento . Las láminas β en las proteínas pueden realizar un movimiento de acordeón de baja frecuencia, como se observa mediante la espectroscopia Raman [15] y se analiza con el modelo cuasi-continuo. [16]

Una hélice β se forma a partir de unidades estructurales repetidas que consisten en dos o tres cadenas β cortas unidas por bucles cortos. Estas unidades se "apilan" unas sobre otras en forma helicoidal, de modo que las repeticiones sucesivas de la misma cadena forman puentes de hidrógeno entre sí en una orientación paralela. Consulte el artículo sobre la hélice β para obtener más información.
En las hélices β levógiras, las hebras en sí son bastante rectas y no están retorcidas; las superficies helicoidales resultantes son casi planas y forman una forma de prisma triangular regular , como se muestra en la anhidrasa carbónica arqueal 1QRE a la derecha. Otros ejemplos son la enzima de síntesis de lípido A LpxA y las proteínas anticongelantes de insectos con una disposición regular de cadenas laterales Thr en una cara que imitan la estructura del hielo. [17]

Las β-hélices dextrógiras, tipificadas por la enzima pectato liasa que se muestra a la izquierda o la proteína de cola del fago P22 , tienen una sección transversal menos regular, más larga y con sangría en uno de los lados; de los tres bucles de enlace, uno tiene consistentemente solo dos residuos de largo y los otros son variables, a menudo elaborados para formar un sitio de unión o activo. [18]
Una β-hélice de dos lados (dextrógiras) se encuentra en algunas metaloproteasas bacterianas ; sus dos bucles tienen cada uno seis residuos de largo y se unen a iones de calcio estabilizadores para mantener la integridad de la estructura, utilizando la cadena principal y los oxígenos de la cadena lateral Asp de un motivo de secuencia GGXGXD. [19] Este pliegue se llama β-rollo en la clasificación SCOP.
Algunas proteínas que están desordenadas o tienen forma helicoidal como monómeros, como la amiloide β (ver placa amiloide ) pueden formar estructuras oligoméricas ricas en láminas β asociadas con estados patológicos. La forma oligomérica de la proteína amiloide β está implicada como causa del Alzheimer . Su estructura aún no se ha determinado por completo, pero datos recientes sugieren que puede parecerse a una inusual hélice β de dos hebras. [20]
Las cadenas laterales de los residuos de aminoácidos que se encuentran en una estructura de lámina β también pueden estar dispuestas de tal manera que muchas de las cadenas laterales adyacentes en un lado de la lámina sean hidrófobas, mientras que muchas de las adyacentes entre sí en el lado alternativo de la lámina sean polares o cargadas (hidrófilas), [21] lo que puede ser útil si la lámina va a formar un límite entre entornos polares/acuosos y no polares/grasosos.
{{cite book}}: |journal=ignorado ( ayuda )