La terapia con células madre utiliza células madre para tratar o prevenir una enfermedad o afección. [1] A partir de 2024 [actualizar], la única terapia aprobada por la FDA que utiliza células madre es el trasplante de células madre hematopoyéticas . [2] [3] Esto generalmente toma la forma de un trasplante de células madre de médula ósea o sangre periférica , pero las células también pueden derivarse de la sangre del cordón umbilical . Se están realizando investigaciones para desarrollar varias fuentes de células madre, así como para aplicar tratamientos con células madre para enfermedades neurodegenerativas [4] y afecciones como la diabetes y las enfermedades cardíacas .
La terapia con células madre ha generado controversia a raíz de avances como la capacidad de los científicos para aislar y cultivar células madre embrionarias , crear células madre mediante transferencia nuclear de células somáticas y el uso de técnicas para crear células madre pluripotentes inducidas . Esta controversia suele estar relacionada con las políticas abortistas y la clonación humana . Además, los esfuerzos por comercializar tratamientos basados en el trasplante de sangre de cordón umbilical almacenada han sido controvertidos.
Durante más de 90 años, el trasplante de células madre hematopoyéticas (TCMH) se ha utilizado para tratar a personas con enfermedades como la leucemia y el linfoma ; esta es la única forma ampliamente practicada de terapia con células madre. [5] [6] [7] Durante la quimioterapia , la mayoría de las células en crecimiento son destruidas por los agentes citotóxicos . Estos agentes, sin embargo, no pueden discriminar entre las células leucémicas o neoplásicas y las células madre hematopoyéticas dentro de la médula ósea. Este es el efecto secundario de las estrategias de quimioterapia convencionales que el trasplante de células madre intenta revertir; la médula ósea sana de un donante reintroduce células madre funcionales para reemplazar las células perdidas en el cuerpo del huésped durante el tratamiento. Las células trasplantadas también generan una respuesta inmune que ayuda a matar las células cancerosas; este proceso puede ir demasiado lejos, sin embargo, dando lugar a la enfermedad de injerto contra huésped , el efecto secundario más grave de este tratamiento. [8]
En 2012, Canadá aprobó condicionalmente otra terapia con células madre, denominada Prococvhymal, para el tratamiento de la enfermedad injerto contra huésped aguda en niños que no responden a los esteroides. [9] Se trata de una terapia alogénica basada en células madre mesenquimales (MSC) derivadas de la médula ósea de donantes adultos. Las MSC se purifican a partir de la médula ósea, se cultivan y se envasan, y se obtienen hasta 10 000 dosis de un solo donante. Las dosis se almacenan congeladas hasta que se necesitan. [10]
La FDA ha aprobado cinco productos de células madre hematopoyéticas derivadas de la sangre del cordón umbilical para el tratamiento de enfermedades sanguíneas e inmunológicas. [11]
En 2014, la Agencia Europea de Medicamentos recomendó la aprobación del uso de células madre limbares para personas con deficiencia grave de células madre limbares debido a quemaduras en el ojo. [12]
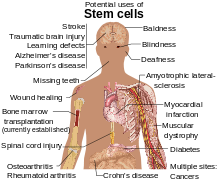
Las células madre se están estudiando por varias razones. Las moléculas y los exosomas liberados por las células madre también se están estudiando en un esfuerzo por fabricar medicamentos. [13] Además de las funciones de las propias células, se ha descubierto que los factores solubles paracrinos producidos por las células madre, conocidos como secretoma de células madre , son otro mecanismo por el cual las terapias basadas en células madre median sus efectos en enfermedades degenerativas , autoinmunes e inflamatorias . [14]
La mayoría de las células madre destinadas a la terapia regenerativa generalmente se aíslan de la médula ósea del paciente o del tejido adiposo . [15] [16] Las células madre mesenquimales pueden diferenciarse en las células que forman el hueso, el cartílago, los tendones y los ligamentos, así como los músculos, los nervios y otros tejidos progenitores. Han sido el principal tipo de células madre estudiado en el tratamiento de enfermedades que afectan a estos tejidos. [17] [18] La cantidad de células madre trasplantadas en el tejido dañado puede alterar la eficacia del tratamiento. En consecuencia, las células madre derivadas de aspirados de médula ósea, por ejemplo, se cultivan en laboratorios especializados para su expansión a millones de células. [15] [16] Aunque el tejido derivado de tejido adiposo también requiere procesamiento antes de su uso, la metodología de cultivo para células madre derivadas de tejido adiposo no es tan extensa como la de las células derivadas de médula ósea. [19] Si bien se cree que las células madre derivadas de la médula ósea son las preferidas para la reparación de huesos, cartílagos, ligamentos y tendones, otros creen que las técnicas de recolección menos desafiantes y el microambiente multicelular ya presente en las fracciones de células madre derivadas de tejido adiposo hacen que estas últimas sean la fuente preferida para el trasplante autólogo. [20]
Se están investigando nuevas fuentes de células madre mesenquimales , incluidas las células madre presentes en la piel y la dermis, que son de interés debido a la facilidad con la que se pueden recolectar con un riesgo mínimo para el animal. [21] También se ha descubierto que las células madre hematopoyéticas viajan en el torrente sanguíneo y poseen la misma capacidad de diferenciación que otras células madre mesenquimales , nuevamente con una técnica de recolección muy no invasiva. [22]
Recientemente, se ha despertado un interés más amplio en el uso de células madre mesenquimales extraembrionarias . Se están realizando investigaciones para examinar las capacidades de diferenciación de las células madre que se encuentran en el cordón umbilical, el saco vitelino y la placenta de diferentes animales. Se cree que estas células madre tienen una mayor capacidad de diferenciación que sus contrapartes adultas, incluida la capacidad de formar más fácilmente tejidos de origen endodérmico y ectodérmico. [23]
A partir de 2010, hubo una controversia generalizada sobre el uso de células madre embrionarias humanas . Esta controversia se dirige principalmente a las técnicas utilizadas para derivar nuevas líneas de células madre embrionarias , que a menudo requieren la destrucción del blastocisto . La oposición al uso de células madre embrionarias humanas en la investigación a menudo se basa en objeciones filosóficas, morales o religiosas. [24] Existe otra investigación con células madre que no implica la destrucción de un embrión humano, y dicha investigación involucra células madre adultas, células madre amnióticas y células madre pluripotentes inducidas.
En enero de 2009, la Administración de Alimentos y Medicamentos de Estados Unidos autorizó a Geron Corporation a realizar el primer ensayo clínico de una terapia basada en células madre embrionarias en seres humanos. El ensayo tenía como objetivo evaluar el fármaco GRNOPC1, células progenitoras de oligodendrocitos derivadas de células madre embrionarias , en personas con lesión aguda de la médula espinal . El ensayo se interrumpió en noviembre de 2011 para que la empresa pudiera centrarse en terapias en el "entorno actual de escasez de capital y condiciones económicas inciertas". [25] En 2013, la empresa de biotecnología y medicina regenerativa BioTime ( AMEX : BTX) adquirió los activos de células madre de Geron en una transacción de acciones, con el objetivo de reiniciar el ensayo clínico. [26]
Los científicos informaron en 2012 que las MSC transfundidas inmediatamente después de la descongelación pueden mostrar una función reducida o una eficacia reducida en el tratamiento de enfermedades en comparación con las MSC que están en la fase logarítmica de crecimiento celular (frescas), por lo que las MSC criopreservadas deben volver a la fase logarítmica de crecimiento celular en un cultivo in vitro antes de su administración. El recultivo de las MSC ayudará a recuperarse del shock que sufren las células durante la congelación y la descongelación. Varios ensayos clínicos de MSC que utilizaron productos criopreservados inmediatamente después de la descongelación han fracasado en comparación con los ensayos clínicos que utilizaron MSC frescas. [27]
La capacidad de cultivar tejidos adultos funcionales de forma indefinida mediante la diferenciación dirigida crea nuevas oportunidades para la investigación de fármacos. Los investigadores pueden cultivar líneas celulares diferenciadas y luego probar nuevos fármacos en cada tipo de célula para examinar posibles interacciones in vitro antes de realizar estudios in vivo . Esto es fundamental en el desarrollo de fármacos para su uso en la investigación veterinaria debido a las posibilidades de interacciones específicas entre especies. La esperanza es que tener estas líneas celulares disponibles para su uso en investigación reducirá la necesidad de utilizar animales de investigación porque los efectos sobre el tejido humano in vitro proporcionarán información que normalmente no se conoce antes de la fase de prueba con animales. [28]
Para su uso en aplicaciones de investigación o tratamiento, se necesitan grandes cantidades de células madre de alta calidad. Por lo tanto, es necesario desarrollar sistemas de cultivo que produzcan poblaciones puras de células madre específicas de tejido in vitro sin pérdida del potencial de las células madre. Para este fin se utilizan dos enfoques principales: cultivo celular bidimensional y tridimensional. [29]
El cultivo de células en dos dimensiones se ha llevado a cabo de forma rutinaria en miles de laboratorios de todo el mundo durante las últimas cuatro décadas. En plataformas bidimensionales, las células suelen estar expuestas a una superficie plana, sólida y rígida en el lado basal y a un líquido en la superficie apical. Habitar en un sustrato tan rígido y bidimensional requiere una adaptación drástica para las células supervivientes, ya que carecen de la matriz extracelular que es exclusiva de cada tipo de célula, lo que puede alterar el metabolismo celular y reducir su funcionalidad. [29]
Los sistemas de cultivo celular tridimensionales pueden crear un microambiente biomimético para las células madre, similar a su matriz extracelular (ECM) tridimensional nativa. Los biomateriales avanzados han contribuido significativamente a los sistemas de cultivo celular tridimensional en las últimas décadas, y se han propuesto biomateriales más únicos y complejos para mejorar la proliferación y la diferenciación controlada de las células madre. Entre ellos, los biomateriales nanoestructurados son de particular interés porque tienen la ventaja de una alta relación superficie-volumen, e imitan las características físicas y biológicas de la ECM natural a escala nanométrica. [29]
Se cree que las células madre median la reparación a través de cinco mecanismos principales: 1) proporcionar un efecto antiinflamatorio, 2) dirigirse a los tejidos dañados y reclutar otras células, como las células progenitoras endoteliales , que son necesarias para el crecimiento del tejido, 3) apoyar la remodelación del tejido en lugar de la formación de cicatrices, 4) inhibir la apoptosis y 5) diferenciarse en tejido óseo, cartilaginoso, tendinoso y ligamentoso. [30] [31]
Para enriquecer aún más el suministro de sangre a las áreas dañadas y, en consecuencia, promover la regeneración tisular, se podría utilizar plasma rico en plaquetas junto con el trasplante de células madre. [20] [15] La eficacia de algunas poblaciones de células madre también puede verse afectada por el método de administración; por ejemplo, para regenerar el hueso, las células madre a menudo se introducen en un andamio donde producen los minerales necesarios para la generación de hueso funcional. [20] [15] [32] [16]
Se ha demostrado que las células madre tienen una baja inmunogenicidad debido al número relativamente bajo de moléculas MHC que se encuentran en su superficie. Además, se ha descubierto que secretan quimiocinas que alteran la respuesta inmunitaria y promueven la tolerancia del nuevo tejido. Esto permite que los tratamientos alogénicos se realicen sin un alto riesgo de rechazo. [23]
Se han realizado investigaciones sobre los efectos de las células madre en modelos animales de degeneración cerebral , como en la enfermedad de Parkinson , la esclerosis lateral amiotrófica y la enfermedad de Alzheimer . [33] [34] [35] Se han realizado estudios preliminares relacionados con la esclerosis múltiple , [36] [37] [38] y un ensayo de fase 2 de 2020 encontró resultados significativamente mejorados para los pacientes tratados con células madre mesenquimales en comparación con los que recibieron un tratamiento simulado. [39] En enero de 2021, la FDA aprobó el primer ensayo clínico para una terapia de células madre en investigación para restaurar las células cerebrales perdidas en personas con enfermedad de Parkinson avanzada. [40]
Los cerebros adultos sanos contienen células madre neuronales , que se dividen para mantener el número general de células madre o se convierten en células progenitoras . En animales de laboratorio adultos sanos, las células progenitoras migran dentro del cerebro y funcionan principalmente para mantener las poblaciones de neuronas para el olfato (el sentido del olfato). Se ha informado que la activación farmacológica de células madre neuronales endógenas induce neuroprotección y recuperación conductual en modelos de ratas adultas con trastornos neurológicos. [41] [42] [43]
Los accidentes cerebrovasculares y las lesiones cerebrales traumáticas provocan la muerte celular , caracterizada por la pérdida de neuronas y oligodendrocitos en el cerebro. Se han realizado estudios clínicos y en animales sobre el uso experimental de células madre en casos de lesión de la médula espinal . [44] [45] [46] [38]
En 2017, un estudio a pequeña escala sobre personas de 60 años o más con fragilidad asociada al envejecimiento mostró, después del tratamiento intravenoso con células madre mesenquimales (MSC) de donantes jóvenes sanos, mejoras significativas en las medidas de rendimiento físico. Las MSC ayudan a bloquear la inflamación al disminuirla, lo que hace que se reviertan los efectos de la fragilidad. [47]
En 2012, se estudiaron células madre en personas con enfermedades cardíacas graves . [48] El trabajo de Bodo-Eckehard Strauer [49] fue desacreditado al identificar cientos de contradicciones fácticas. [50] Entre varios ensayos clínicos que informaron que la terapia con células madre adultas es segura y efectiva, solo se han reportado evidencias reales de beneficios de unos pocos estudios. [51] Algunos ensayos clínicos preliminares lograron solo mejoras modestas en la función cardíaca luego del uso de la terapia con células madre de la médula ósea . [52] [53]
La terapia con células madre para el tratamiento del infarto de miocardio generalmente utiliza células madre autólogas de médula ósea, pero se pueden utilizar otros tipos de células madre adultas, como las células madre derivadas de tejido adiposo. [54]
Los posibles mecanismos de recuperación incluyen: [33] Generación de células musculares cardíacas, estimulación del crecimiento de nuevos vasos sanguíneos para repoblar el tejido cardíaco dañado y secreción de factores de crecimiento .
La especificidad del repertorio de células inmunitarias humanas es lo que permite al cuerpo humano defenderse de los antígenos que se adaptan rápidamente. Sin embargo, el sistema inmunitario es vulnerable a la degradación en la patogénesis de la enfermedad y, debido al papel crítico que desempeña en la defensa general, su degradación a menudo es fatal para el organismo en su conjunto. Las enfermedades de las células hematopoyéticas se diagnostican y clasifican a través de una subespecialidad de patología conocida como hematopatología . La especificidad de las células inmunitarias es lo que permite el reconocimiento de antígenos extraños, lo que provoca más desafíos en el tratamiento de la enfermedad inmunitaria. Ya no se requieren coincidencias idénticas entre el donante y el receptor para un trasplante exitoso. En cambio, las coincidencias haploidénticas han facilitado numerosos trasplantes, dadas las mejoras en los regímenes inmunosupresores posteriores al trasplante. [55] La investigación que utiliza células madre adultas hematopoyéticas y células madre embrionarias ha proporcionado información sobre los posibles mecanismos y métodos de tratamiento para muchas de estas dolencias. [56]
Los glóbulos rojos humanos completamente maduros pueden generarse ex vivo a partir de células madre hematopoyéticas (CMH), que son precursoras de los glóbulos rojos. En este proceso, las CMH se cultivan junto con células del estroma , creando un entorno que imita las condiciones de la médula ósea, el sitio natural de crecimiento de los glóbulos rojos. Se añade eritropoyetina , un factor de crecimiento , que induce a las células madre a completar la diferenciación terminal en glóbulos rojos. [57] La investigación futura sobre esta técnica debería tener beneficios potenciales para la terapia génica, la transfusión de sangre y la medicina tópica.
En 2004, los científicos del King's College de Londres descubrieron una forma de cultivar un diente completo en ratones [58] y lograron hacer crecer dientes biodiseñados de manera independiente en el laboratorio. Los investigadores confían en que la tecnología de regeneración dental se pueda utilizar para hacer crecer dientes vivos en personas.
En teoría, las células madre extraídas del paciente podrían ser inducidas en el laboratorio a convertirse en un brote dental que, al implantarse en las encías, dará lugar a un nuevo diente, y se espera que crezca en un período de más de tres semanas. [59] Se fusionará con el hueso maxilar y liberará sustancias químicas que estimulan a los nervios y vasos sanguíneos a conectarse con él. El proceso es similar a lo que sucede cuando los seres humanos desarrollan sus dientes adultos originales. Sin embargo, aún quedan muchos desafíos antes de que las células madre puedan ser una opción para el reemplazo de dientes faltantes en el futuro. [60] [61]
Heller ha informado que ha tenido éxito en el recrecimiento de células ciliadas de la cóclea con el uso de células madre embrionarias . [62]
En una revisión de 2019 que analizó la regeneración auditiva y la medicina regenerativa, los progenitores óticos derivados de células madre tienen el potencial de mejorar enormemente la audición. [63]
Desde 2003, los investigadores han trasplantado con éxito células madre de la córnea en ojos dañados para restaurar la visión. "Las láminas de células de la retina utilizadas por el equipo se extraen de fetos abortados, lo que algunas personas consideran inaceptable". Cuando estas láminas se trasplantan sobre la córnea dañada , las células madre estimulan una nueva reparación, restaurando finalmente la visión. [64] El último desarrollo de este tipo se produjo en junio de 2005, cuando los investigadores del Hospital Queen Victoria de Sussex , Inglaterra, pudieron restaurar la vista de cuarenta personas utilizando la misma técnica. El grupo, dirigido por Sheraz Daya , pudo utilizar con éxito células madre adultas obtenidas del paciente, un familiar o incluso un cadáver . Se están llevando a cabo más rondas de ensayos. [65]
Las personas con diabetes tipo 1 pierden la función de las células beta productoras de insulina dentro del páncreas. En una publicación de experimentos de 2007, los científicos han podido convencer a las células madre embrionarias para que se conviertan en células beta en el laboratorio. En teoría, si la célula beta se trasplanta con éxito, podrá reemplazar a las que funcionan mal en un paciente diabético. [66] Sin embargo, las altas concentraciones de glucosa tienen efectos adversos en la terapia con células madre. [67]

A partir de 2017, el uso de células madre mesenquimales (MSC) derivadas de células madre adultas estaba bajo investigación preliminar para posibles aplicaciones ortopédicas en traumatismos óseos y musculares, reparación de cartílago , osteoartritis , cirugía de disco intervertebral , cirugía del manguito rotador y trastornos musculoesqueléticos , entre otros. [68] Otras áreas de investigación ortopédica para usos de MSC incluyen ingeniería de tejidos y medicina regenerativa . [68]
Las células madre también se pueden utilizar para estimular el crecimiento de tejidos humanos. En un adulto, el tejido herido se reemplaza con mayor frecuencia por tejido cicatricial , que se caracteriza en la piel por una estructura de colágeno desorganizada, pérdida de folículos pilosos y estructura vascular irregular. Sin embargo, en el caso del tejido fetal herido, el tejido herido se reemplaza por tejido normal a través de la actividad de las células madre. [69] Un posible método para la regeneración de tejidos en adultos es colocar "semillas" de células madre adultas dentro de un "suelo" de lecho de tejido en un lecho de herida y permitir que las células madre estimulen la diferenciación en las células del lecho de tejido. Este método provoca una respuesta regenerativa más similar a la curación de heridas fetales que a la formación de tejido cicatricial adulto. [69] A partir de 2018, los investigadores todavía estaban investigando diferentes aspectos del tejido "suelo" que conducen a la regeneración. [69] Debido a las capacidades generales de curación de las células madre, han ganado interés para el tratamiento de heridas cutáneas, como en el cáncer de piel . [70]
En 2013, los científicos han estado investigando un enfoque alternativo para tratar el VIH-1/SIDA, basado en la creación de un sistema inmunológico resistente a la enfermedad mediante el trasplante de células madre y progenitoras hematopoyéticas autólogas modificadas genéticamente (resistentes al VIH-1) (GM-HSPC). [71]
En 2013, se encontró que los estudios de células madre autólogas de médula ósea sobre la función ventricular contenían "cientos" de discrepancias. [50] Los críticos informan que de 48 informes, solo cinco ensayos subyacentes parecían haber sido utilizados, y que en muchos casos, ya fueran aleatorizados o meramente observacionales, la diferencia entre los informes del mismo ensayo era contradictoria. Un par de informes con características iniciales y resultados finales idénticos se presentó en dos publicaciones como, respectivamente, un ensayo aleatorizado de 578 pacientes y como un estudio observacional de 391 sujetos. Otros informes exigían desviaciones estándar negativas (imposibles) en subconjuntos de personas o contenían sujetos fraccionarios, clases negativas de la NYHA. En general, se informó que muchas más personas habían recibido células madre en los ensayos que el número de células madre procesadas en el laboratorio del hospital durante ese tiempo. Una investigación universitaria, cerrada en 2012 sin informe, se reabrió en julio de 2013. [72]
En 2014, un metanálisis sobre la terapia con células madre utilizando células madre de la médula ósea para enfermedades cardíacas reveló discrepancias en los informes de ensayos clínicos publicados, por lo que los estudios con un mayor número de discrepancias mostraron un aumento en los tamaños del efecto. [73] Otro metanálisis basado en los datos intra-sujeto de 12 ensayos aleatorios no pudo encontrar ningún beneficio significativo de la terapia con células madre en los puntos finales primarios, como eventos adversos importantes o aumento en las medidas de la función cardíaca, y concluyó que no hubo ningún beneficio. [74]
Los resultados de 2018 del ensayo TIME, que utilizó un diseño de ensayo aleatorizado, doble ciego y controlado con placebo, concluyeron que "la administración de células mononucleares de médula ósea no mejoró la recuperación de la función del VI durante 2 años" en personas que habían tenido un infarto de miocardio. [75] En consecuencia, el ensayo BOOST-2 realizado en 10 centros médicos en Alemania y Noruega informó que el resultado del ensayo "no respalda el uso de células madre mononucleares en pacientes con STEMI y FEVI moderadamente reducida". [76] Además, el ensayo tampoco cumplió con ningún otro criterio de valoración secundario de resonancia magnética, [77] lo que lleva a la conclusión de que la terapia intracoronaria con células madre de médula ósea no ofrece un beneficio funcional o clínico. [78]
En 2021, las inyecciones de células madre en los EE. UU. han causado infecciones graves en al menos 20 pacientes que recibieron productos derivados de la sangre del cordón umbilical comercializados como "tratamiento con células madre". [79] En 2023, se publicó el caso de una mujer que se infectó con Mycobacterium abscessus y sufrió meningitis después del tratamiento con células madre para la esclerosis múltiple en una clínica comercial en Baja California, México. [80]
Las investigaciones realizadas en caballos, perros y gatos han llevado al desarrollo de tratamientos con células madre en medicina veterinaria que pueden dirigirse a una amplia gama de lesiones y enfermedades, como infarto de miocardio , accidente cerebrovascular, daño en tendones y ligamentos , osteoartritis , osteocondrosis y distrofia muscular , tanto en animales grandes como en humanos. [81] [82] [83] [84] Si bien la investigación de terapias basadas en células generalmente refleja las necesidades médicas humanas, el alto grado de frecuencia y gravedad de ciertas lesiones en caballos de carreras ha colocado a la medicina veterinaria a la vanguardia de este novedoso enfoque regenerativo. [85] Los animales de compañía pueden servir como modelos clínicamente relevantes que imitan de cerca la enfermedad humana. [86] [87]
Las aplicaciones veterinarias de la terapia con células madre como un medio de regeneración tisular han sido en gran medida determinadas por la investigación que comenzó con el uso de células madre mesenquimales derivadas de adultos para tratar animales con lesiones o defectos que afectan a los huesos, cartílagos, ligamentos y/o tendones. [88] [17] [89] Hay dos categorías principales de células madre utilizadas para tratamientos: células madre alogénicas derivadas de un donante genéticamente diferente dentro de la misma especie, [16] [90] y células madre mesenquimales autólogas , derivadas del paciente antes de su uso en varios tratamientos. [20] Una tercera categoría, las células madre xenogénicas , o células madre derivadas de diferentes especies, se utilizan principalmente con fines de investigación, especialmente para tratamientos humanos. [28]
El hueso tiene un proceso de curación natural único y bien documentado que normalmente es suficiente para reparar fracturas y otras lesiones comunes. Las fracturas desalineadas debido a traumatismos graves, así como los tratamientos como las resecciones tumorales del cáncer de hueso, son propensos a una curación inadecuada si se dejan al proceso natural por sí solo. Los andamios compuestos de componentes naturales y artificiales se siembran con células madre mesenquimales y se colocan en el defecto. Dentro de las cuatro semanas posteriores a la colocación del andamio, el hueso recién formado comienza a integrarse con el hueso viejo y dentro de las 32 semanas, se logra la unión completa. [91] Se necesitan más estudios para caracterizar completamente el uso de terapias basadas en células para el tratamiento de fracturas óseas.
Las células madre se han utilizado para tratar enfermedades óseas degenerativas en perros. El tratamiento que normalmente se recomienda para los perros que padecen la enfermedad de Legg-Calvé-Perthes es extirpar la cabeza del fémur una vez que la degeneración ha avanzado. Recientemente, se han inyectado células madre mesenquimales directamente en la cabeza del fémur, con éxito no solo en la regeneración ósea, sino también en la reducción del dolor. [91]
Los tratamientos basados en células madre autólogas para lesiones de ligamentos , lesiones de tendones , osteoartritis , osteocondrosis y quistes óseos subcondrales han estado disponibles comercialmente para veterinarios en ejercicio para tratar caballos desde 2003 en los Estados Unidos y desde 2006 en el Reino Unido. Los tratamientos basados en células madre autólogas para lesiones de tendones, lesiones de ligamentos y osteoartritis en perros han estado disponibles para veterinarios en los Estados Unidos desde 2005. Más de 3000 caballos y perros de propiedad privada han sido tratados con células madre autólogas derivadas de tejido adiposo. La eficacia de estos tratamientos se ha demostrado en ensayos clínicos doble ciego para perros con osteoartritis de cadera y codo y caballos con daño en los tendones. [92] [93]
Los caballos de carreras son especialmente propensos a sufrir lesiones en tendones y ligamentos. Las terapias convencionales no consiguen que el caballo recupere su pleno potencial funcional. La curación natural, guiada por los tratamientos convencionales, conduce a la formación de tejido cicatricial fibroso que reduce la flexibilidad y el movimiento completo de las articulaciones. Los tratamientos tradicionales han impedido que un gran número de caballos vuelvan a la actividad completa y también tienen una alta incidencia de nuevas lesiones debido a la naturaleza rígida del tendón cicatrizado. La introducción de células madre derivadas de la médula ósea y del tejido adiposo, junto con un estímulo mecánico natural, promovió la regeneración del tejido del tendón. El movimiento natural promovió la alineación de las nuevas fibras y tendocitos con la alineación natural que se encuentra en los tendones no lesionados. El tratamiento con células madre no sólo permitió que más caballos volvieran a la actividad completa, sino que también redujo en gran medida la tasa de nuevas lesiones durante un período de tres años. [23]
El uso de células madre embrionarias también se ha aplicado a la reparación de tendones. Se ha demostrado que las células madre embrionarias tienen una mejor tasa de supervivencia en el tendón, así como una mejor capacidad de migración para alcanzar todas las áreas del tendón dañado. La calidad general de la reparación también fue mayor, con una mejor arquitectura del tendón y una mejor formación de colágeno. Tampoco se observó formación de tumores durante el período experimental de tres meses. Es necesario realizar estudios a largo plazo para examinar la eficacia a largo plazo y los riesgos asociados con el uso de células madre embrionarias. [23] Se han encontrado resultados similares en animales pequeños. [23]
La osteoartritis es la principal causa de dolor articular tanto en animales como en humanos. Los caballos y los perros son los más frecuentemente afectados por la artritis. La regeneración natural del cartílago es muy limitada. Todavía se están investigando diferentes tipos de células madre mesenquimales y otros aditivos para encontrar el mejor tipo de célula y método para el tratamiento a largo plazo. [23]
Las células mesenquimales derivadas de tejido adiposo son las más utilizadas actualmente para el tratamiento de la osteoartritis con células madre debido a que su obtención no es invasiva. Se trata de una técnica no invasiva desarrollada recientemente para facilitar su uso clínico. Los perros que recibieron este tratamiento mostraron una mayor flexibilidad en sus articulaciones y menos dolor. [94]
Las células madre se han utilizado con éxito para mejorar la cicatrización del corazón después de un infarto de miocardio en perros. Se extrajeron células madre derivadas de tejido adiposo y médula ósea y se las indujo a convertirse en células cardíacas antes de inyectarlas en el corazón. Se observó que el corazón presentaba una mejor contractilidad y una reducción de la zona dañada cuatro semanas después de la aplicación de las células madre. [95]
En 2007 se estaba llevando a cabo un ensayo con un parche hecho de una sustancia porosa sobre la que se "siembran" células madre para inducir la regeneración tisular en defectos cardíacos. El tejido se regeneró y el parche se incorporó bien al tejido cardíaco. Se cree que esto se debe, en parte, a una mejor angiogénesis y a una reducción de la inflamación. Aunque los cardiomiocitos se produjeron a partir de células madre mesenquimales , no parecían ser contráctiles. Otros tratamientos que inducían un destino cardíaco en las células antes del trasplante tuvieron mayor éxito en la creación de tejido cardíaco contráctil. [96]
Las investigaciones de 2018, como el proyecto de investigación europeo nTRACK, tienen como objetivo demostrar que las nanopartículas multimodales pueden rastrear estructural y funcionalmente las células madre en la terapia de regeneración muscular. La idea es etiquetar las células madre con nanopartículas de oro que estén completamente caracterizadas en cuanto a absorción, funcionalidad y seguridad. Las células madre etiquetadas se inyectarán en un músculo lesionado y se rastrearán mediante sistemas de imágenes. [97] Sin embargo, el sistema aún necesita demostrarse a escala de laboratorio.
Las lesiones de la médula espinal son uno de los traumatismos más comunes que se llevan a los hospitales veterinarios. [91] Las lesiones de la médula espinal se producen de dos maneras después del traumatismo: el daño mecánico primario y en procesos secundarios, como la inflamación y la formación de cicatrices, en los días posteriores al traumatismo. Estas células involucradas en la respuesta al daño secundario secretan factores que promueven la formación de cicatrices e inhiben la regeneración celular. Las células madre mesenquimales que son inducidas a un destino de célula neuronal se cargan en un andamio poroso y luego se implantan en el sitio de la lesión. Las células y el andamio secretan factores que contrarrestan los secretados por las células formadoras de cicatrices y promueven la regeneración neuronal. Ocho semanas después, los perros tratados con células madre mostraron una inmensa mejoría en comparación con los tratados con terapias convencionales. Los perros tratados con células madre pudieron ocasionalmente soportar su propio peso, lo que no se ha visto en perros sometidos a terapias convencionales. [98] [99] [100]
En un estudio para evaluar el tratamiento de la EM inducida experimentalmente en perros utilizando células madre derivadas de tejido adiposo no expandidas activadas por láser, los resultados mostraron una mejoría de los signos clínicos con el tiempo, confirmada por la resolución de las lesiones previas en la resonancia magnética. La migración positiva de las células inyectadas al sitio de la lesión, el aumento de la remielinización detectado por las proteínas básicas de mielina, la diferenciación positiva en oligodendrocitos positivos para Olig2, evitaron la formación de cicatrices gliales y restauraron la arquitectura axonal. [38]
También se están realizando ensayos clínicos con tratamientos para reparar y regenerar los nervios periféricos. Los nervios periféricos tienen más probabilidades de sufrir daños, pero los efectos del daño no son tan generalizados como los que se observan en las lesiones de la médula espinal. Actualmente se están realizando ensayos clínicos con tratamientos para reparar nervios dañados, con un éxito temprano. Se inyectaron células madre inducidas a un destino neuronal en un nervio dañado. En cuatro semanas, se observó la regeneración de las células madre previamente dañadas y haces nerviosos completamente formados. [21]
Las células madre también se encuentran en fase clínica para su uso en oftalmología. Las células madre hematopoyéticas se han utilizado para tratar úlceras corneales de diferente origen en varios caballos. Estas úlceras eran resistentes a los tratamientos convencionales disponibles, pero respondieron rápidamente de forma positiva al tratamiento con células madre. Las células madre también fueron capaces de restaurar la visión en un ojo de un caballo con desprendimiento de retina, lo que permitió al caballo volver a sus actividades diarias. [22]
Se están estudiando las células madre para su uso en iniciativas de conservación. Se han extraído células madre espermatogoniales de una rata y se han colocado en un ratón huésped, con lo que se han producido espermatozoides completamente maduros capaces de producir crías viables. Actualmente se están realizando investigaciones para encontrar huéspedes adecuados para la introducción de células madre espermatogoniales de donantes. Si esta se convierte en una opción viable para los conservacionistas, se pueden producir espermatozoides a partir de individuos de alta calidad genética que mueren antes de alcanzar la madurez sexual, preservando así una línea que de otro modo se perdería. [101]
A finales de los años 1990 y principios de los años 2000, hubo una ola inicial de empresas y clínicas que ofrecían terapias con células madre, aunque no fundamentaban sus afirmaciones sobre sus propiedades saludables ni contaban con la aprobación regulatoria. [102] En 2012, había surgido una segunda ola de empresas y clínicas, generalmente ubicadas en países en desarrollo donde la medicina está menos regulada y que ofrecían terapias con células madre en un modelo de turismo médico . [103] [104] Al igual que las empresas y clínicas de la primera ola, hicieron afirmaciones similares, fuertes, pero sin fundamento, principalmente por parte de clínicas en los Estados Unidos, México, Tailandia, India y Sudáfrica . [103] [104] En 2016, las investigaciones indicaron que solo en los EE. UU. había más de 550 clínicas de células madre que vendían terapias generalmente no probadas para una amplia gama de condiciones médicas en casi todos los estados del país, [105] alterando la dinámica del turismo de células madre . En 2018, la FDA envió una carta de advertencia a StemGenex Biologic Laboratories en San Diego, que comercializaba un servicio en el que tomaba grasa corporal de personas, la procesaba en mezclas que decían que contenían varias formas de células madre y se la administraba a la persona por inhalación, vía intravenosa o infusión en la médula espinal; la compañía dijo que el tratamiento era útil para muchas afecciones crónicas y potencialmente mortales. [106]
Una táctica de marketing habitual es el registro en ClinicalTrials.gov , la base de datos del gobierno estadounidense sobre ensayos clínicos. El registro de un estudio notifica a la agencia, pero no prueba que se haya realizado una revisión. El registro en la FDA tampoco prueba que se haya concedido la aprobación. [107]
Los costos de las terapias con células madre varían ampliamente según la clínica, la condición y el tipo de célula, pero lo más común es que oscile entre $10,000 y $20,000. [108] El seguro no cubre las inyecciones de células madre en las clínicas, por lo que los pacientes a menudo usan la recaudación de fondos en línea. [109] En 2018, la Comisión Federal de Comercio de los EE. UU. encontró centros de salud y un médico individual haciendo afirmaciones sin fundamento sobre terapias con células madre y obligó a reembolsos de unos $500,000. [110] La FDA presentó una demanda contra dos empresas de clínicas de células madre casi al mismo tiempo, buscando medidas cautelares permanentes contra su comercialización y uso de productos de células madre adiposas no aprobados. [111]
Aunque según el NIH no se han aprobado tratamientos con células madre para la COVID-19 , y la agencia recomienda no utilizar células madre madre para la enfermedad, [112] algunas clínicas de células madre comenzaron a comercializar células madre y exosomas no probados y no aprobados por la FDA para la COVID-19 en 2020. [113] La FDA tomó medidas rápidas enviando cartas a las empresas en cuestión. [114] [115] La FTC también advirtió a una empresa de células madre por marketing engañoso relacionado con la COVID-19. [116] [117]
[118]