La alfa-queratina , o α-queratina, es un tipo de queratina que se encuentra en los vertebrados mamíferos . Esta proteína es el componente principal de los pelos , cuernos , garras , uñas y la capa de la epidermis de la piel . La α-queratina es una proteína estructural fibrosa , lo que significa que está formada por aminoácidos que forman una estructura secundaria repetitiva. La estructura secundaria de la α-queratina es muy similar a la de una proteína α-hélice tradicional y forma una espiral enrollada . [1] Debido a su estructura firmemente enrollada, puede funcionar como uno de los materiales biológicos más fuertes y tiene varias funciones en los mamíferos, desde garras depredadoras hasta cabello para dar calor. La α-queratina se sintetiza a través de la biosíntesis de proteínas , utilizando la transcripción y la traducción , pero a medida que la célula madura y está llena de α-queratina, muere, creando una fuerte unidad no vascular de tejido queratinizado . [2]

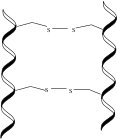
La α-queratina es una cadena polipeptídica , típicamente rica en alanina , leucina , arginina y cisteína , que forma una α-hélice dextrógira . [3] [4] Dos de estas cadenas polipeptídicas se retuercen entre sí para formar una estructura helicoidal levógira conocida como espiral en espiral . Estos dímeros espirales en espiral , de aproximadamente 45 nm de largo, están unidos entre sí con enlaces disulfuro , utilizando los numerosos aminoácidos de cisteína que se encuentran en las α-queratinas. [2] Luego, los dímeros se alinean, sus extremos se unen con los extremos de otros dímeros, y dos de estas nuevas cadenas se unen longitudinalmente, todas a través de enlaces disulfuro, para formar un protofilamento. [5] Dos protofilamentos se agregan para formar una protofibrilla, y cuatro protofibrillas se polimerizan para formar el filamento intermedio (IF). El IF es la subunidad básica de las α-queratinas. Estos IF pueden condensarse en una formación de superenrollamiento de aproximadamente 7 nm de diámetro y pueden ser de tipo I , ácidos, o de tipo II , básicos. Los IF finalmente se incrustan en una matriz de queratina que es rica en residuos de cisteína o glicina , tirosina y fenilalanina . Los diferentes tipos, alineaciones y matrices de estos IF explican la gran variación en las estructuras de α-queratina encontradas en los mamíferos. [6]
La síntesis de α-queratina comienza cerca de las adherencias focales en la membrana celular . Allí, los precursores de filamentos de queratina pasan por un proceso conocido como nucleación , donde los precursores de queratina de dímeros y filamentos se alargan, se fusionan y se agrupan. [2] Mientras se produce esta síntesis, los precursores de filamentos de queratina son transportados por fibras de actina en la célula hacia el núcleo . Allí, los filamentos intermedios de alfa-queratina se recogerán y formarán redes de estructura dictadas por el uso de la célula de queratina a medida que el núcleo se degrada simultáneamente. [7] Sin embargo, si es necesario, en lugar de seguir creciendo, el complejo de queratina se desarmará en precursores de queratina no filamentosos que pueden difundirse por todo el citoplasma celular . Estos filamentos de queratina podrán usarse en futuras síntesis de queratina, ya sea para reorganizar la estructura final o crear un complejo de queratina diferente. Cuando la célula se ha llenado con la queratina correcta y se ha estructurado correctamente, sufre una estabilización de la queratina y muere, una forma de muerte celular programada . Esto da como resultado una célula de queratina no vascularizada y completamente madura. [8] Estas células de queratina alfa completamente maduras, o cornificadas , son los componentes principales del cabello, la capa externa de las uñas y los cuernos, y la capa de la epidermis de la piel. [9]
La propiedad de mayor importancia biológica de la alfa-queratina es su estabilidad estructural . Cuando se exponen a estrés mecánico , las estructuras de α-queratina pueden conservar su forma y, por lo tanto, pueden proteger lo que rodean. [10] Bajo alta tensión, la alfa-queratina puede incluso transformarse en beta-queratina , una formación de queratina más fuerte que tiene una estructura secundaria de láminas beta-plegadas . [11] Los tejidos de alfa-queratina también muestran signos de viscoelasticidad , lo que les permite estirarse y absorber el impacto hasta cierto punto, aunque no son impermeables a la fractura . La resistencia de la alfa-queratina también se ve afectada por el contenido de agua en la matriz del filamento intermedio; un mayor contenido de agua disminuye la resistencia y la rigidez de la célula de queratina debido a su efecto sobre los diversos enlaces de hidrógeno en la red de alfa-queratina. [2]
Las proteínas alfa-queratinas pueden ser de dos tipos: tipo I o tipo II . Hay 54 genes de queratina en los seres humanos, 28 de los cuales codifican para el tipo I y 26 para el tipo II. [12] Las proteínas de tipo I son ácidas, lo que significa que contienen más aminoácidos ácidos, como el ácido aspártico , mientras que las proteínas de tipo II son básicas, lo que significa que contienen más aminoácidos básicos, como la lisina . [13] Esta diferenciación es especialmente importante en las alfa-queratinas porque en la síntesis de su subunidad dímera, la coiled coil , una proteína coil debe ser de tipo I, mientras que la otra debe ser de tipo II. [2] Incluso dentro de los tipos I y II, hay queratinas ácidas y básicas que son particularmente complementarias dentro de cada organismo. Por ejemplo, en la piel humana, K5 , una alfa-queratina de tipo II, se empareja principalmente con K14 , una alfa-queratina de tipo I, para formar el complejo alfa-queratina de la capa de células de la epidermis en la piel. [14]
Las alfa-queratinas duras, como las que se encuentran en las uñas, tienen un mayor contenido de cisteína en su estructura primaria . Esto provoca un aumento de los enlaces disulfuro que son capaces de estabilizar la estructura de la queratina, lo que le permite resistir un mayor nivel de fuerza antes de fracturarse. Por otro lado, las alfa-queratinas blandas, como las que se encuentran en la piel, contienen una cantidad comparativamente menor de enlaces disulfuro, lo que hace que su estructura sea más flexible. [1]
{{cite book}}: CS1 maint: varios nombres: lista de autores ( enlace )