Los compuestos aromáticos o arenos generalmente se refieren a compuestos orgánicos "con una química tipificada por el benceno " y "cíclicamente conjugados". [1] La palabra "aromático" se origina en la antigua agrupación de moléculas basadas en el olor, antes de que se comprendieran sus propiedades químicas generales. La definición actual de compuestos aromáticos no tiene ninguna relación con su olor. Los compuestos aromáticos ahora se definen como compuestos cíclicos que satisfacen la regla de Hückel . Los compuestos aromáticos tienen las siguientes propiedades generales:
Los arenos normalmente se dividen en dos categorías: benzoides, que contienen un derivado de benceno y siguen el modelo del anillo de benceno, y no benzoides que contienen otros derivados cíclicos aromáticos. Los compuestos aromáticos se utilizan comúnmente en la síntesis orgánica y participan en muchos tipos de reacciones, tanto después de adiciones como eliminaciones, así como de saturación y desaromatización.
Los heteroarenos son compuestos aromáticos, donde al menos un grupo metino o vinileno (-C= o -CH=CH-) está reemplazado por un heteroátomo : oxígeno , nitrógeno o azufre . [3] Ejemplos de compuestos distintos del benceno con propiedades aromáticas son el furano , un compuesto heterocíclico con un anillo de cinco miembros que incluye un solo átomo de oxígeno, y la piridina , un compuesto heterocíclico con un anillo de seis miembros que contiene un átomo de nitrógeno. Los hidrocarburos sin anillo aromático se denominan alifáticos . Aproximadamente la mitad de los compuestos conocidos en el año 2000 se describen como aromáticos hasta cierto punto. [4]



Los compuestos aromáticos están omnipresentes en la naturaleza y la industria. Los hidrocarburos aromáticos industriales clave son el benceno, el tolueno y el xileno, llamado BTX. Muchas biomoléculas tienen grupos fenilo entre ellos los llamados aminoácidos aromáticos .


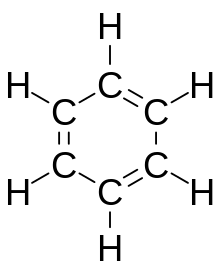
El benceno , C 6 H 6 , es el hidrocarburo aromático menos complejo, y fue el primero en definirse como tal. [6] Su naturaleza vinculante fue reconocida por primera vez de forma independiente por Joseph Loschmidt y August Kekulé en el siglo XIX. [6] Cada átomo de carbono en el ciclo hexagonal tiene cuatro electrones para compartir. Un electrón forma un enlace sigma con el átomo de hidrógeno y el otro se utiliza para unirse covalentemente a cada uno de los dos carbonos vecinos. Esto deja seis electrones, compartidos equitativamente alrededor del anillo en orbitales moleculares pi deslocalizados del tamaño del propio anillo. [5] Esto representa la naturaleza equivalente de los seis enlaces carbono-carbono, todos de orden de enlace 1,5. Esta equivalencia también puede explicarse por formas de resonancia . [5] Los electrones se visualizan flotando por encima y por debajo del anillo, y los campos electromagnéticos que generan actúan para mantener el anillo plano. [5]
El símbolo circular de la aromaticidad fue introducido por Sir Robert Robinson y su alumno James Armit en 1925 y popularizado a partir de 1959 por el libro de texto de Morrison & Boyd sobre química orgánica. [7] El uso adecuado del símbolo es objeto de debate: algunas publicaciones lo utilizan para cualquier sistema π cíclico, mientras que otras lo utilizan sólo para aquellos sistemas π que obedecen a la regla de Hückel . Algunos argumentan que, para mantenerse en línea con la propuesta original de Robinson, el uso del símbolo del círculo debería limitarse a sistemas monocíclicos de 6 electrones π. [8] De esta manera, el símbolo del círculo para un enlace de seis centros y seis electrones se puede comparar con el símbolo Y para un enlace de tres centros y dos electrones . [8]

Los derivados de benceno tienen de uno a seis sustituyentes unidos al núcleo central de benceno. Ejemplos de compuestos de benceno con un solo sustituyente son el fenol , que lleva un grupo hidroxilo , y el tolueno, con un grupo metilo . Cuando hay más de un sustituyente presente en el anillo, su relación espacial se vuelve importante para lo cual se idean los patrones de sustitución de areno orto , meta y para . [9] Cuando se reacciona para formar derivados de benceno más complejos, los sustituyentes en un anillo de benceno pueden describirse como activados o desactivados , que son donadores y atractores de electrones, respectivamente. [9] Los activadores se conocen como orto-paradirectores y los desactivadores se conocen como metadirectores. [9] Al reaccionar, se agregarán sustituyentes en las posiciones orto, para o meta, dependiendo de la directividad de los sustituyentes actuales para formar derivados de benceno más complejos, a menudo con varios isómeros. El flujo de electrones que conduce a la rearomatización es clave para garantizar la estabilidad de dichos productos. [9]
Por ejemplo, existen tres isómeros para el cresol porque el grupo metilo y el grupo hidroxilo (ambos ortoparadirectores) pueden colocarse uno al lado del otro ( orto ), una posición separada entre sí ( meta ), o dos posiciones separadas entre sí. ( párrafo ). [10] Dado que tanto el grupo metilo como el hidroxilo son directores orto-para, los isómeros orto y para suelen ser los preferidos. [10] El xilenol tiene dos grupos metilo además del grupo hidroxilo y, para esta estructura, existen 6 isómeros. [ cita necesaria ]
Los anillos de areno pueden estabilizar las cargas, como se ve, por ejemplo, en el fenol (C 6 H 5 –OH), que es ácido en el hidroxilo (OH), ya que la carga en el oxígeno (alcóxido –O − ) se deslocaliza parcialmente en el benceno. anillo.
Aunque los arenos bencílicos son comunes, los compuestos no bencílicos también son sumamente importantes. Cualquier compuesto que contenga una porción cíclica que se ajuste a la regla de Hückel y no sea un derivado del benceno puede considerarse un compuesto aromático no bencílico. [5]
De los anulenos más grandes que el benceno, [12] anuleno y [14] anuleno son compuestos débilmente aromáticos y [18] anuleno, ciclooctadecanonaeno , es aromático, aunque la tensión dentro de la estructura provoca una ligera desviación de la estructura precisamente plana necesaria para la categorización aromática. [11] Otro ejemplo de areno monocíclico no bencílico es el ciclopropenilo (catión ciclopropenio), que satisface la regla de Hückel con un n igual a 0. [12] Tenga en cuenta que sólo la forma catiónica de este propenilo cíclico es aromática, dado que la neutralidad en este compuesto violaría la regla del octeto o la regla de Hückel . [12]
Otros arenos monocíclicos no bencílicos incluyen los heteroarenos antes mencionados que pueden reemplazar átomos de carbono con otros heteroátomos como N, O o S. [5] Ejemplos comunes de estos son el pirrol de seis miembros y la piridina de cinco miembros , los cuales tienen una nitrógeno sustituido [13]
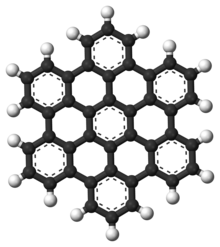
Los hidrocarburos aromáticos policíclicos , también conocidos como compuestos aromáticos polinucleares (HAP), son hidrocarburos aromáticos que consisten en anillos aromáticos fusionados y no contienen heteroátomos ni llevan sustituyentes . [14] La naftaleno es el ejemplo más simple de HAP. Los HAP se encuentran en depósitos de petróleo , carbón y alquitrán , y se producen como subproductos de la quema de combustible (ya sea fósil o biomasa). [15] Como contaminantes, son motivo de preocupación porque algunos compuestos han sido identificados como cancerígenos , mutagénicos y teratogénicos . [16] [17] [18] [19] Los HAP también se encuentran en los alimentos cocinados. [15] Los estudios han demostrado que se encuentran altos niveles de HAP, por ejemplo, en la carne cocinada a altas temperaturas, como la parrilla o la barbacoa, y en el pescado ahumado. [15] [16] También son una buena molécula candidata para actuar como base para las primeras formas de vida . [20] En el grafeno, el motivo PAH se extiende a grandes láminas 2D. [21]
Los sistemas de anillos aromáticos participan en muchas reacciones orgánicas.
En la sustitución aromática , un sustituyente del anillo areno, normalmente hidrógeno, se reemplaza por otro reactivo. [5] Los dos tipos principales son la sustitución aromática electrófila , cuando el reactivo activo es un electrófilo, y la sustitución aromática nucleófila , cuando el reactivo es un nucleófilo. En la sustitución aromática radical-nucleofílica , el reactivo activo es un radical . [22] [23]
Un ejemplo de sustitución aromática electrófila es la nitración del ácido salicílico , donde se añade un grupo nitro al sustituyente hidróxido:
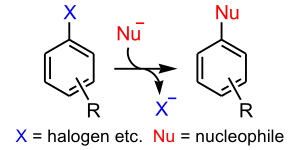
La sustitución aromática nucleófila implica el desplazamiento de un grupo saliente , como un haluro , en un anillo aromático . Los anillos aromáticos suelen ser nucleofílicos, pero en presencia de grupos aceptores de electrones los compuestos aromáticos sufren sustitución nucleófila. Mecánicamente, esta reacción difiere de una reacción S N 2 común porque ocurre en un átomo de carbono trigonal ( hibridación sp 2 ). [24]
La hidrogenación de arenos crea anillos saturados. El compuesto 1-naftol se reduce completamente a una mezcla de isómeros de decalin -ol . [25]
El compuesto resorcinol , hidrogenado con níquel Raney en presencia de hidróxido de sodio acuoso , forma un enolato que se alquila con yoduro de metilo a 2-metil-1,3-ciclohexandiona: [26]
En las reacciones de desaromatización se pierde la aromaticidad del reactivo. En este sentido, la desaromatización está relacionada con la hidrogenación. Un enfoque clásico es la reducción de Birch . La metodología se utiliza en síntesis. [27]
