Los genes Hox , un subconjunto de genes homeobox , son un grupo de genes relacionados que especifican regiones del plan corporal de un embrión a lo largo del eje cabeza-cola de los animales. Las proteínas Hox codifican y especifican las características de "posición", asegurando que se formen las estructuras correctas en los lugares correctos del cuerpo. Por ejemplo, los genes Hox en los insectos especifican qué apéndices se forman en un segmento (por ejemplo, patas, antenas y alas en las moscas de la fruta), y los genes Hox en los vertebrados especifican los tipos y la forma de las vértebras que se formarán. En animales segmentados, las proteínas Hox confieren identidad segmentaria o posicional, pero no forman los segmentos en sí.
Los estudios sobre los genes Hox en larvas ciliadas han demostrado que sólo se expresan en futuros tejidos adultos. En las larvas con metamorfosis gradual los genes Hox se activan en tejidos del cuerpo larvario, generalmente en la región del tronco, que se mantendrán durante la metamorfosis. En larvas con metamorfosis completa, los genes Hox se expresan principalmente en rudimentos juveniles y están ausentes en los tejidos larvarios transitorios. Las larvas de la especie hemicordada Schizocardium californicum y la larva de pilidium de Nemertea no expresan genes Hox. [1] [2]
Se puede hacer una analogía con los genes Hox con el papel del director de una obra de teatro que determina qué escena deben representar los actores a continuación. Si el director de la obra presenta las escenas en el orden incorrecto, la obra en general se presentará en el orden incorrecto. De manera similar, las mutaciones en los genes Hox pueden provocar que partes del cuerpo y extremidades se encuentren en el lugar equivocado del cuerpo. Al igual que un director de obra, los genes Hox no actúan en la obra ni participan por sí mismos en la formación de las extremidades.
El producto proteico de cada gen Hox es un factor de transcripción . Cada gen Hox contiene una secuencia de ADN bien conservada conocida como homeobox, de la cual el término "Hox" era originalmente una contracción. Sin embargo, en el uso actual, el término Hox ya no es equivalente a homeobox, porque los genes Hox no son los únicos genes que poseen una secuencia homeobox; por ejemplo, los humanos tienen más de 200 genes homeobox, de los cuales 39 son genes Hox. [3] [4] Los genes Hox son, por tanto, un subconjunto de los genes del factor de transcripción homeobox. En muchos animales, la organización de los genes Hox en el cromosoma es la misma que el orden de su expresión a lo largo del eje anteroposterior del animal en desarrollo y, por lo tanto, se dice que muestran colinealidad. [5] [6] La producción de productos del gen Hox en una ubicación incorrecta del cuerpo se asocia con metaplasia y predispone a enfermedades oncológicas; por ejemplo, el esófago de Barrett es el resultado de una codificación Hox alterada y es un precursor del cáncer de esófago . [7]
Los productos de los genes Hox son proteínas Hox. Las proteínas Hox son un subconjunto de factores de transcripción, que son proteínas que son capaces de unirse a secuencias de nucleótidos específicas en el ADN llamadas potenciadores a través de las cuales activan o reprimen cientos de otros genes. La misma proteína Hox puede actuar como represor en un gen y activador en otro. La capacidad de las proteínas Hox para unirse al ADN la confiere una parte de la proteína denominada homeodominio . El homeodominio es un dominio de unión al ADN de 60 aminoácidos de longitud (codificado por su correspondiente secuencia de ADN de 180 pares de bases , la homeocaja). Esta secuencia de aminoácidos se pliega en un motivo de "hélice-giro-hélice" (es decir, pliegue de homeodominio ) que está estabilizado por una tercera hélice. La cadena polipeptídica de consenso se muestra a continuación: [8] Las proteínas Hox a menudo actúan en asociación con cofactores, como las proteínas PBC y Meis codificadas por tipos muy diferentes de genes homeobox. [9]
Hélice 1 Hélice 2 Hélice 3/4 ______________ __________ _________________RRRKRTAYTRYQLLELEKEFLFNRYLTRRRRIELAHSLNLTERHIKIWFQNRRMKWKKEN....|....|....|....|....|....|....|....|....|....| ....|....| 10 20 30 40 50 60

Los genes homeobox y, por tanto, el motivo proteico del homeodominio, se encuentran en la mayoría de los eucariotas . Los genes Hox, al ser un subconjunto de genes homeobox, surgieron más recientemente en la evolución dentro del reino animal o Metazoa . Dentro del reino animal, los genes Hox están presentes en los bilateria [10] (animales con un eje claro de la cabeza a la cola) y también se han encontrado en cnidarios como las anémonas de mar . [11] Esto implica que los genes Hox surgieron hace más de 550 millones de años. En la bilateria, los genes Hox suelen estar dispuestos en grupos de genes, aunque hay muchas excepciones en las que los genes han sido separados por reordenamientos cromosómicos. [12] La comparación de secuencias de homeodominio entre proteínas Hox a menudo revela una mayor similitud entre especies que dentro de una especie; Esta observación llevó a la conclusión de que los grupos de genes Hox evolucionaron temprano en la evolución animal a partir de un solo gen Hox mediante duplicación en tándem y divergencia posterior, y que un grupo de genes Hox prototípico que contenía al menos siete genes Hox diferentes estaba presente en el ancestro común de todos los bilaterales. animales. [10] [13]
En la mayoría de los animales bilaterales , los genes Hox se expresan en dominios escalonados a lo largo del eje de la cabeza a la cola del embrión, lo que sugiere que su papel en la especificación de la posición es una característica antigua compartida. [14] La conservación funcional de las proteínas Hox puede demostrarse por el hecho de que una mosca puede funcionar en gran medida con una proteína Hox de pollo en lugar de la suya propia. [15] Entonces, a pesar de tener un último ancestro común que vivió hace más de 550 millones de años, [16] la versión del pollo y la mosca del mismo gen Hox son lo suficientemente similares como para apuntar a los mismos genes posteriores en las moscas.

Drosophila melanogaster es un modelo importante para comprender la generación y evolución del plan corporal. Los principios generales de la función y la lógica del gen Hox dilucidados en las moscas se aplicarán a todos los organismos bilaterales, incluidos los humanos. Drosophila , como todos los insectos, tiene ocho genes Hox. Estos se agrupan en dos complejos, ambos ubicados en el cromosoma 3. El complejo Antennapedia (que no debe confundirse con el gen Antp ) consta de cinco genes: labial ( lab ), proboscipedia ( pb ), deformado ( Dfd ), sexo. peines reducidos ( Scr ), y Antennapedia ( Antp ). El complejo Bithorax, que lleva el nombre del gen Ultrabithorax, consta de los tres genes restantes: Ultrabithorax ( Ubx ), abdominal-A ( abd-A ) y abdominal-B ( abd-B ).
El gen de laboratorio es el gen expresado más anteriormente. Se expresa en la cabeza, principalmente en el segmento intercalar (un segmento sin apéndices entre la antena y la mandíbula), y también en el intestino medio. La pérdida de la función de laboratorio provoca que el embrión de Drosophila no internalice las estructuras de la boca y la cabeza que inicialmente se desarrollan en el exterior de su cuerpo (un proceso llamado involución de la cabeza). La falta de involución de la cabeza altera o elimina las glándulas salivales y la faringe. Inicialmente, el gen del laboratorio recibió ese nombre porque alteraba el apéndice labial; sin embargo, el gen lab no se expresa en el segmento labial y el fenotipo del apéndice labial probablemente sea resultado de la amplia desorganización resultante de la falla de la involución de la cabeza. [17]
El gen pb es responsable de la formación de los palpos labiales y maxilares. Alguna evidencia muestra que pb interactúa con Scr . [18]
El gen Dfd es responsable de la formación de los segmentos maxilar y mandibular en la cabeza larvaria. [19] Los fenotipos mutantes de Dfd son similares a los de labial. La pérdida de función de Dfd en el embrión da como resultado una falla en la involución de la cabeza (ver gen labial), con una pérdida de las estructuras de la cabeza larvaria. Las mutaciones en el adulto implican eliminaciones de partes de la cabeza o transformaciones de la cabeza a una identidad torácica. [17]
El gen Scr es responsable del desarrollo cefálico y torácico en embriones y adultos de Drosophila . [20]
El segundo segmento torácico, o T2, desarrolla un par de patas y un par de alas. El gen Antp especifica esta identidad al promover la formación de patas y permitir (pero no activar directamente) la formación de alas. Una mutación Antp dominante , causada por una inversión cromosómica , hace que Antp se exprese en el disco imaginal antenal, de modo que, en lugar de formar una antena, el disco forma una pata, lo que da como resultado una pata que sale de la cabeza de la mosca. [ cita necesaria ]

El tercer segmento torácico, o T3, tiene un par de patas y un par de halterios (alas muy reducidas que sirven para mantener el equilibrio durante el vuelo). Ubx modela T3 en gran medida reprimiendo genes implicados en la formación de alas. La lámina del ala se compone de dos capas de células que se adhieren firmemente entre sí y reciben nutrientes de varias venas del ala. Uno de los muchos genes que reprime Ubx es el ampollado, que activa las proteínas implicadas en la adhesión entre células, y el spalt, que modela la ubicación de las venas de las alas. En los mutantes con pérdida de función de Ubx , Ubx ya no reprime los genes de las alas y los halterios se desarrollan como un segundo par de alas, lo que da como resultado las famosas moscas de cuatro alas. Cuando Ubx se expresa mal en el segundo segmento torácico, como ocurre en las moscas con la mutación potenciadora "Cbx", reprime los genes de las alas y las alas se desarrollan como halterios, lo que da como resultado una mosca de cuatro cabestros. [21]
En Drosophila , abd-A se expresa a lo largo de la mayor parte del abdomen, desde los segmentos abdominales 1 (A1) hasta A8. La expresión de abd-A es necesaria para especificar la identidad de la mayoría de los segmentos abdominales. Una función importante de abd-A en los insectos es reprimir la formación de extremidades. En los mutantes con pérdida de función abd-A , los segmentos abdominales A2 a A8 se transforman en una identidad más parecida a A1. Cuando abd-A se expresa ectópicamente en todo el embrión, todos los segmentos anteriores de A4 se transforman en una identidad abdominal similar a A4. [17] El gen abd-A también afecta el patrón de generación de cutícula en el ectodermo y el patrón de generación de músculo en el mesodermo . [18]
El gen abd-B se transcribe en dos formas diferentes, una proteína reguladora y una proteína morfogénica. El abd-B regulador suprime las estructuras epidérmicas ventrales embrionarias en los segmentos octavo y noveno del abdomen de Drosophila . Tanto la proteína reguladora como la proteína morfogénica participan en el desarrollo del segmento de la cola. [18]
Generalmente también se supone que las proteínas con un alto grado de similitud de secuencia exhiben un alto grado de similitud funcional, es decir, se supone que las proteínas Hox con homeodominios idénticos tienen propiedades de unión al ADN idénticas (a menos que se sepa que secuencias adicionales influyen en la unión al ADN). Para identificar el conjunto de proteínas entre dos especies diferentes que tienen más probabilidades de tener una función más similar, se utilizan esquemas de clasificación. Para las proteínas Hox, existen tres esquemas de clasificación diferentes: basado en inferencia filogenética, basado en sintenia y basado en similitud de secuencia. [22] Los tres esquemas de clasificación proporcionan información contradictoria para las proteínas Hox expresadas en el medio del eje del cuerpo ( Hox6-8 y Antp, Ubx y abd-A ). Un enfoque combinado utilizó información basada en inferencias filogenéticas de las diferentes especies y trazó los tipos de secuencias de proteínas en el árbol filogenético de las especies. El enfoque identificó las proteínas que mejor representan formas ancestrales ( Hox7 y Antp ) y las proteínas que representan versiones nuevas derivadas (o se perdieron en un ancestro y ahora faltan en numerosas especies). [23]
Los genes Hox actúan en muchos niveles dentro de las jerarquías genéticas del desarrollo: en el nivel "ejecutivo" regulan genes que a su vez regulan grandes redes de otros genes (como la vía genética que forma un apéndice). También regulan directamente los llamados genes realizadores o genes efectores que actúan en la base de dichas jerarquías para formar en última instancia los tejidos, estructuras y órganos de cada segmento. La segmentación implica procesos como la morfogénesis (diferenciación de células precursoras en sus células terminales especializadas), la estrecha asociación de grupos de células con destinos similares, la escultura de estructuras y límites de segmentos mediante la muerte celular programada y el movimiento de las células desde donde se originan. nacen hasta donde finalmente funcionarán, por lo que no es sorprendente que los genes diana de los genes Hox promuevan la división celular, la adhesión celular, la apoptosis y la migración celular. [5]
La secuencia de ADN unida por la proteína del homeodominio contiene la secuencia de nucleótidos TAAT, siendo la T 5' terminal la más importante para la unión. [28] Esta secuencia se conserva en casi todos los sitios reconocidos por los homeodominios y probablemente distingue tales ubicaciones como sitios de unión al ADN. Los pares de bases que siguen a esta secuencia inicial se utilizan para distinguir entre proteínas de homeodominio, todas las cuales tienen sitios de reconocimiento similares. Por ejemplo, el nucleótido que sigue a la secuencia TAAT es reconocido por el aminoácido en la posición 9 de la proteína del homeodominio. En la proteína materna Bicoide, esta posición la ocupa la lisina , que reconoce y se une al nucleótido guanina . En Antennapedia, esta posición la ocupa la glutamina , que reconoce y se une a la adenina . Si la lisina de Bicoid se reemplaza por glutamina, la proteína resultante reconocerá los sitios potenciadores de unión de Antennapedia. [29] [30]
Sin embargo, todos los factores de transcripción que contienen homeodominios se unen esencialmente a la misma secuencia de ADN. La secuencia unida por el homeodominio de una proteína Hox tiene sólo seis nucleótidos de longitud, y una secuencia tan corta se encontraría al azar muchas veces en todo el genoma, mucho más que el número de sitios funcionales reales. Especialmente para las proteínas Hox, que producen cambios tan dramáticos en la morfología cuando se expresan mal, esto plantea la pregunta de cómo cada factor de transcripción puede producir resultados tan específicos y diferentes si todos se unen a la misma secuencia. Un mecanismo que introduce una mayor especificidad de secuencia de ADN para las proteínas Hox es la unión de cofactores proteicos. Dos de estos cofactores Hox son Extradenticle (Exd) y Homothorax (Hth). Exd y Hth se unen a las proteínas Hox y parecen inducir cambios conformacionales en la proteína Hox que aumentan su especificidad. [31]
Así como los genes Hox regulan los genes realizadores, a su vez están regulados por otros genes. En Drosophila y algunos insectos (pero no en la mayoría de los animales), los genes Hox están regulados por genes gap y genes de regla de par , que a su vez están regulados por ARNm suministrado por la madre . Esto da como resultado una cascada de factores de transcripción: los factores maternos activan genes de regla de par o brecha; los genes gap y de regla de pares activan los genes Hox; luego, finalmente, los genes Hox activan los genes realizadores que hacen que los segmentos del embrión en desarrollo se diferencien.
La regulación se logra mediante gradientes de concentración de proteínas, llamados campos morfogénicos . Por ejemplo, concentraciones altas de una proteína materna y concentraciones bajas de otras activarán un conjunto específico de genes de regla de par o brecha. En las moscas, la raya 2 en el embrión es activada por las proteínas maternas Bicoid y Hunchback, pero reprimida por las proteínas gap Giant y Kruppel. Por lo tanto, la franja 2 solo se formará donde estén Bicoid y Hunchback, pero no donde estén Giant y Kruppel. [32]
Se ha demostrado que las hebras de microARN ubicadas en grupos de Hox inhiben más genes hox anteriores ("fenómeno de prevalencia posterior"), posiblemente para afinar mejor su patrón de expresión. [33]
Se ha demostrado que el ARN no codificante (ARNnc) es abundante en los grupos Hox. En los seres humanos, puede haber 231 ncRNA. Uno de ellos, HOTAIR , silencia en trans (se transcribe del grupo HOXC e inhibe los genes HOXD tardíos) uniéndose a proteínas del grupo Polycomb (PRC2). [34]
La estructura de la cromatina es esencial para la transcripción, pero también requiere que el grupo salga del territorio cromosómico . [35]
En animales superiores, incluidos los humanos, el ácido retinoico regula la expresión diferencial de los genes Hox a lo largo del eje anteroposterior. [36] Los genes en los extremos 3' de los grupos Hox son inducidos por el ácido retinoico, lo que da como resultado dominios de expresión que se extienden más anteriormente en el cuerpo en comparación con los genes 5' Hox que no son inducidos por el ácido retinoico, lo que da como resultado dominios de expresión que permanecen más posteriores.
La PCR cuantitativa ha mostrado varias tendencias con respecto a la colinealidad: el sistema está en equilibrio y el número total de transcripciones depende del número de genes presentes según una relación lineal. [37]
En algunos organismos, especialmente en los vertebrados, los distintos genes Hox se encuentran muy cerca unos de otros en el cromosoma en grupos o clusters. El orden de los genes en el cromosoma es el mismo que la expresión de los genes en el embrión en desarrollo, expresándose el primer gen en el extremo anterior del organismo en desarrollo. La razón de esta colinealidad aún no se comprende completamente, pero podría estar relacionada con la activación de los genes Hox en una secuencia temporal mediante el descompresión gradual de la cromatina a lo largo de un grupo de genes.
Los genes Hox reciben su nombre de los fenotipos homeóticos que resultan cuando se altera su función, en los que un segmento se desarrolla con la identidad de otro (por ejemplo, patas donde deberían estar las antenas). A los genes Hox en diferentes filos se les han dado nombres diferentes, lo que ha generado confusión sobre la nomenclatura. El complemento de genes Hox en Drosophila se compone de dos grupos, el complejo Antennapedia y el complejo Bithorax, que en conjunto se denominaron históricamente HOM-C (por complejo homeótico). Aunque históricamente los genes HOM-C se han referido a homólogos de Drosophila , mientras que los genes Hox se referían a homólogos de vertebrados, esta distinción ya no se hace, y tanto los genes HOM-C como Hox se denominan genes Hox. [ cita necesaria ]
Los ratones y los humanos tienen 39 genes Hox en cuatro grupos: [38] [39]
Los antepasados de los vertebrados tenían un solo grupo de genes Hox, [40] [41] [ cita necesaria ] que se duplicó (dos veces) al principio de la evolución de los vertebrados mediante duplicaciones del genoma completo para dar cuatro grupos de genes Hox: Hoxa, Hoxb, Hoxc y Hoxd. Actualmente no está claro si estas duplicaciones ocurrieron antes o después de la divergencia de las lampreas y los mixinos de otros vertebrados. [42] La mayoría de los tetrápodos tienen cuatro grupos de genes HOX, mientras que la mayoría de los peces teleósteos , incluidos el pez cebra y el medaka , tienen siete u ocho grupos de genes Hox debido a una duplicación adicional del genoma que ocurrió en su historia evolutiva. [43] [38] En el pez cebra, uno de los ocho grupos de genes Hox (un grupo Hoxd) ha perdido todos los genes codificadores de proteínas, y solo un gen de microARN marca la ubicación del grupo original. [44] En algunos peces teleósteos, como el salmón , se produjo una duplicación del genoma aún más reciente, duplicando los siete u ocho grupos de genes Hox para dar al menos 13 grupos [45] Otro teleósteo, el pez mariposa de agua dulce , ha experimentado en cambio una pérdida significativa. en grupos de genes HOX, con solo 5 grupos presentes. [46]
Los cuerpos de los vertebrados no están segmentados de la misma forma que los insectos; En promedio, son mucho más complejos, lo que lleva a una mayor infraestructura en su estructura corporal en comparación con los insectos. Los genes HOX controlan la regulación y el desarrollo de muchas estructuras clave del cuerpo, como los somitas , que forman las vértebras y las costillas, la dermis de la piel dorsal, los músculos esqueléticos de la espalda y los músculos esqueléticos de la pared corporal y las extremidades. . Los genes HOX ayudan a diferenciar las células somitas en identidades más específicas y las dirigen a desarrollarse de manera diferente dependiendo de dónde se encuentren en el cuerpo. [47] Una gran diferencia entre vertebrados e invertebrados es la ubicación y estratificación de los genes HOX. Los mecanismos fundamentales de desarrollo están fuertemente conservados entre los vertebrados, desde peces hasta mamíferos.
Debido al hecho de que los genes HOX están tan conservados, la mayoría de las investigaciones se han realizado en organismos modelo mucho más simples, como los ratones. Una de las principales diferencias que se notó al comparar ratones y drosophila , en particular, tiene que ver con la ubicación y la estratificación de los genes HOX dentro del genoma . Los vertebrados tienen genes HOX que son homólogos a los de la mosca, ya que es uno de los genes mejor conservados , pero la ubicación es diferente. Por ejemplo, hay más genes HOX en el lado 5' del segmento del ratón en comparación con los invertebrados. [48] Estos genes corresponden a la expresión en la cola, lo que tendría sentido ya que las moscas no tendrían nada similar a la cola que tienen todos los vertebrados. Además, en la mayoría de los vertebrados hay 39 miembros segregados en cuatro conjuntos de genes separados y estrechamente agrupados (A-D) en cuatro cromosomas separados , mientras que hay ocho genes HOX en total para Drosophila. [49] Los grupos son mucho más redundantes y es menos probable que generen mutaciones . En las moscas se puede mutar un gen, dando como resultado un halterio , algo fundamental para que puedan volar, transformándose en un ala, o una antena convirtiéndose en pata; en el ratón, se deben eliminar simultáneamente de dos a cuatro genes para obtener una transformación completa similar. Algunos investigadores creen que, debido a la redundancia del plan de grupos HOX de vertebrados y más restringido en comparación con los grupos HOX de invertebrados, la capacidad de evolución de los grupos HOX de vertebrados es, por alguna razón estructural o funcional, mucho menor que la de sus homólogos de invertebrados. [50] Esta rápida evolución se debe en parte a que los invertebrados experimentaron episodios mucho más dramáticos de radiación adaptativa y mutaciones. Más de 20 clados principales de invertebrados difieren tan radicalmente en la organización corporal, en parte debido a una mayor tasa de mutación, que pasaron a clasificarse formalmente como filos diferentes . [51] Es necesario eliminar todos los genes parálogos para que se produzcan cambios fenotípicos en su mayor parte. Esta es también una de las razones por las que las mutaciones homeóticas en los vertebrados son tan raras.
En los embriones de ratón, los genes HOX10, que es uno de los genes que se encuentran en la parte de la cola del animal, desactivan el sistema de "formación de costillas" cuando se activa el gen. Los genes están activos en la parte baja de la espalda, donde a las vértebras no les crecen costillas, e inactivos en la parte media de la espalda, lo que permite que se formen las costillas. Cuando los parálogos de HOX10 se inactivan experimentalmente, a las vértebras de la espalda baja les crecen costillas. [52] Esta investigación impulsó una búsqueda evolutiva de estas mutaciones entre todos los animales. Un ejemplo de esto son los lagartos y las serpientes. En las serpientes, los genes HOX10 han perdido de esa manera su capacidad de bloquear las costillas. [53]
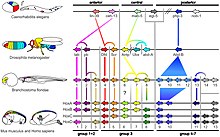
Los amphioxus como Branchiostoma floridae tienen un solo grupo Hox con 15 genes, conocido como AmphiHox1 a AmphiHox15 . [54]
Seis genes Hox están dispersos en el genoma de Caenorhabditis elegans , un gusano redondo . [10] : fig. 3 Hydra y Nematostella vectensis , ambas del filo Cnidaria , tienen algunos genes homeobox similares a Hox/ParaHox. [55] [11]
La expresión del gen Hox también se ha estudiado en braquiópodos , [56] anélidos , [57] y un conjunto de moluscos . [58]
Los genes Hox reciben ese nombre porque las mutaciones en ellos provocan transformaciones homeóticas . Las transformaciones homeóticas fueron identificadas y estudiadas por primera vez por William Bateson en 1894, quien acuñó el término "homeosis". Después del redescubrimiento de los principios genéticos de Mendel , Bateson y otros se dieron cuenta de que algunos ejemplos de homeosis en órganos florales y esqueletos de animales podían atribuirse a variaciones en los genes.
Se obtuvo evidencia definitiva de una base genética de algunas transformaciones homeóticas aislando mutantes homeóticos. El primer mutante homeótico fue encontrado por Calvin Bridges en el laboratorio de Thomas Hunt Morgan en 1915. Este mutante muestra una duplicación parcial del tórax y por ello se denominó Bithorax ( bx ). Transforma el tercer segmento torácico (T3) hacia el segundo (T2). Bithorax surgió espontáneamente en el laboratorio y desde entonces se ha mantenido continuamente como reserva de laboratorio. [59]
Los estudios genéticos de Morgan y otros proporcionaron la base para los análisis sistemáticos de Edward B. Lewis y Thomas Kaufman, que proporcionaron definiciones preliminares de los numerosos genes homeóticos de los complejos Bithorax y Antennapedia, y también demostraron que los fenotipos mutantes de la mayoría de estos Los genes podrían remontarse a patrones de defectos en el plan corporal embrionario.
Ed Lewis , Christiane Nüsslein-Volhard y Eric F. Wieschaus identificaron y clasificaron 15 genes de importancia clave para determinar el plan corporal y la formación de segmentos corporales de la mosca de la fruta D. melanogaster en 1980. [60] Por su trabajo, Lewis, Nüsslein-Volhard y Wieschaus recibieron el Premio Nobel de Fisiología o Medicina en 1995. [61]
En 1983, la homeobox fue descubierta de forma independiente por investigadores de dos laboratorios: Ernst Hafen, Michael Levine y William McGinnis (en el laboratorio de Walter Gehring en la Universidad de Basilea , Suiza) y Matthew P. Scott y Amy Weiner (en el laboratorio de Thomas Kaufman). laboratorio de la Universidad de Indiana en Bloomington ).
Los genes Hox desempeñan un papel fundamental en el desarrollo de estructuras como las extremidades, los pulmones, el sistema nervioso y los ojos. Como observaron TR Lappin y sus colegas en 2006, "la conservación evolutiva proporciona un alcance ilimitado para la investigación experimental del control funcional de la red del gen Hox, que está proporcionando importantes conocimientos sobre las enfermedades humanas". En el futuro, se podrán realizar más investigaciones para investigar las funciones de los genes Hox en la leucemia y el cáncer (como el COE). [38]