El interferón beta-1a (también interferón beta 1-alfa ) es una citocina de la familia del interferón que se utiliza para tratar la esclerosis múltiple (EM). [5] Es producido por células de mamíferos, mientras que el interferón beta-1b se produce en E. coli modificada . [6] Algunas investigaciones indican que las inyecciones de interferón pueden dar como resultado una reducción del 18 al 38 % en la tasa de recaídas de la EM. [7]
No se ha demostrado que el interferón beta desacelere el avance de la discapacidad. [8] [9] [10] [11] Los interferones no son una cura para la EM (no se conoce ninguna cura); la afirmación es que los interferones pueden retardar el progreso de la enfermedad si se inician tempranamente y se continúan mientras dure la enfermedad. [12]
La presentación clínica más temprana de la esclerosis múltiple remitente-recurrente es el síndrome clínicamente aislado (CIS), es decir, un ataque único de un solo síntoma. Durante un CIS, hay un ataque subagudo que sugiere desmielinización que debería incluirse en el espectro de fenotipos de EM. [13] El tratamiento con interferones después de un ataque inicial disminuye el riesgo de desarrollar EM clínica definitiva. [14] [15]
Los medicamentos son modestamente eficaces para disminuir el número de ataques en la esclerosis múltiple remitente-recurrente [16] y para reducir la acumulación de lesiones cerebrales, que se mide utilizando gadolinio : imágenes por resonancia magnética (IRM) mejoradas . [14] Los interferones reducen las recaídas en aproximadamente un 30% y su perfil seguro los convierte en los tratamientos de primera línea. [14] Sin embargo, no todos los pacientes responden a estas terapias. Se sabe que el 30% de los pacientes con EM no responden al interferón Beta. [17] Se pueden clasificar en no respondedores genéticos, farmacológicos y patogénicos. [17] Uno de los factores relacionados con la falta de respuesta es la presencia de altos niveles de anticuerpos neutralizantes del interferón beta . La terapia con interferón, y especialmente el interferón beta 1b, induce la producción de anticuerpos neutralizantes, generalmente en los segundos 6 meses de tratamiento, en entre el 5 y el 30% de los pacientes tratados. [14] Además, un subconjunto de pacientes con EMRR con EM especialmente activa, a veces denominada "EM que empeora rápidamente", normalmente no responden al interferón beta 1a. [18] [19]
Si bien se necesitan más estudios sobre los efectos a largo plazo de los medicamentos, [12] [14] los datos existentes sobre los efectos de los interferones indican que la terapia a largo plazo iniciada tempranamente es segura y está relacionada con mejores resultados. [12]
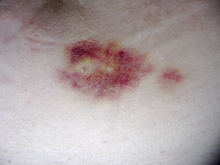
El interferón beta-1a está disponible sólo en formas inyectables y puede provocar reacciones cutáneas en el lugar de la inyección que pueden incluir necrosis cutánea . Las reacciones cutáneas con interferón beta son más comunes con la administración subcutánea y varían mucho en su presentación clínica. [20] Suelen aparecer dentro del primer mes de tratamiento, aunque su frecuencia e importancia disminuyen después de seis meses de tratamiento. [20] Las reacciones cutáneas son más frecuentes en las mujeres. [20] Las reacciones cutáneas leves normalmente no impiden el tratamiento, mientras que las necrosis aparecen en alrededor del 5% de los pacientes y conducen a la interrupción del tratamiento. [20] También con el tiempo, se puede desarrollar una abolladura visible en el lugar de la inyección debido a la destrucción local del tejido adiposo, conocida como lipoatrofia ; sin embargo, esto rara vez ocurre con el tratamiento con interferón. [21]
Los interferones , una subclase de citoquinas , se producen en el cuerpo durante enfermedades como la influenza para ayudar a combatir la infección. Son responsables de muchos de los síntomas de las infecciones por influenza, como fiebre , dolores musculares , fatiga y dolores de cabeza . [22] Muchos pacientes informan síntomas similares a los de la influenza horas después de tomar interferón beta que generalmente mejoran dentro de las 24 horas, estando dichos síntomas relacionados con el aumento temporal de citocinas. [14] [20] Esta reacción tiende a desaparecer después de 3 meses de tratamiento y sus síntomas pueden tratarse con medicamentos antiinflamatorios no esteroides de venta libre , como el ibuprofeno , que reducen la fiebre y el dolor. [20] Otro efecto secundario transitorio común con el interferón beta es un deterioro funcional de los síntomas ya existentes de la enfermedad. [20] Dicho deterioro es similar al que se produce en pacientes con EM debido al calor, la fiebre o el estrés ( fenómeno de Uhthoff ), suele aparecer dentro de las 24 horas posteriores al tratamiento, es más común en los primeros meses de tratamiento y puede durar varios días. [20] Un síntoma especialmente sensible a empeorar es la espasticidad . [20] El interferón beta también puede reducir el número de glóbulos blancos ( leucopenia ), linfocitos ( linfopenia ) y neutrófilos ( neutropenia ), además de afectar la función hepática . [20] En la mayoría de los casos, estos efectos no son peligrosos y son reversibles después de suspender o reducir el tratamiento. [20] Sin embargo, la recomendación es que todos los pacientes deben ser monitoreados mediante análisis de sangre de laboratorio , incluidas pruebas de función hepática , para garantizar el uso seguro de los interferones. [20]
Para ayudar a prevenir reacciones en el lugar de la inyección, se recomienda a los pacientes que roten los lugares de inyección y utilicen una técnica de inyección aséptica. Hay dispositivos de inyección disponibles para optimizar el proceso de inyección. Los efectos secundarios suelen ser lo suficientemente onerosos como para que muchos pacientes finalmente dejen de tomar interferones [ cita necesaria ] (o acetato de glatiramero , una terapia modificadora de la enfermedad comparable que requiere inyecciones regulares).
El interferón beta equilibra la expresión de agentes proinflamatorios y antiinflamatorios en el cerebro y reduce la cantidad de células inflamatorias que cruzan la barrera hematoencefálica . [23] En general, la terapia con interferón beta conduce a una reducción de la inflamación neuronal. [23] Además, también se cree que aumenta la producción del factor de crecimiento nervioso y, en consecuencia, mejora la supervivencia neuronal. [23] In vitro, el interferón beta reduce la producción de células Th17 , que son un subconjunto de linfocitos T que se cree que tienen un papel en la fisiopatología de la EM. [24]

Avonex fue aprobado en los EE.UU. en 1996, [25] y en la Unión Europea en 1997, y está registrado en más de 80 países en todo el mundo. [ cita necesaria ] Es la terapia líder para la EM en los EE. UU., con alrededor del 40% del mercado total, y en la Unión Europea, con alrededor del 30% del mercado total. [ cita necesaria ] Es producido por la empresa de biotecnología Biogen , originalmente bajo protección de competencia en los EE. UU. bajo la Ley de Medicamentos Huérfanos .
Avonex se vende en tres formulaciones: un polvo liofilizado que requiere reconstitución, un kit de jeringa para líquido premezclado y una pluma; se administra mediante inyección intramuscular . [1]
Rebif es un fármaco modificador de la enfermedad (DMD) que se utiliza para tratar la esclerosis múltiple en casos de síndromes clínicamente aislados, así como formas recurrentes de esclerosis múltiple, y es similar a la proteína interferón beta producida por el cuerpo humano. Merck Serono y Pfizer lo comercializan conjuntamente en los EE. UU. bajo una excepción a la Ley de Medicamentos Huérfanos . [ cita necesaria ] Fue aprobado en la Unión Europea en 1998 y en Estados Unidos en 2002; Desde entonces, ha sido aprobado en más de 90 países de todo el mundo, incluidos Canadá y Australia. [ cita necesaria ] Merck Serono tiene los derechos exclusivos de Rebif en los EE. UU. desde enero de 2016. [26] [27] Rebif se administra mediante inyección subcutánea . [2]
Cinnovex es la marca del interferón beta-1a recombinante, que se fabrica como biosimilar/biogenérico en Irán . Se produce en forma liofilizada y se vende con agua destilada para inyección. Cinnovex fue desarrollado en la Sociedad Fraunhofer en colaboración con CinnaGen y es la primera proteína terapéutica de un laboratorio Fraunhofer aprobada como medicamento biogenérico/biosimilar. Existen varios estudios clínicos que demuestran la similitud de CinnoVex y Avonex. [28] Actualmente, Vakzine Projekt Management (VPM) GmbH en Braunschweig, Alemania, está investigando una variante más soluble en agua.
Plegridy es una marca de una forma pegilada de interferón beta-1a. La ventaja de Plegridy es que sólo es necesario inyectarlo una vez cada dos semanas. [29]
Estrechamente relacionado con el interferón beta-1a está el interferón beta-1b , que también está indicado para la EM, pero está formulado con una dosis diferente y se administra con una frecuencia diferente. Cada medicamento tiene un perfil de seguridad/eficacia diferente. [30] El interferón beta-1b lo comercializa únicamente Bayer en los EE. UU. como Betaseron y fuera de los EE. UU. como Betaferon.
En los Estados Unidos, a partir de 2015 [actualizar], el costo es de entre 1284 y 1386 dólares estadounidenses por vial de 30 mcg. [31] A partir de 2020, el costo promedio nacional de adquisición de medicamentos (NADAC) en los Estados Unidos para Avonex fue de $ 6872,94 por un kit de 30 mcg. [32]
Avonex y Rebif se encuentran entre los diez medicamentos para la esclerosis múltiple más vendidos en 2013. [33]
Es un ejemplo de un medicamento especializado que sólo estaría disponible a través de una farmacia especializada . Esto se debe a que requiere una cadena de distribución refrigerada y cuesta 17.000 dólares al año. [34]
El interferón beta-1a administrado por vía subcutánea o intravenosa se investiga desde marzo de 2020 como tratamiento potencial en pacientes hospitalizados con COVID-19 en un ensayo multinacional Solidaridad (inicialmente en combinación con lopinavir ), pero no redujo la mortalidad hospitalaria en comparación con el estándar local de cuidado. [35]
Synairgen está desarrollando SNG001, una formulación para inhalación de interferón beta-1a, como tratamiento para COVID-19 . [36] [37] Un ensayo piloto en pacientes hospitalizados mostró mayores probabilidades de mejoría clínica con SNG001 en comparación con el placebo [38] y en enero de 2021 comenzó un ensayo de fase 3 en esta población. [39]