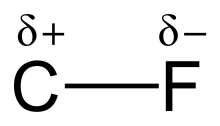Enlace carbono-flúor
Es el enlace más fuerte en química orgánica, y es relativamente corto debido a su carácter iónico parcial.
Esto introduce un carácter iónico al enlace a través de cargas parciales (Cδ+—Fδ−).
[3] Típicamente, la longitud de enlace carbono-flúor es aproximadamente 1,35 ángstroms (1,39 Å en el fluorometano).
La corta longitud de este enlace puede ser atribuida a las atracciones electrostáticas/carácter iónico entre las cargas parciales en el carbono y el flúor.
Cuando dos átomos de flúor están en átomos de carbono adyacentes, como en el 1,2-difluoroetano (FCH2CH2F), el confórmero gauche es más estable que el confórmero anti-esto es lo opuesto a lo que normalmente se esperaría ver y lo que es más observado para los etanos 1,2-disustituido; este fenómeno es conocido como el 'efecto gauche.
[9] Existen dos explicaciones principales para el efecto gauche: hiperconjugación y enlaces flexionados.
El traslape de orbitales reducido puede ser parcialmente compensado cuando se asume una conformación gauche, formando un enlace flexionado.
De estos dos modelos, se considera que la hiperconjugación es la principal causa detrás del efecto gauche en el difluoroetano.
Los corrimientos químicos en 19F-NMR aparecen en un rango muy amplio, dependiendo del grado de sustitución y grupo funcional.