Cloruro de acilo
Se les suele considerar como reactivos derivados de los ácidos carboxílicos.
Entonces: Cuando otros grupos funcionales tienen la prioridad, se toma a los cloruros de acilo como prefijos -clorocarbonil-:[1]
El intermediario iminio reacciona con el ácido carboxílico, abstrayendo un óxido, y regenerando el catalizador DMF.
Considere la comparación con su análogo ácido RCOOH: el ion cloruro es un excelente grupo saliente, mientras que el ion hidróxido no lo es en condiciones normales; esto es, incluso nucleófilos débiles atacan al carbonilo.
En contraste, las dos reacciones involucradas en preparar ésteres y amidas usando cloruros de acilo (formación del cloruro de acilo a partir del ácido carboxílico, seguido por condensación con el alcohol o amina) son rápidas y esencialmente irreversibles.
Son lacrimógenos debido a que pueden reaccionar con el agua de la superficie del ojo liberando ácido clorhídrico y ácidos orgánicos que irritan al ojo.

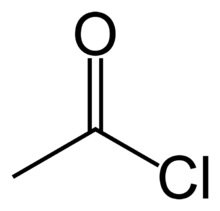
cloruro de acetilo o cloruro de etanoílo