El reordenamiento de Meyer-Schuster es la reacción química descrita como un reordenamiento catalizado por ácido de alcoholes propargílicos secundarios y terciarios a cetonas α,β-insaturadas si el grupo alquino es interno y aldehídos α,β-insaturados si el grupo alquino es terminal. [1] Swaminathan y Narayan, [2] Vartanyan y Banbanyan, [3] y Engel y Dudley han publicado reseñas , [4] la última de las cuales describe formas de promover el reordenamiento de Meyer-Schuster sobre otras reacciones disponibles para los alcoholes propargílicos. .
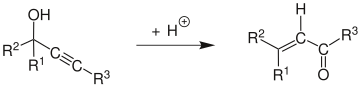

El mecanismo de reacción [5] comienza con la protonación del alcohol que sale en una reacción E1 para formar el aleno a partir del alquino . Al ataque de una molécula de agua sobre el carbocatión y a la desprotonación le sigue la tautomerización para dar el compuesto carbonílico α,β-insaturado .
Edens et al. han investigado el mecanismo de reacción. [6] Descubrieron que se caracterizaba por tres pasos principales: (1) la rápida protonación del oxígeno, (2) el paso lento que determina la velocidad , que comprende el desplazamiento 1,3 del grupo hidroxi protonado, y (3) la Tautomerismo cetoenol seguido de una rápida desprotonación.
En un estudio del paso limitante de la velocidad de la reacción de Meyer-Schuster, Andrés et al. demostró que la fuerza impulsora de la reacción es la formación irreversible de compuestos carbonílicos insaturados a través de iones carbonio . [7] También descubrieron que la reacción era asistida por el disolvente. Esto fue investigado más a fondo por Tapia et al. quienes demostraron que la jaula de solvente estabiliza el estado de transición. [8]
La reacción de alcoholes terciarios que contienen un grupo α- acetilénico no produce los aldehídos esperados, sino más bien metilcetonas α,β-insaturadas a través de un intermedio enino . [9] [10] Esta reacción alternativa se llama reacción de Rupe y compite con el reordenamiento de Meyer-Schuster en el caso de los alcoholes terciarios.


Si bien el reordenamiento tradicional de Meyer-Schuster utiliza condiciones duras con un ácido fuerte como catalizador, esto introduce competencia con la reacción de Rupe si el alcohol es terciario. [2] Se han utilizado con éxito condiciones más suaves con catalizadores basados en metales de transición y ácidos de Lewis (por ejemplo, catalizadores basados en Ru- [11] y Ag [12] ). Cadierno et al. informan el uso de radiación de microondas con InCl como catalizador para obtener excelentes rendimientos con tiempos de reacción cortos y una estereoselectividad notable . [13] A continuación se ofrece un ejemplo de su artículo:

El reordenamiento de Meyer-Schuster se ha utilizado en una variedad de aplicaciones, desde la conversión de ω-alquinil-ω-carbinol lactamas en enamidas usando PTSA catalítico [14] hasta la síntesis de tioésteres α,β-insaturados a partir de propargilo sustituido con γ-azufre. alcoholes [15] a la transposición de 3-alquinil-3-hidroxil-1H - isoindoles en condiciones ligeramente ácidas para dar compuestos carbonílicos α,β-insaturados. [16] Sin embargo, una de las aplicaciones más interesantes es la síntesis de una parte de paclitaxel de forma diastereoméricamente selectiva que conduce únicamente al E -alqueno. [17]

El paso mostrado anteriormente tuvo un rendimiento del 70 % (91 % cuando el subproducto se convirtió en el producto Meyer-Schuster en otro paso). Los autores utilizaron el reordenamiento de Meyer-Schuster porque querían convertir una cetona impedida en un alqueno sin destruir el resto de su molécula.