
Una proteína transmembrana es un tipo de proteína de membrana integral que abarca la totalidad de la membrana celular . Muchas proteínas transmembrana funcionan como puertas de entrada para permitir el transporte de sustancias específicas a través de la membrana. Con frecuencia sufren cambios conformacionales importantes para mover una sustancia a través de la membrana. Suelen ser muy hidrófobos y se agregan y precipitan en agua. Requieren de detergentes o disolventes apolares para su extracción, aunque algunos de ellos ( beta-barriles ) también pueden extraerse mediante agentes desnaturalizantes .
La secuencia peptídica que atraviesa la membrana, o el segmento transmembrana , es en gran medida hidrófoba y se puede visualizar mediante el gráfico de hidropatía . [1] Dependiendo del número de segmentos transmembrana, las proteínas transmembrana se pueden clasificar como proteínas de membrana de paso único o proteínas de membrana de paso múltiple. [2] Algunas otras proteínas integrales de membrana se denominan monotópicas , lo que significa que también están unidas permanentemente a la membrana, pero no la atraviesan. [3]
Hay dos tipos básicos de proteínas transmembrana: [4] barriles alfa-helicoidales y beta . Las proteínas alfa-helicoidales están presentes en las membranas internas de las células bacterianas o en la membrana plasmática de las células eucariotas y, a veces, en la membrana externa bacteriana . [5] Esta es la categoría principal de proteínas transmembrana. En los seres humanos, se estima que el 27% de todas las proteínas son proteínas de membrana de hélice alfa. [6] Las proteínas beta-barril se encuentran hasta ahora sólo en las membranas externas de las bacterias gramnegativas , las paredes celulares de las bacterias grampositivas , las membranas externas de las mitocondrias y los cloroplastos , o pueden secretarse como toxinas formadoras de poros . Todas las proteínas transmembrana del barril beta tienen una topología ascendente y descendente más simple, que puede reflejar su origen evolutivo común y su mecanismo de plegado similar. [ cita necesaria ]
Además de los dominios proteicos, existen elementos transmembrana inusuales formados por péptidos. Un ejemplo típico es la gramicidina A , un péptido que forma una hélice β transmembrana dimérica. [7] Este péptido es secretado por bacterias grampositivas como antibiótico . No se ha informado de una hélice transmembrana de poliprolina-II en proteínas naturales. No obstante, esta estructura se observó experimentalmente en péptidos artificiales diseñados específicamente. [8]
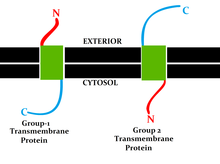
Esta clasificación se refiere a la posición de los extremos N y C de las proteínas en los diferentes lados de la bicapa lipídica . Los tipos I, II, III y IV son moléculas de paso único . Las proteínas transmembrana de tipo I están ancladas a la membrana lipídica con una secuencia de anclaje de parada de transferencia y tienen sus dominios N-terminales dirigidos a la luz del retículo endoplásmico (RE) durante la síntesis (y al espacio extracelular, si las formas maduras se encuentran en las membranas celulares ). . Los tipos II y III están anclados con una secuencia de anclaje de señal, con el tipo II dirigido a la luz del RE con su dominio C-terminal, mientras que el tipo III tiene sus dominios N-terminales dirigidos a la luz del RE. El tipo IV se subdivide en IV-A, con sus dominios N-terminales dirigidos al citosol y IV-B, con un dominio N-terminal dirigido a la luz. [9] Las implicaciones para la división en los cuatro tipos son especialmente manifiestas en el momento de la translocación y la traducción unida al RE, cuando la proteína debe pasar a través de la membrana del RE en una dirección que depende del tipo. [ cita necesaria ]

Las estructuras de las proteínas de membrana se pueden determinar mediante cristalografía de rayos X , microscopía electrónica o espectroscopia de RMN . [11] Las estructuras terciarias más comunes de estas proteínas son el haz de hélice transmembrana y el barril beta . La porción de las proteínas de membrana que están unidas a la bicapa lipídica (ver capa lipídica anular ) consiste principalmente en aminoácidos hidrofóbicos. [12]
Proteínas de membrana que tienen superficies hidrofóbicas, son relativamente flexibles y se expresan en niveles relativamente bajos. Esto crea dificultades para obtener suficiente proteína y luego hacer crecer cristales. Por lo tanto, a pesar de la importante importancia funcional de las proteínas de membrana, determinar las estructuras de resolución atómica para estas proteínas es más difícil que las proteínas globulares. [13] En enero de 2013, menos del 0,1% de las estructuras proteicas determinadas eran proteínas de membrana a pesar de representar entre el 20% y el 30% del proteoma total. [14] Debido a esta dificultad y a la importancia de esta clase de proteínas, se han desarrollado métodos de predicción de la estructura de las proteínas basados en gráficos de hidropatía, la regla interna positiva y otros métodos. [15] [16] [17]
Las proteínas transmembrana de hélice alfa (helicoidal α) son inusualmente estables a juzgar por los estudios de desnaturalización térmica , porque no se despliegan completamente dentro de las membranas (el despliegue completo requeriría romper demasiados enlaces H de hélice α en los medios no polares). Por otro lado, estas proteínas se pliegan mal fácilmente , debido a la agregación no nativa en las membranas, la transición a estados de glóbulos fundidos , la formación de enlaces disulfuro no nativos o el despliegue de regiones periféricas y bucles no regulares que son localmente menos estables. [ cita necesaria ]
También es importante definir adecuadamente el estado desplegado . El estado desplegado de las proteínas de membrana en las micelas de detergente es diferente al de los experimentos de desnaturalización térmica . [ cita necesaria ] Este estado representa una combinación de hélices α hidrofóbicas plegadas y segmentos parcialmente desplegados cubiertos por el detergente . Por ejemplo, la bacteriorrodopsina "desplegada" en las micelas de SDS tiene cuatro hélices α transmembrana plegadas, mientras que el resto de la proteína está situada en la interfaz micela-agua y puede adoptar diferentes tipos de estructuras anfifílicas no nativas . Las diferencias de energía libre entre los estados nativo y desnaturalizado con detergente son similares a las estabilidades de las proteínas solubles en agua (< 10 kcal/mol). [ cita necesaria ]
El replegamiento de proteínas transmembrana de hélice α in vitro es técnicamente difícil. Hay relativamente pocos ejemplos de experimentos de replegamiento exitosos, como ocurre con la bacteriorrodopsina . In vivo , todas estas proteínas normalmente se pliegan de forma cotraduccional dentro del gran translocón transmembrana . El canal translocón proporciona un entorno muy heterogéneo para las hélices α transmembrana nacientes. Una hélice α anfifílica relativamente polar puede adoptar una orientación transmembrana en el translocón (aunque estaría en la superficie de la membrana o desplegada in vitro ), porque sus residuos polares pueden mirar hacia el canal central lleno de agua del translocón. Este mecanismo es necesario para la incorporación de hélices α polares en estructuras de proteínas transmembrana. Las hélices anfifílicas permanecen unidas al translocón hasta que la proteína se sintetiza y se pliega por completo. Si la proteína permanece desplegada y unida al translocón durante demasiado tiempo, es degradada por sistemas celulares específicos de "control de calidad". [ cita necesaria ]
La estabilidad de las proteínas transmembrana de barril beta (barril β) es similar a la estabilidad de las proteínas solubles en agua, según estudios de desnaturalización química. Algunos de ellos son muy estables incluso en agentes caotrópicos y altas temperaturas. Su plegamiento in vivo se ve facilitado por chaperonas solubles en agua , como la proteína Skp. Se cree que las proteínas de la membrana del barril β provienen de un ancestro incluso con un número diferente de láminas que podrían agregarse o duplicarse durante la evolución. Algunos estudios muestran una enorme conservación de secuencias entre diferentes organismos y también aminoácidos conservados que mantienen la estructura y ayudan con el plegamiento. [18]
Nota: n y S son, respectivamente, el número de cadenas beta y el "número de corte" [20] del barril beta.